Красные кристаллы
Выращиваем кристаллы из красной кровяной соли!
Реагенты
Безопасность
- Перед началом опыта наденьте защитные перчатки и очки.
- Проводите эксперимент на подносе.
- Соблюдайте меры предосторожности при работе с кипятком.
- Не допускайте попадания химических реагентов в глаза или рот.
- Не допускайте к месту проведения экспериментов людей без защитных очков, а также маленьких детей и животных.
- Храните экспериментальный набор в месте, недоступном для детей младше 10 лет.
- Помойте или очистите всё оборудование и оснастку после использования.
- Убедитесь, что все контейнеры с реагентами плотно закрыты и хранятся по правилам после использования.
- Убедитесь, что все одноразовые контейнеры правильно утилизированы.
- Используйте только оборудование и реактивы, поставляемые в наборе или рекомендуемые текущими инструкциями.
- Если вы использовали контейнер для еды или посуду для проведения экспериментов, немедленно выбросьте их. Они больше не пригодны для хранения пищи.
- В случае попадания реагентов в глаза тщательно промойте глаза водой, при необходимости держа глаз открытым. Немедленно обратитесь к врачу.
- В случае проглатывания реагентов промойте рот водой, выпейте немного чистой воды. Не вызывайте рвоту. Немедленно обратитесь к врачу.
- В случае вдыхания реагентов выведите пострадавшего на свежий воздух.
- В случае контакта с кожей или ожогов промывайте поврежденную зону большим количеством воды в течение 10 минут или дольше.
- В случае сомнений немедленно обратитесь к врачу. Возьмите с собой химический реагент и контейнер от него.
- В случае травм всегда обращайтесь к врачу.
- Неправильное использование химических реагентов может вызвать травму и нанести вред здоровью. Проводите только указанные в инструкции эксперименты.
- Данный набор опытов предназначен только для детей 10 лет и старше.
- Способности детей существенно различаются даже внутри возрастной группы. Поэтому родители, проводящие эксперименты вместе с детьми, должны по своему усмотрению решить, какие опыты подходят для их детей и будут безопасны для них.
- Родители должны обсудить правила безопасности с ребенком или детьми перед началом проведения экспериментов. Особое внимание следует уделить безопасному обращению с кислотами, щелочами и горючими жидкостями.
- Перед началом экспериментов очистите место проведения опытов от предметов, которые могут вам помешать. Следует избегать хранения пищевых продуктов рядом с местом проведения опытов. Место проведения опытов должно хорошо вентилироваться и находиться близко к водопроводному крану или другому источнику воды. Для проведения экспериментов потребуется устойчивый стол.
- Вещества в одноразовой упаковке должны быть использованы полностью или утилизированы после проведения одного эксперимента, т.е. после открытия упаковки.
Часто задаваемые вопросы
Такое возможно. Вылейте раствор в чашку Петри, оставляя нерастворимый остаток в стакане.
Подождите еще чуть-чуть — ваши кристалы в конце концов вырастут!
Возможно, это произошло из-за загрязнения пылью или смены температур в процессе их образования.
Не расстраивайтесь! Все можно исправить. Подождите, пока кристаллы не сформируются окончательно. Затем растворите их же в 10 мл кипящей воды и вылейте полученный раствор в чашку Петри. Постарайтесь как-нибудь защитить его от пыли и смены температуры воздуха.
Покройте кристаллы бесцветным лаком для ногтей. После того, как лак высохнет, спрячьте их в плотно закрывающийся контейнер.
В данном случае, перелейте раствор обратно в стакан и хорошенько промойте чашку Петри водой. Осторожно вылейте раствор снова в чашку Петри, но в этот раз уже без осадка.
Другие эксперименты
Пошаговая инструкция
Растворите в горячей воде немного гексацианоферрата(III) калия K3[Fe(CN)6]. Он гораздо лучше растворяется в горячей воде, чем в холодной, поэтому с нагревом насыщенный раствор получится быстрее.
Оставьте раствор K3[Fe(CN)6], чтоб он остыл, а вода из него стала испаряться.
Ожидаемый результат
Раствор красной кровяной соли остывает, и из него испаряется вода. При этом образуются необычные красные кристаллы.
Утилизация
Утилизируйте твёрдые отходы эксперимента вместе с бытовым мусором.
Что произошло
Как правило, в горячей воде растворяется бóльшее количество веществ, чем в холодной. Пока раствор постепенно остывает, а вода испаряется из чашки Петри, ионы придвигаются теснее к друг другу и, соответственно, не могут перемещаться так же легко, как и раньше. Они сталкиваются с друг другом и слипаются. С объединением ионов образуются и кристаллы. Постепенно они становятся крупнее и виднее!
Как образуются кристаллы?
Образование кристалла — это торжество порядка над хаосом. Ведь кристаллы отличаются удивительной правильностью и точностью строения, одинакового в любой его части.
Кристаллы бывают разной природы. Они могут состоять из молекул (например, как сахар) или из ионов (как поваренная соль NaCl). Такие кристаллы, как алмаз или кварц, состоят из прочно соединенных с соседями атомов. Особняком стоят кристаллы металлов. Да-да, металлы тоже могут образовывать кристаллы: в них атомы металлов связаны между собой общим для всего кристалла «облаком» электронов. Встречаются и более сложные кристаллы — они содержат как ионы, так и молекулы. Есть и такие кристаллы, которые состоят из непрерывных цепочек атомов, в том числе атомов металлов.
Мир вокруг нас находится в постоянном движении. На его фоне кристаллы выглядят столпами неизменности и постоянства. Как же они могут возникнуть из круговорота природы, который не останавливается ни на секунду?
Рост любого кристалла можно сравнить со строительством кирпичного здания. Если просто высыпать все кирпичи в одном месте, они останутся лишь грудой кирпичей. Но если набраться терпения и действовать последовательно, внимательно выкладывая кирпич за кирпичом, можно возвести надежные стены. Так и с кристаллами: при правильном изменении условий в растворе формируются красивые упорядоченные структуры. Правда, в отличие от настоящих кирпичей, «кирпичики», из которых состоят кристаллы, сами могут скрепляться между собой без дополнительного связующего материала.
Например, ионы с противоположными зарядами притягиваются друг к другу. Их чередование в кристалле приводит к тому, что отталкивание одноименно заряженных ионов с лихвой компенсируется притягиванием «разноименных».
Именно так происходит и в случае кристаллов красной кровяной соли — гексацианоферрата(III) калия K3[Fe(CN)6].
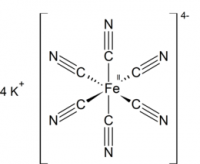
Ещё в первой половине двадцатого века люди научились изучать структуру кристаллов: определять взаимное расположение атомов и молекул в его составе и точно измерять расстояние между ними. Так, исследование кристаллов красной кровяной соли, которые мы получали в этом опыте, показывает, что каждый отрицательно заряженный ион [Fe(CN)_6] 3– окружен шестью положительно заряженными ионами K + , тогда как ионы K + окружены тремя-четырьмя отрицательно заряженными ионами. Их связывает электростатическое притяжение, которое не позволяет кристаллу рассыпаться в порошок. Хотя каждый такой кристалл можно в конечном счете превратить в мелкую пыль, для этого придется изрядно потрудиться.
Почему же в этом опыте образуются кристаллы красной кровяной соли?
В нашем опыте воды столько, что красная кровяная соль почти полностью растворяется в ней только при высокой температуре (почти 100 °С). Постепенно раствор остывает, составляющим соль ионам становится в нем тесно, и они стремятся его покинуть.
Можно ли растворить кристаллы и повторить опыт?
Да, кристаллы можно растворить и повторить эксперимент. Кристаллы красной кровяной соли растворимы в воде.
Подпишитесь на наборы MEL Chemistry и проведите эти опыты у себя дома!
Источник
Желтая кровяная соль
| Калий железистосинеродистый | |
|---|---|
 | |
 |
наименование
тригидрат — бледно-жёлтые кристаллы
650 °C