Вопрос 32. Кислотность почв, её виды, расчёт доз извести.



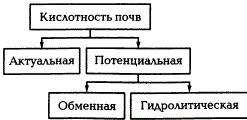
Состав поглощенных ионов определяет многие свойства почв, например, кислотность и щелочность. Различают следующие формы или виды почвенной кислотности: актуальная кислотность; потенциальная кислотность, которая подразделяется на обменную и гидролитическую кислотность.
Актуальная кислотность. Эта форма кислотности наиболее проста для понимания; так называют кислотность почвенного раствора, обусловленную растворенными в нем компонентами. На практике редко измеряют рН почвенного раствора. Вместо этого анализируют водные вытяжки или водные суспензии почв. Согласно решению, II Международного конгресса почвоведов, водные вытяжки и суспензии для измерения рН готовят при отношении почва: вода, равном 1: 2,5. Для торфянистых почв и торфов это отношение расширяют до 1: 25.
Степень кислотности почвенных растворов, вытяжек и суспензий оценивают величиной рН, количество кислотности — по содержанию титруемых щелочью веществ, обладающих кислотными свойствами.
Кислотность почвенных растворов обусловлена присутствием свободных органических кислот или других органических соединений, содержащих кислые функциональные группы, свободных минеральных кислот (главным образом угольной кислоты), а также других компонентов, проявляющих кислотные свойства. В числе последних наибольшее влияние оказывают ионы А1 3+ и Ре 3+ , причем их кислотные свойства соизмеримы с кислотными свойствами таких кислот, как угольная и уксусная.
По данным И.Н. Скрынниковой, в кислых почвенных растворах дерново-подзолистых почв содержатся:
• свободные нелетучие органические кислоты;
• соли сильных оснований и слабых органических кислот;
• свободный СО2 и соли угольной кислоты;
• аммонийные соли слабых органических кислот. Сочетание этих компонентов в почвенных растворах обусловливает значение рН в интервале 4,2—6,8.
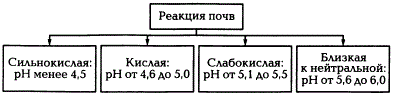
По степени кислотности почвы подразделяются на очень сильнокислые (рН ниже 4,0), сильнокислые (4,1—4,5), кислые (4,6—5,2), слабокислые (5,3—6,4), нейтральные и близкие к нейтральным (6,5—7,4) и щелочные (свыше 7,5). Почвенная кислотность неблагоприятна для жизнедеятельности растений и микроорганизмов, поэтому для ее устранения применяют известкование почв. При внесении извести в почву поглощенный водород замещается кальцием. Дозы извести: т/га = 1,5Н. Также в качестве сырья вносят мергель, долонит, мел.
Способность почвы подкислять почвенный раствор обусловлена наличием в почве кислот, гидролитически кислых солей, а также поглощенных ионов водорода и алюминия.
Кислотность почвы вызывается ионами водорода. В зависимости от того, в каком состоянии ионы водорода находятся в почве, кислотность может быть активной (актуальной) и потенциальной.
Активная (актуальная) кислотность зависит от концентрации свободных ионов водорода в почвенном растворе. Их источником являются органические кислоты, образующиеся при разложении растительных остатков, и угольная кислота, появляющаяся в почве при растворении диоксида углерода в воде.
Кислую реакцию имеют подзолистые, дерново-подзолистые и болотные почвы, нейтральную – черноземы, щелочную – каштановые почвы, сероземы и солонцы.
Для определения активной кислотности почву заливаю дистиллированной водой, взбалтывают, фильтруют и в полученном растворе с помощью индикатора рН-метра определяют рН.
Потенциальная кислотность подразделяется на обменную и гидролитическую. Она обусловлена содержанием ионов водорода и алюминия, находящихся в поглощенном состоянии.
Обменная кислотность обусловлена содержанием поглощенных ионов водорода, которые могут быть вытеснены из ППК раствором нейтральной соли КСl. Также её создают поглощенные ионы алюминия, которые вытесняются из ППК катионами нейтральной соли и переходят в раствор. Обменная кислотность сильно выражена в кислых подзолистых и дерново-подзолистых почвах, а в нейтральных и щелочных почвах она не проявляется.
Гидролитическая кислотность зависит от содержания как обменных, так и прочносвязанных ионов водорода. Для определения гидролитической кислотности почву обрабатывают ацетатом натрия.
ДОЗА ИЗВЕСТИ=1.5НГ, Hг-гидролитическая кислотность(сумма ионов водорода)

Виды сырья для понижения кислотности — катионы кальция магния повышают плодородие почв, нейтрализуют кислую реакцию и создают цельную структуру. Катионы водорода разрушают структуру и повышают кислотность почв. Катиона натрия повышают щелочность.
Применение половинных доз извести (0,5 Нг) обеспечивает в первой ротации севооборота прибавку урожая примерно 70% от полной дозы, а во второй ротации — 40-50%. Внесение более высоких доз извести (>1,0 Нг) неэффективно, поскольку прибавки урожая незначительны, а затраты и потери кальция из почвы вследствие вымывания осадками возрастают. Полную дозу извести определяют по величине гидролитической кислотности:
Д = (Нг ∙ Эм ∙ 10 ∙ 3 000 000)/1 000 000 000 = (Нг ∙ Эм ∙ 3)/100, где: Д — доза извести, т/га; Нг — гидролитическая кислотность по Каппену, мг-экв/100 г почвы; Эм — эквивалентная масса известкового удобрения; 10 — коэффициент для пересчета Нг в мг-экв/кг почвы; 3000000 — масса 1 га пахотного слоя почвы, кг; 1 000 000 000 — коэффициент пересчета мг в тонны.
Если в качестве известкового удобрения используется СаСО3 , то формула приобретает вид: СаСО3, т/га = 1,5 Нг.
Дозы извести можно также рассчитать по формуле: Д = 0,05 ∙ Нг ∙ d ∙ h, где Д — доза СаСО3, т/га; Нг — гидролитическая кислотность, мг-экв/100 г почвы; d-объемная масса почвы, г/см 3 ; h — глубина пахотного слоя, см.
Метод определения доз извести по гидролитической кислотности принят в РФ и многих других странах в качестве основного (стандартного) для дерново-подзолистых, серых лесных почв, оподзоленных и выщелоченных и черноземов. В производственных условиях дозы извести часто устанавливают, пользуясь справочными таблицами, по рН солевой вытяжки (1 н. KCl) и гранулометрическому составу почвы.
В отличие от минеральных почв, торфяно-болотные почвы имеют обычно высокую потенциальную кислотность, однако они практически не содержат в ППК обменный алюминий. Их кислотность обусловлена в основном ионами водорода, поэтому, несмотря на большую величину гидролитической кислотности, она менее токсична для растений. Эти почвы обладают большой буферной способностью и при рНKCl более 5,2 в известковании не нуждаются.
В севооборотах, в структуре которых преобладают культуры слабо чувствительные к кислотности почвы (картофель, лен, рожь, овес, козлятник, люпин, сераделла и другие) не требуется полное устранение кислотности. В таких севооборотах необходимо поддерживать оптимальную для культур слабокислую реакцию (рНKCl) почвы. Дозы СаСО3 для достижения заданного уровня реакции почвы рассчитывают по формуле Д = 10 dpH∙M, где Д — доза СаСО3, т/га; dpН — планируемый сдвиг рН; 10 — коэффициент; М — норма расхода СаСО3, т/га для сдвига рН на 0,1. Затраты (нормативы) СаСО3 для доведения кислотности почвы до заданного значения.
При возделывании в севооборотах люцерны, сахарной и кормовой свеклы, капусты и других культур, относящихся к первой группе, почву известкуют при Нг выше 2 мг-экв и степени насыщенности основаниями менее 90%. Дозы извести для этих почв устанавливают по величине гидролитической кислотности.
При определении необходимости известкования почвы следует учитывать не только гидролитическую кислотность и степень насыщенности основаниями, но и активность Н+ почвенного раствора, поскольку непосредственное негативное воздействие на сельскохозяйственные культуры оказывает не общее количество ионов водорода в ППК, а концентрация (активность) ионов водорода.
Известковые удобрения (известняковая и доломитовая мука, металлургические шлаки и др.) существенно различается по химическому составу, тонине помола и механическим примесям, поэтому их действие оценивают по нейтрализующей способности. Нейтрализующее действие известковых удобрений зависит от содержания в них карбонатов (СаСО3 и МgСО3), механических примесей, влаги, размера частиц (тонины помола) и их прочности. Для агрохимической оценки качества известковых удобрений определяют «активно действующее вещество» (АДВ) по формуле (%): АВД = (Х ∙ (100 — Н) ∙ (100 — Х1)) / (100 ∙ 100), где Х — суммарная массовая доля карбоната кальция и магния; Н — содержание недеятельной фракции извести — для металлургических шлаков, известняковой и доломитовой муки частиц крупнее 1 мм, для меловой муки — крупнее 3 мм; Х1 — массовая доля влаги, %. Доза известкового удобрения в физической массе рассчитывается по следующей формуле: Дф = (Др ∙ 100)/АВД, т/га, где Дф — доза известкового удобрения в физической массе, т/га; Др — доза рассчитанная на 100% содержание карбонатов; АДВ — содержание активно действующего вещества, %; 100 — коэффициент.
Источник
Кислотность как фактор, влияющий на плодородие почвы
Кислотность почвы – важный агрохимический параметр, характеризующий пригодность субстрата для выращивания тех или иных культур. Начинающие огородники часто совершают ошибку – регулируют рН на всем участке, в то время, когда нужно создавать оптимальные условия для каждого растения индивидуально. Рассмотрим связь уровня кислотности с плодородием почвы и урожайностью культур.

Кислотность и показатели рН почвы
Кислотность или ph почвы – биохимический показатель, который характеризует ее способность проявлять (нейтрализовать) свойства кислот. В процессе обмена ионов водорода с почвенными минералами и органическими веществами в плодородном слое образуются кислоты и основания (щелочи). РН указывает на их баланс в почвенном растворе, обозначают его числами от 1 до 14. Чем ниже числовое обозначение pH, тем кислее среда. От чего зависит кислотность почвы?
Определяющий фактор – изначальный материал, из которого сформированы почвы: на песчанике, граните – более кислые, на известняке – щелочные.
Постепенное повышение кислотности происходит в регионах с частыми обильными осадками. Влага, накапливаясь в почве, вымывает минералы и соли из корнеобитаемого слоя.
Причиной выщелачивания может быть интенсивный полив водой с низким показателем рН (кислой).
Подкисление происходит при чрезмерном внесении в землю растительных остатков, органических и минеральных удобрений.
Увеличению кислотности способствует плохая воздухопроницаемость грунта. Если органика разлагается без доступа кислорода, освобождаемые в результате химической реакции органические кислоты и углекислый газ остаются в почве.
Интересно! В РФ примерно треть сельскохозяйственных земель – кислые и требуют регулярного известкования. Это большая часть дерново-подзолистых, дерновых и серых лесных почв средней полосы и Сибири. В Западной Европе таких земель почти 60 %.
Рассмотрим оптимальные показатели кислотности почвы для растений, а ниже в таблице конкретизируем их в разрезе садовых и огородных культур.
Наиболее приемлемый для большинства культурных растений уровень кислотности находится в диапазоне от 5,5 до 7,5 – это слабокислые (5–6), нейтральные (6,5–7) и слабощелочные(7–8) почвы. РН ниже 5 означает средне и сильнокислую реакцию, выше 8 – щелочную. Кислотно-щелочной баланс выше 9 говорит о том, что перед нами солонцово-карбонатные почвы или даже солончаки.
Оптимальный диапазон кислотности для распространенных садово-огородных культур
Источник
Кислотность почв
Кислотно-щелочная характеристика, или реакция, — это способность почв проявлять свойства кислот и щелочей при взаимодействии с водой или растворами солей. Мерой реакции почв является соотношение в почвенном растворе водородных (Н + ) и гидроксильных (ОН — ) ионов. Реакция почв характеризуется величиной pH — отрицательным логарифмом активности водородных ионов в растворах. Почвы могут иметь кислую (pH 7) реакцию.
Различают два вида почвенной кислотности: актуальную и потенциальную, которая в свою очередь подразделяется на обменную и гидролитическую.
Виды кислотности почв
Актуальной кислотностью называется кислотность почвенного раствора. Она измеряется при взаимодействии почвы с дистиллированной водой (pHH2O). Актуальная кислотность зависит от наличия в почвенном растворе свободных органических и минеральных кислот (главным образом, угольной кислоты). Актуальная кислотность в почвах проявляется в диапазоне pH от 3 до 7.
Обменная кислотность обусловлена наличием в ППК обменных водорода и алюминия и определяется путем вытеснения ионов Н + и Аl 3+ раствором нейтральной соли КСl. Степень кислотности оценивают по величине pH солевой вытяжки. Обменная кислотность всегда больше актуальной. В почвах с ППК, насыщенны основаниями, обменная кислотность не определяется. Наиболее сильно она выражена в подзолистых почвах и краснозёмах. Существует четыре градации потенциальной кислотности почв, характеризуемой рНКСl.
Градации кислотности почв
Гидролитическая кислотность определяется путем воздействия на почву гидролитически щелочной соли. При взаимодействии почвы с солью происходит более полное вытеснение из ППК обменных водорода и алюминия. Для определения гидролитической кислотности принято использовать 1,0 н. раствор CH3COONa. Он выражается в мг-экв на 100 г почвы.
По величине гидролитической кислотности (Н) находят необходимую для известкования почвы дозу извести и рассчитываю степень насыщенности почвы основаниями (V, %):
где S — сумма поглощенных оснований.
Почвы, обладающие кислотностью, распространены очень широко в бореальном поясе, а также в условиях влажных субтропиков и тропиков.
В Российской Федерации в конце XX в. кислые почвы занимал 51 млн га сельскохозяйственных угодий, в том числе 43 % всей пашни. Среди них преобладают сильно- и среднекислые почвы (рНКСl менее 5,0), площадь которых составляла 28 млн га. Во многих странах площади, занятые кислыми почвами, увеличиваются, и растет степень их кислотности. Причин тому несколько. Одна из них — внесение минеральных, часто физиологически кислых удобрений, не сопровождаемое необходимым известкованием.
Для многих, особенно промышленных, регионов характерно выпадение кислых и даже сильнокислых дождевых осадков с pH примерно 4,0—4,5, содержащих серную и частично азотную кис-лоты. Кислые дожди служат дополнительным фактором ускорения развития кислотности почв. В Нечерноземной зоне РФ потери СаCO3 в результате антропогенного подкисления почв достигают 400—450 кг/га в год.
Негативное влияние повышенной кислотности на растения обусловлено несколькими причинами, среди которых наибольшее значение имеют следующие:
- недостаток Са 2+ — необходимого для растений элемента питания;
- повышенная концентрация ионов Аl 3+ , Мn 2+ , Н + ;
- изменение доступности растениям макро — и микроэлементов питания;
- изменение физических свойств почвы.
От величины pH зависят подвижность и доступность растениям практически всех элементов питания. Усвояемость фосфора максимальна при pH = 6,5, снижаясь как в более кислой, так и в щелочной среде. Только в сильнощелочных почвах при pH около 9 и выше растворимость фосфатов вновь возрастает.
В кислых почвах повышается растворимость соединений железа, марганца, алюминия, бора, меди, цинка. При избытке этих элементов продуктивность растений снижается. В то же время высокая кислотность понижает доступность такого важного микроэлемента, как молибден.
Оптимальный интервал pH связан не только с растворимостью почвенных компонентов, но и с физиологическими особенностями возделываемых культур. Для одних растений оптимум pH лежит в интервале 4,0 — 5,0 (чайный куст, клюква), для других — от 6,0 до 8,0 (вишня, груша, орех грецкий, слива, яблоня). Для снижения поденной кислотности в качестве химических мелиорантов используют различные материалы. Наиболее употребительны осадочные породы, состоящие преимущественно из кальцита, доломита СаМn(СO3)2, доломитизированные известняки, мергели. Кроме того, применяют известковые туфы и различные промышленные отходы: дефекат (отход свеклосахарного производства), другие шлаки. В большинстве мелиорантов действующим веществом является СаСО3.
С химической точки зрения карбонат кальция является лучшим средством для снижения почвенной кислотности.
При внесении карбоната кальция в кислую почву происходят реакции:
В результате этих реакций создаются наиболее благоприятные условия: почвенный поглощающий комплекс насыщается кальцием, а в почвенном растворе образуется слабая угольная кислота.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Источник