Статьи
Как вырастить колонии бактерий в чашке Петри в домашних условиях
У Вас появился инвертированный биологический микроскоп Эврика 40х-320х! Вы изучили под ним воду из канавы, воду из вазы с букетом цветов… Вы посмотрели все, что можно было быстро налить в чашечку Петри. Что же теперь? Давайте попробуем провести настоящие научные исследования. От Вас потребуется терпение, время и фантазия.
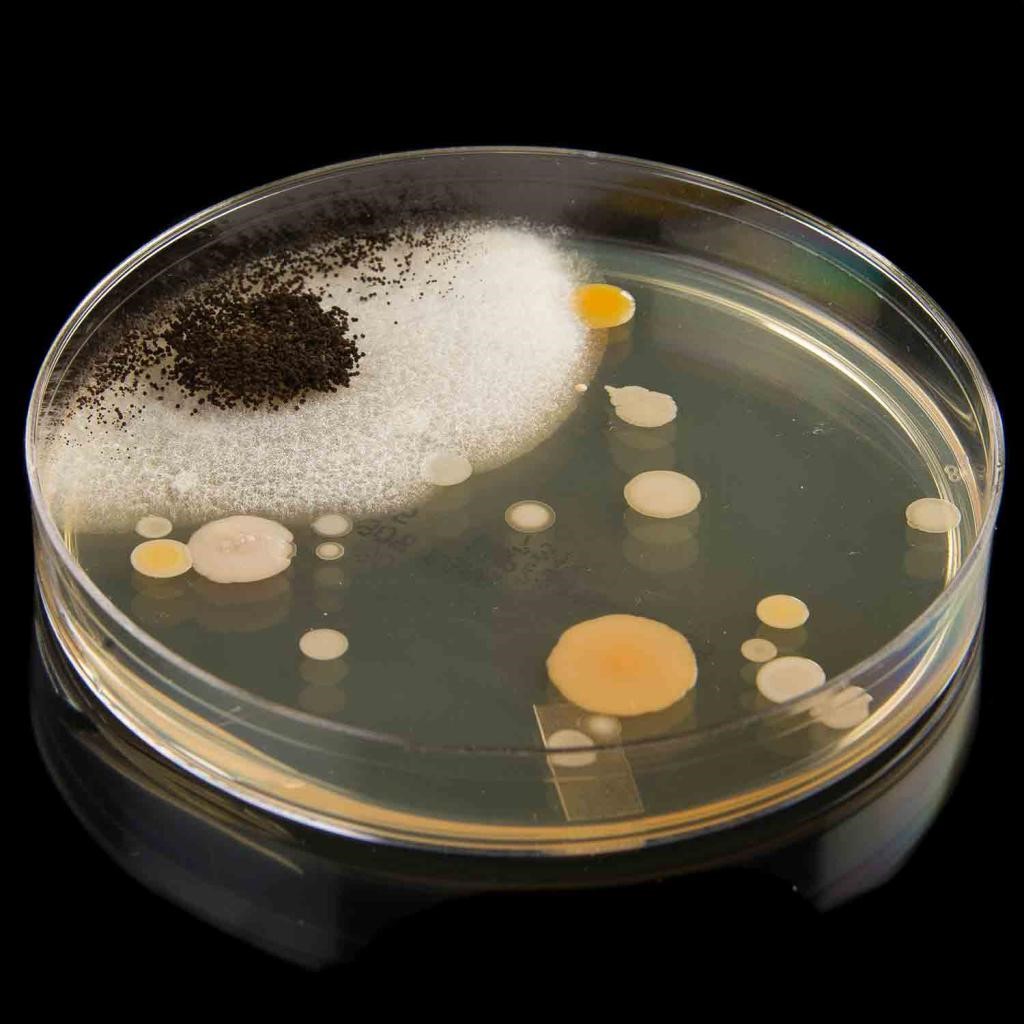
Мы вырастим колонии бактерий в чашечке, которая идет в комплекте с микроскопом. Вы можете приобрести несколько чашек, чтобы выращивать несколько разных колоний одновременно. Думаю, Вы будете поражены разнообразием бактерий, которые окружают нас.
Будьте осторожны! Эти опыты рекомендуются для детей старше 8 лет и только под наблюдением взрослых! Опыты включают использование кипящей воды и хлорки. Взрослый контроль обязателен!
• Порошок агар-агар. Он продается в продуктовых магазинах в том же отделе, где ванилин, желатин, корица и другие вкусности для выпечки.
• 1 чайная ложка сахара.
• Маленькая кастрюлька или ковшик для кипящей смеси.
• Инкубатор. В качестве инкубатора мы будем использовать какое-нибудь теплое место. Зимой удобно использовать место рядом с обогревателем. А летом, когда батареи выключены, можно использовать место за холодильником.
Для начала не забываем пригласить взрослого человека присоединиться к нашему опыту. Нам очень потребуется его помощь.
1. Наливаем воду в кастрюлю (ковшик) и доводим до кипения. Растворяем сахар в этой воде.
2. Добавляем порошок агар-агар в кипящую воду и перемешиваем в течение минуты, пока он полностью растворится.
3. Охлаждаем смесь в течение нескольких минут. Во-первых, смесь должна быть еще горячей, чтобы избежать установки желе прямо в кастрюле. А во-вторых, нам необходимо предотвратить загрязнение нашей смеси бактериями из воздуха. Наши домашние условия далеки от стерильности, но мы постараемся избежать лишних загрязнений.
4. Открываем чашку Петри. И сразу просим взрослого помощника налить на ее дно горячую смесь из кастрюльки. Заранее открывать не надо, чтобы лишние бактерии не мешали нашему опыту.
5. Накрываем крышкой чашку Петри и убираем ее в холодильник примерно на 4 часа. За это время установится желе.
6. Теперь пришло время собирать бактерии и выращивать колонии на агар-агаре в чашке Петри.
Примечание: чашки Петри с застывшим агар-агаром можно хранить в холодильнике в течение 1-2 месяцев перед использованием. Нужно их перевернуть, чтобы конденсат не испортил подготовленную питательную среду.
7. Бактерии собрать не трудно, потому что они есть повсюду. Берем чистую ватную палочку и проводим ею там, где хотим найти бактерии – на грязной посуде или под ногтями на руках, или на земле, или на ручке двери, или на мобильном телефоне, или на клавиатуре. Потом аккуратно проводим этой палочкой по застывшему агар-агару в чашке Петри.
8. Закрываем чашки Петри крышками и заклеиваем скотчем. Чтобы не перепутать чашки, наклеиваем на них наклейки с надписями (откуда были собраны бактерии). Переворачиваем и убираем в инкубатор (теплое темное место). Переворачивать нужно для того, чтобы капли, которые могут образоваться на крышке от испарения, не падали на наш объект исследования. Оставляем на несколько дней.
9. Через несколько дней можно наблюдать под микроскопом, что происходит в чашке Петри. Мы увидим, как начали расти колонии. Раз в день или раз в несколько дней можно проверять, какие происходят изменения.
10. Хотя бактерии, которые мы собрали дома, вероятно, будут безвредными, предосторожность не помешает. Нам снова потребуется помощь взрослого, поскольку пластмассовую чашку Петри нужно хорошенько вымыть хлорным раствором, и только потом утилизировать. Если у Вас стеклянная чашка Петри, то ее можно использовать повторно после стерилизации. Напомните Вашему взрослому помощнику о необходимости надеть резиновые перчатки. Ни в коем случае не работайте с хлоркой самостоятельно!
Если опыт не получился с первого раза, не отчаивайтесь. Попросите совета у учителя биологии в школе. Некоторые виды бактерий любят животную среду, и для них нужно добавить в агар-агар питательную среду, например говяжий бульон. Другие бактерии хорошо размножаются на растительно среде, для них можно добавить картофельный отвар.
Почему это происходит?
Бактерии настолько малы, что их нельзя увидеть невооруженным глазом. Но если их поместить на питательную среду и создать им комфортные условия для размножения, то каждая бактерия вырастает в колонию из тысячи бактерий. И вот колонию уже можно разглядеть в микроскоп. Вырастить бактерии может оказаться не просто. Поэтому не сдавайтесь, если ваши первые попытки потерпят неудачу. Но когда опыт будет удачным, подсчитайте количество колоний и обратите внимание на различия в цвете, форме и размере. Где Вы обнаружили больше бактерий? Попробуйте в середину растущей колонии добавить капельку дезинфицирующего средства для рук или средство для мытья унитаза. Произойдут ли изменения в росте и форме колонии?
Источник
ОСНОВЫ МИКРОБИОЛОГИИ — В. М. Самыгин — 2015
ГЛАВА 10. ОСНОВНЫЕ ПРИНЦИПЫ ВЫРАЩИВАНИЯ БАКТЕРИЙ
Выращивание (культивирование) микроорганизмов необходимо для получения биомассы или различных метаболитов (продуктов обмена веществ) микробной клетки. Выращивание микробов в лабораторных условиях производят на искусственных питательных средах, в культурах тканей и в организме экспериментальных животных. Культуральные признаки микроорганизмов определяют по характеру роста на питательных средах. Эти признаки имеют важное диагностическое значение и являются постоянными для каждого вида микроорганизмов.
На плотных питательных средах при посеве большого количества микробных клеток наблюдается сплошной рост в виде «газонной» культуры микроорганизмов. При посеве ограниченного числа клеток образуются различные по форме и величине колонии, которые представляют собой видимые скопления особей одного вида микроорганизмов, формирующиеся в результате размножения одной клетки. Колонии бывают плоскими, выпуклыми, куполообразными, вдавленными, поверхность их — гладкой (S-формы), шероховатой (R-формы), исчерченной, бугристой, края — ровными, зазубренными, волокнистыми, бахромчатыми. Форма колоний разнообразна: круглая, розеткообразная, звездчатая, древовидная. По величине колонии бывают крупные (4-5 мм в диаметре), средние (2-4 мм), мелкие (1-2 мм) и карликовые (менее 1 мм). Колонии отличаются по консистенции, плотности, цвету. Они бывают прозрачными и непрозрачными, окрашенными и бесцветными, влажными, сухими и слизистыми (рис. 10 и 11).
Рис. 10. Основные типы колоний микроорганизмов
Рис. 11. Морфологическое и структурное разнообразие колоний: 1 — формы выпуклости колоний над поверхностью питательной среды: 2 — очертания колоний: 3 — характер края колоний: 4 — внутренняя структура колоний
В жидких питательных средах микробы растут с образованием диффузной мути, пленки, осадка, видимых невооруженным глазом. Иногда наблюдается пристеночный рост бактерий.
В лабораторных условиях бактерии выращивают в пробирках, чашках Петри, флаконах, бактериологических матрицах. В производственных условиях культивирование микроорганизмов осуществляют в различных ферментерах (ферментаторах, биореакторах) по специально разработанной технологии.
При оценке эффективности роста обычно измеряют биомассу или число микробных клеток. Прямой способ измерения клеточной массы — это определение веса сухого вещества клеток, содержащихся в определенном объеме культуры, путем отделения их от среды, высушивания и последующего взвешивания. Однако с помощью обычных весов трудно точно определить массу менее 1 мг, а такое количество сухого вещества может содержать до 5 млрд бактерий.
Более удобным методом определения массы одноклеточных микроорганизмов является оптический метод — измерение количества света, рассеянного суспензией клеток. Он основан на том, что рассеяние света мелкими частицами в определенных пределах пропорционально их концентрации, и доля пропущенного света служит мерой оптической плотности суспензии. Измерения проводят с помощью спектрофотометра или фотоэлектроколориметра. Эти приборы показывают единицы оптической плотности, которая представляет собой логарифм отношения интенсивности света, падающего на суспензию, к интенсивности пропущенного света. Нижний предел чувствительности данного метода — около 10 млн клеток в 1 мл.
Для определения числа клеток можно использовать микроскопический метод на специальных предметных стеклах — счетных камерах, прямой подсчет клеток с помощью электронного прибора (счетчик Коултера) и др. Однако чаще подсчет общего количества клеток в суспензии проводят с помощью бактериального стандарта мутности, а также высевом микроорганизмов на плотную питательную среду в чашки Петри.
Стандарт мутности представляет собой взвешенные в дистиллированной воде частицы стекла диаметром от 0,5 до 3,5 мкм. Взвесь этого стекла при взбалтывании осадка соответствует определенной концентрации клеток. Стандарт состоит из запаянных пробирок-эталонов, эквивалентных по степени мутности 5 и 10 международным единицам мутности (5 • 10 8 и 10 9 кл/мл соответственно). К комплекту бактериальных эталонов прилагается шрифтовая таблица, содержащая набор различных шрифтов. Исследуемую культуральную взвесь помещают в стандартную пробирку, толщина стенок и цвет стекла которых соответствует пробиркам- эталонам. Разбавляя культуру измеренными количествами физиологического раствора, доводят мутность в исследуемой пробирке до эталонной и производят расчет исходной концентрации микробных клеток. Расчет производят либо по степени разведения культуры, либо на основе общего количества клеток в бактериальной суспензии.
Число одноклеточных микроорганизмов можно подсчитать также после высева на плотную питательную среду в чашки Петри, поскольку жизнеспособные клетки, пространственно отдаленные друг от друга на поверхности плотной среды, в процессе роста образуют отдельные колонии, видимые невооруженным глазом. Следовательно, приготовив соответствующие разведения бактериальной популяции и использовав их для засева среды, можно определить число жизнеспособных клеток в исходной суспензии путем подсчета числа вырастающих после инкубации колоний и умножения этой цифры на коэффициент разведения. Этот метод называют определением концентрации жизнеспособных клеток,так как он позволяет учесть только те микроорганизмы, которые могут расти на питательной среде. Определение числа жизнеспособных клеток, несомненно, является наиболее чувствительным методом количественного учета бактерий, так как он дает возможность зарегистрировать даже единичную жизнеспособную клетку в суспензии. Для установления доли жизнеспособных клеток в популяции можно использовать методы отдельного определения общего числа клеток (с помощью стандарта мутности) и числа жизнеспособных клеток.
Биологическая библиотека — материалы для студентов, учителей, учеников и их родителей.
Наш сайт не претендует на авторство размещенных материалов. Мы только конвертируем в удобный формат материалы, которые находятся в открытом доступе и присланные нашими посетителями.
Если вы являетесь обладателем авторского права на любой размещенный у нас материал и намерены удалить его или получить ссылки на место коммерческого размещения материалов, обратитесь для согласования к администратору сайта.
Разрешается копировать материалы с обязательной гипертекстовой ссылкой на сайт, будьте благодарными мы затратили много усилий чтобы привести информацию в удобный вид.
© 2018-2021 Все права на дизайн сайта принадлежат С.Є.А.
Источник
Как выращивают бактерии для септика
Владельцы загородных жилых домов вынуждены обслуживать автономные канализационные системы самостоятельно. В последние годы хорошим подспорьем в этом им стали специальные микроорганизмы. Однако каким бы ни было ощутимым удобство, необходимость периодически закупать пакетики с бактериями для септиков приводит к ощутимым расходам. Поэтому и сельские жители, и сезонные обитатели дачных посёлков задаются вопросом — можно ли вырастить бактерии в домашних условиях?
Да, можно. Кому-то даже покажется, что выведение колонии микроорганизмов для септика напоминает процесс размножения кефирного грибка. Но это только на первый взгляд. Бактерии для септика требуют более тщательного ухода ввиду особой восприимчивости к внешним условиям. Необходимый атрибут для начала процесса выращивания бактерий для септика – расхожий лабораторный инструмент — чашка Петри. Она свободно продаётся.
Следующее, о чём следует позаботиться – среда. Средой называют раствор органического вещества, который создает благоприятные условия для жизни и размножения бактерий. Различают производственные и диагностические среды. Выращивание бактерий для септиков, как и создание колоний других микроорганизмов, происходит в производственной среде.
Стерильность – одно из важнейших условий работы с бактериями, так как наличие сторонних «собратьев» может помешать процессу выращивания определенной колонии. Чашку Петри перед использованием обдают сухим жаром и охлаждают до 50 градусов. После этого можно приступать к процессу.
Среда, в которой происходит выращивание бактерий для септиков, имеет минеральную основу. Состав минерального раствора может варьироваться в зависимости от разновидности штамма бактерий. Штаммы бактерий для септика – это совокупность организмов, аминокислот и ферментов, которые впадают в анабиоз при отсутствии питательной среды или понижении температуры. При создании колонии микроорганизмов для канализационных систем в чашку Петри, содержащую минеральный раствор, подселяют нужный штамм и наблюдают за процессом, строго соблюдая температурный режим и стерильность в помещении.
Создать нужные условия размножения бактерий в домашней обстановке сложно, но возможно. Шансы на успех особенно высоки у тех, кто получил медицинское, химическое или биологическое образование, и имеет опыт работы в лаборатории.
Источник
Современный подход к культивированию микроорганизмов и культур клеток
Большинство научных исследований в области биологии и медицины проводятся не на живых организмах, а «в пробирке». Клеточные культуры и культуры микроорганизмов являются наиболее простым и удобным модельным объектом, позволяющим как тестировать на них воздействие извне, так и исправлять ошибки внутри клетки. Благодаря исследованиям в области клеточного редактирования постепенно становится возможным лечение многих генетических заболеваний. Но каким образом мы можем добиться культуры, максимально соответствующей требованиям к модели для сложных экспериментов? Рассмотрим наиболее популярные современные способы выращивания микроорганизмов и культур клеток.
Общее понимание культивирования
Культивирование как микроорганизмов, так и отдельных клеток – это выращивание изъятого из определенной среды материала в лабораторных условиях. Выращенная таким образом подборка единообразных микробов или клеток уже может называться культурой.
Для того, чтобы выращивание прошло успешно, требуется наличие определенного оборудования, а также соблюдение условий, необходимых для роста и созревания культуры. Стандартно для культивирования используются:
- Питательная среда, на которой будущая культура должна расти.
- Факторы роста – питательные вещества, используемые клетками.
- Посуда, включающая в себя стерильные чашки Петри, инструменты для переноса клеток на среду и др.
- Дополнительное оборудование: термостаты, аппараты для ферментации и другие.
Также в процессе культивирования от лаборатории требуется соблюдение условий роста для каждой конкретной культуры. Ввиду того, что как клетки, так и микробы, требуют для себя условий, приближенных к естественным, в лаборатории должны поддерживаться различные условия роста при наличии разных культур. Основные условия: приемлемая для культур температура, влажность, давление, постоянная подача кислорода (для аэробных бактерий) или исключение доступа к кислороду (для анаэробных). (Рекомендуем статью: «Флуоресцентная микроскопия»)
Факторы роста
Факторами роста называют все питательные вещества, которые требуются бактериям и клеткам для оптимального роста и развития. В случае если сама среда не обладает достаточным количеством нужных элементов, их добавляют извне. При этом количество строго регулируется в зависимости от требований к конечной культуре.
К наиболее часто использующимся в современном лабораторном культивировании факторам роста относятся:
- Аминокислоты. Отдельным микроорганизмам или группам клеток требуются дополнительные аминокислоты извне. При этом требоваться может только одна кислота, например, лейцин и аргинин для стрептококков.
- Пуриновые или пиримидиновые основания. Также используются и их производные (аденин, гуанин и др.).
- Витамины. Они требуются для того, чтобы поддерживать работу коферментов, участвующих в метаболизме как клеток, так и бактерий.
В зависимости от типа культивируемых клеток или бактерий, фактор роста может как входить в состав питательной среды, так и вноситься извне.
Питательные среды и требования к ним
Питательная среда – это пространство, в котором находится необходимая группа клеток или бактерий. Среды бывают очень разными, в том числе и узкоспециализированными, для роста наиболее привередливых микроорганизмов. Однако существуют и общие требования, предъявляемые ко всем средам без исключения:
- Питательность. Среда должна содержать все необходимые вещества, которые используются бактериями для роста и не могут быть синтезированы ими без среды.
- Нужный уровень pH. Это требуется для регулирования проницаемости мембраны клетки и, как следствие, уровень питательных веществ, попадающих внутрь.
- Уровень осмотического давления, равный уровню давления в культивируемой клетке.
- Оптимальный для конкретной бактерии уровень влажности.
- Окислительно-восстановительные качества. Наибольшие различия требований по данной характеристике существуют при культивировании аэробов и анаэробов.
- Единый состав среды. Каждая конкретная среда должна иметь одинаковое количество веществ, чтобы не было вариативности в результатах культивирования.
При этом питательные среды могут значительно различаться по всем остальным характеристикам. Они могут быть как натуральными, так и синтезированными искусственно, а также жидкими, полужидкими или плотными.
Условия роста
Рост микроорганизмов и клеток невозможен без соблюдения определенных условий, таких как температура, влажность, давление, свет и аэрация (насыщение кислородом). Существуют микроорганизмы, которые имеют диаметрально противоположные требования по условиям роста. Для решения проблемы условий при культивировании различных клеток или микроорганизмов используется специальная аппаратура с камерами, внутри которых поддерживается нужный уровень температуры, света или давления. В одном таком устройстве, но в разных камерах, может быть одновременно несколько чашек Петри с материалом, имеющим различные требования по условиям роста. (Рекомендуем статью: «Инновационные технологии для поиска и разработки новых лекарств»)
Стерилизация посуды, сред и окружения
Одним из наиболее важных требований к процессу культивирования, является отсутствие загрязнений на оборудовании, при помощи которого происходит выращивание. Этого добиваются, проводя мероприятия по стерилизации. Стерилизация может проводиться несколькими способами, наиболее известные и используемые в современных лабораториях:
- Прокаливание. Экспресс-метод устранения микробиологического загрязнения через нагрев, может выполняться на спиртовке. Однако данный метод не может быть использован с чем-то, кроме игл и петель для переноса материала.
- Кипячение. Данный метод широко используется для устранения микробов, но споры бактерий он не устраняет.
- Сухожаровая стерилизация. Проводится в сушильном шкафу, наиболее часто используется для лабораторной посуды.
- Автоклавирование под давлением. Один из самых популярных и универсальных методов, однако многие материалы и среды разрушаются при использовании автоклавов.
Основным моментом в современном культивировании клеток и микроорганизмов, всегда будет являться неуниверсальность методик. Из-за большого разнообразия объектов культивирования, всегда будет необходимость подбирать наилучшие условия для конкретного объекта.
Источник