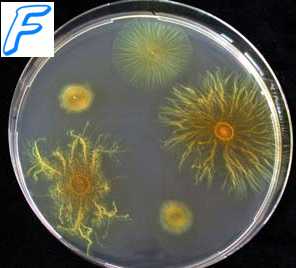
Какие питательные среды используются для выращивания бордетелл
Возбудители этих заболеваний относятся к роду Bordetella.
1. Bordetella pertussis — возбудитель коклюша, описан Борде и Жангу в 1906 г.
2. Bordetella parapertussis — возбудитель паракоклюша, описан Элдеринг и Кондрик в 1937 г.
3. Bordetella bronchiseptica — вызывает заболевание у животных. У человека эти бактерии вызывают бронхопневмонию с коклюшеподобным кашлем. Впервые у человека это заболевание описано Брауном в 1926 г. (встречается редко).
Морфология. Бактерии коклюша — мелкие палочки овоидной формы, 0,3-0,5 × 1-1,5 мкм. Возбудитель пара-коклюша несколько большей величины. Оба микроба не имеют спор, неподвижны. При специальной окраске видна капсула. Грамотрицательны. Более интенсивно окрашиваются по полюсам.
На ультрасрезах видны капсулоподобная оболочка, зерна валютина, в нуклеиде — вакуоли.
Культивирование. Возбудители коклюша и паракоклюша — аэробы. Прихотливы к питательным средам. Для их выращивания применяют среду Борде — Жангу (глицериново-картофельный агар с кровью). В настоящее время пользуются средой КУА (казеиново-угольный агар) — это полусинтетическая среда без крови. Источником аминокислот здесь является гидролизат казеина. Среда КУА отличается от среды Борде — Жангу более простым и доступным методом изготовления.
Для угнетения роста посторонней флоры к среде добавляют пенициллин по 0,25 — 0,5 ME на 1 мл среды или метициллин — 2,5-4 мкг на 1 мл. Пенициллин можно наносить на поверхность среды в чашках.
Засеянные среды инкубируют в термостате при температуре 35-36° С, рН среды 6,8-7,4. Посевы необходимо предохранять от высыхания, для этого в термостат ставят сосуд с водой.
Колонии В. pertussis появляются через 48-72 ч, а В. parapertussis — через 24-48 ч.
На среде КУА колонии В. pertussis мелкие 1-2 мм в диаметре, В. parapertussis несколько крупнее. Колонии обоих микробов блестящие, серовато-кремового цвета (на казеиново-угольном агаре они напоминают капельки ртути). При снятии колоний остается вязкий, сметанообразный след. При изучении колоний в стереоскопическом микроскопе виден световой конус (колонии отбрасывают тень). Когда меняется положение светового источника (электролампочки) тень меняет положением Наличие светового конуса (хвостика) имеет диагностическое значение.
В. parapertussis образует фермент тирозиназу, поэтому в средах, содержащих тирозин, происходит его расщепление и среда окрашивается в коричневый цвет. Изменение цвета среды является дифференциально-диагностическим признаком.
В жидкой среде бактерии коклюша и паракоклюша образуют равномерную муть и придонный осадок. На агаре с кровью они дают зону гемолиза.
Свежевыделенные культуры чаще всего имеют гладкую S-форму (I фаза). При культивировании в неблагоприятных условиях или в материале, взятом в поздние сроки заболевания, могут появиться диссоциированные формы (II-IV фазы).
Ферментативные свойства. Возбудители коклюша не расщепляют углеводы и не ферментируют белки. Бактерии паракоклюша образуют ферменты уреазу и тирозиназу.
Бактерии коклюша и паракоклюша продуцируют ферменты патогенности: гиалуронидазу, плазмокоагулазу и лецитиназу.
Токсинообразование. В опытах на животных у коклюшной палочки были выявлены четыре типа токсина белковой природы: 1) термолабильный дермонекротический токсин; 2) термостабильный эндотоксин; 3) лейкоцитозостимулирующий фактор (стимулирующий лейкоцитоз); парентеральное введение его вызывало гибель экспериментальных животных; 4) гистаминсенсибилизирующий фактор — при введении его мышам у них повышалась чувствительность к гистамину.
Первые два типа токсина свойственны и возбудителю паракоклюша.
Таблица 47. Дифференциальные признаки бактерий рода Bordetella
Антигенная структура. У бактерий рода Bordetella сложная антиренная структура. Наиболее важными антигенами для лабораторной диагностики являются агглютиногены. Родовым агглютиногеном является 7. Видоспецифическим агглютиногеном для бордетелл коклюша является 1, для бордетелл паракоклюша — 14, для бордетелл бронхосептика — 12.
Моноспецифические сыворотки 1, 14, 12 используются для дифференциации видов (сыворотки выпускает Институт эпидемиологии и микробиологии им. Н. Ф. Гамалеи).
Кроме видоспецифических антигенов, у представителей Bordetella имеются и другие агглютиногены, разное сочетание которых определяет серовар (табл. 48.).
Таблица 48. Схема состава агглютиногенного рода бордетелл
По сочетанию трех главных агглютиногенов 1,2,3, определяемых в реакции агглютинации с моноспецифическими сыворотками, В. pertussis различают три серовара: 1,2,3; 1,2,0; 1,0,3.
Устойчивость к факторам окружающей среды. Возбудители коклюша и паракоклюша мало устойчивы. При температуре 56° С они погибают через 20-30 мин. Низкие температуры также губительно на них действуют. Прямой солнечный свет убивает их через 1-2 ч; УФ-лучи — через несколько минут. В сухой мокроте эти бактерии сохраняются в течение нескольких часов. Обычные растворы дезинфицирующих веществ губят их быстро.
Оба вида микробов мало чувствительны к антибиотикам, не чувствительны к пенициллину.
Восприимчивость животных. В естественных условиях животные не восприимчивы к возбудителям этого рода. В экспериментальных условиях удается воспроизвести коклюш у обезьян и молодых собак, вызвать гибель мышей.
Источники инфекции. Больной человек. Особенно заразны больные в катаральном периоде.
Пути передачи. Воздушно-капельный путь. Роль различных предметов мало вероятна ввиду неустойчивости коклюшных бактерий во внешней среде.
Патогенез. Возбудители коклюша и паракоклюша вызывают острое заболевание, сопровождающееся конвульсивным кашлем. Попав на слизистую оболочку верхних дыхательных путей, бактерии размножаются там и частично разрушаются. Выделившийся токсин действует на центральную нервную систему, раздражает нервные рецепторы слизистой оболочки верхних дыхательных путей, что приводит в действие кашлевой рефлекс. В результате возникают приступы судорожного кашля. В процессе заболевания наблюдается несколько периодов: катаральный, спазматического кашля и разрешения процесса.
Иммунитет. После перенесенного заболевания вырабатывается стойкий иммунитет, который обусловливается гуморальными и клеточными факторами.
Профилактика. Выявление и изоляция больных. Ослабленным детям, находившимся в контакте с больным коклюшем, вводят иммуноглобулин. Основные меры специфической профилактики — иммунизация детей АКДС (коклюшно-дифтерийно-столбнячной вакциной). Вакцину вводят троекратно в возрасте до 6 мес с последующей ревакцинацией.
Лечение. В ранних стадиях заболевания применяют противококлюшный иммуноглобулин. Для лечения используют эритромицин и ампициллин.
Контрольные вопросы
1. Опишите морфологические свойства возбудителя коклюша и паракоклюша.
2. На каких средах и каков характер роста коклюшных и паракоклюшных микробов?
3. Устойчивость возбудителей коклюша и паракоклюша во внешней среде.
4. Дифференциальные признаки возбудителей коклюша и паракоклюша.
5. Источники заражения, пути передачи, патогенез коклюша.
Микробиологическое исследование
Цель исследования: выявление возбудителя и дифференциация возбудителей коклюша от паракоклюша.
Отделяемое слизистой оболочки носоглотки.
Способы сбора материала
Источник
Выделение и идентификация бордетелл



Микроскопическая исследование исходного материала
Бактериологическое исследование
Объектом исследования обычно являются взятые стерильным ватным тампоном образцы носовой, трахеальной слизи, участки пораженных
Из поступившего материала готовят мазки, окрашивают по Граму. Бордетеллы, независимо от видовой принадлежности, выглядят как мелкие грамотрицательные коккобактерии шириной 0,2-0,5 мкм, длиной 0,5-2,0 мкм; окрашиваются биполярно, располагаются одиночно, парно, редко — короткими цепочками. Вирулентные штаммы В. bronchiseptica имеют микрокапсулу. Фирма Health Gene выпускает набор для детекции возбудителя в ПЦР.
Культивирование. Бордетеллы — строгие аэробы, температурный оптимум 37-38° С, рН питательных сред 7,2-7,6. Посев исследуемого материала проводят на кровяной, сывороточной агар, агар Мак-Конки. Поскольку объектом исследования чаще всего является контаминированный посторонней микрофлорой материал (носовая, трахеальная слизь), то предпочтительнее посев производить на элективные среды. При этом необходимо учитывать, что при наличие в материале бактерий, расщепляющих углеводы, может тормозить рост бордетелл, так как бордетеллы требуют слабощелочных или нейтральных значений среды, а контаминанты закисляют ее. Из числа элективных сред для изоляции В. bronchiseptica используют кровяной агар с клиндами-цином и неомицином, пенициллиннитрофурантоиновый агар, среду Мак-Конки, среду Smith и Baskerville с гентамицином, пенициллином, фуранта-доном (SB-среда). B.avium на SB-среде культивируют без внесения антибиотиков. Посевы инкубируют в условиях обычной атмосферы в течение 24-48 часов.
B.bronchiseptica на кровяном (овца, лошадь) агаре формирует через 24 часа очень мелкие, выпуклые, с гладкой поверхностью и ровными краями колонии, обычно с зоной β-гемолиза. В наибольшей степени гемолитическая активность выражена на среде Борде-Жангу (рН 6,2-6,8). Колонии B.avium аналогичного типа, но обычно негемолитичные. На МПА свеже-выделенные культуры образуют гладкие, полупрозрачные, с блестящей поверхностью колонии диаметром 0,2-1,5 мм, которые позднее (48-72 часа) становятся серо-белыми. В зависимости от культуральных вариаций могут быть выявлены колонии трех типов: S-форма — 1-й тип, SR-форма — 2-й тип, R-форма — 3-й тип. На агаре Гартоха колонии имеют беловатый цвет, на агаре Мак-Конки колонии мелкие, с розоватой периферией и светлым центром. На селективной среде Smith-Baskerville (SB-среда) колонии
B.bronchiseptica и В. avium через сутки инкубирования имеют размер около 0,5 мм, голубой цвет и с голубым окрашиванием среды вокруг колонии, что свидетельствует о защелочении рН в зоне роста, позднее колонии достигают размера 1,5-2,0 мм. Сходные по культуральным признакам сахаролитические бактерии вызывают закисление рН, поэтому колонии и окружающая среда приобретают желтоватый цвет. В жидких питательных средах (сывороточный МПБ) бордетеллы растут с равномерным помутнением среды, в последующем образуется осадок и пристеночное кольцо, среда становится прозрачной.
Морфология клеток бордетелл в культуре. Морфология клеток в окрашенных препаратах из культур и патологического материала сходна. Капсул не образуют. B.bronchiseptica и B.avium, в отличие от В.parapertussis и B.pertussis, имеют жгутики, поэтому обязательно исследуют выделенную культуру на подвижность.
Идентификация бордетелл на уровне рода. Бактерии рода Bordetella по морфологическим и тинкториальным свойствами сходны с бруцеллами, гемофильными бактериями и видами рода Alcaligenes. Для дифференциации от этих бактерий исследуют способность к росту в анаэробных условиях (гемофилы являются факультативными анаэробами); ферментацию углеводов (бордетеллы не закисляют среды с углеводами); потребность в никотинамиде (бордетеллы зависят от этого ростового фактора); редукцию нитратов (бордетеллы и гемофилы всегда редуцируют нитраты); окисление аминокислот (бордетеллы, в отличие от гемофильных бактерий, окисляют аминокислоты); редукцию тетразолия (бордетеллы, в отличие от видов рода Alcaligenes, редуцируют этот субстрат); утилизацию цитратов (В.hronchiseptica использует цитраты); защелочение лакмусового молока (защелачивают бордетеллы и алкалигенес); способность к росту в питательных средах, содержащих 320 мг/л теллурита калия (бордетеллы не растут). Данные дифференцирующие признаки представлены в таблице 77.
Источник