Рекомендовано Ученым советом ПГУ им С Торайгырова Рецензенты – доктор сельскохозяйственных наук профессор заведующий кафедры Генетики и биотехнологии ПГУ
Задание 1 Определение актуальной и обменной кислотности почвы
Материалы и оборудование : образцы почв, весы с разновесами, прибор Н.И. Алямовского, 1 н. раствор KCl (74,56 г соли растворяют в 400-500 мл дистиллированной воды и доводят объем до 1 л). Раствор должен иметь рН 5,6-6,0. В противном случае добавляют по каплям 10-процентный раствор HCl или КОН до получения заданной величины рН.
Пояснения к заданию . Определение кислотности почвы чаще всего проводят потенциометрическим и колориметрическим, или цветным, методом по шкале Н.И. Алямовского. Колориметрический метод основан на свойствах некоторых веществ, называемых индикаторами, менять окраску при изменении реакции среды.
1) из смешанного образца отвесить 20 г почвы и насыпать в коническую колбу вместимостью 100 мл;
2) прилить к почве 50мл 1 н. раствора KCl (если определяют обменную кислотность) или 50 мл дистиллированной воды (если определяют актуальную кислотность);
3) закрыть колбу чистой пробкой и хорошо взболтать в течение 5 мин;
4) дать жидкости хорошо отстояться до полного осветления в течение 18-24 ч;
5) перенести пипеткой 5 мл прозрачной почвенной вытяжки в чистую пробирку и добавить туда 5-6 капель (0,3 мл) комбинированного индикатора;
6) содержимое пробирки хорошо взболтать;
7) цвет вытяжки сравнить с окраской стандартной шкалы растворов-эталонов и записать величину рН.
Задание 2 Определение дозы извести в зависимости от кислотности почвы
Главная цель известкования состоит в устранении избыточной кислотности и улучшении других свойств почвы.
При внесении извести в почву она нейтрализует угольную кислоту и азотную кислоту, органические кислоты в почвенном растворе, а также ионы водорода в почвенном поглощающем комплексе. Таким образом, известь устраняет актуальную и обменную кислотности и значительно снижает гидролитическую кислотность.
При известковании почва насыщается кальцием, а образующаяся углекислота распадается на СО 2 и Н 2 О. Схематично эту реакцию можно представить следующим образом
[почва] Са + Н 2 О+СО 2
[почва] 2Са + 2Н 2 О
Целесообразность известкования устанавливают по показателям обменной кислотности с учетом степени насыщенности почв основаниями и механического состава (таблица 1.9.2).
Таблица 1.9.2 — Установление необходимости известкования почв по рН и степени насыщенности основаниями (по М.Ф. Корнилову)
Необходимость известкования почв
Тяжело и среднесуглинистая………………..
Супесчаная и песчаная
Приблизительно необходимость в известковании можно определить только по обменной кислотности или только по степени насыщенности почв основаниями.
Об этом можно судить и по данным изучения дикой и культурной растительности поля. Если на участке растут щавелек, едкий лютик, хвощ, осока, мох, то почву следует известковать; на это же указывает сильная изреженность клевера, люцерны, заболевание капусты килой, ржавая окраска воды (в кислой почве растворяются соли железа) и т.д.
Дозу извести устанавливают по величине гидролитической кислотности, умножая ее на 1,5. Например, при гидролитической кислотности, равной 2 мг-экв, доза извести равна (2,0 · 1,5) =3 т/га.
При отсутствии данных по гидролитической кислотности дозу извести можно ориентировочно определить по обменной кислотности (таблица 1.9.3).
Таблица 1.9.3 — Примерные дозы извести, установленные в зависимости от обменной кислотности почвы
Доза (т/га) при рН солевой вытяжки
Супесчаные и легкосуглинистые
Средне и тяжелосуглинистые
Результаты записать по следующей форме
номер почвенного образца
Обменная кислотность (рН солевой вытяжки)
Примерная доза извести, т/га
1.10 Химический состав почвы
В процессе разложения растительных и животных остатков, т.е. одновременно с минерализацией органических веществ, в почве идет процесс образования сложных органических соединений, процесс гумификации (образование почвенного гумуса, или перегноя). Перегнойные вещества почвы имеют сложное химическое строение, более сложное, чем исходный материал. Почвенный перегной содержит гуминовые и ульминовые кислоты, фульвокислоты, аминокислоты, почвенные гумины, воскосмолы, витамины, фенолы, антибиотики и т.п. При разложении гумуса высвобождается углерод, нитраты, фосфаты и т.д. В состав гумуса входит около 5% азота. Поэтому перегнойные вещества служат источником обогащения почвы элементами зольной и азотной пищи. Кроме того, перегнойные вещества – важнейший фактор образования почвенной структуры, они улучшают также аэрацию, тепловые свойства почвы, поглотительную ее способность, влагоемкость и другие физические и химические свойства, определяющие плодородие почвы.
В различных почвах состав и количество образующегося гумуса неодинаково. Большое его количество содержат черноземы. К югу от этой зоны и к северу количество перегноя постепенно убывает. Например, черноземы содержат 8-12, а иногда и 15% гумуса от общей массы почвы, серые лесные почвы – 3-5%, сероземы – 1-3%, а песчаные – всего лишь 0,5-1% (даже сотые доли процента).
Задание 1 Определение количества гумуса по методу И.В. Тюрина
Материалы и оборудование : образцы почвы, сита с диаметром отверстия 1,0 и 0,25 мм, пинцеты, лупы, стеклянные палочки, фарфоровые ступки, резиновые пестики, конические колбы вместимостью 100 мл, химические стаканы или колбы вместимостью 500 и 1000 мл, бюретки, небольшие стеклянные воронки (холодильник), электроплитка или газовая горелка, технические и аналитические весы.
1) 0,4 н. раствор хромовой кислоты (смеси). 40 г хорошо измельченного кристаллического двухромовокислого калия (K 2 Cr 2 O 7 ) или 32 г хромового ангидрида (Cr 2 O 3 ) растворяют примерно в 600-800 мл дистиллированной воды и фильтруют через бумажный фильтр в мерную колбу вместимостью 1 л. Раствор доводят дистиллированной водой до метки, выливают в большую фарфоровую чашку или в колбу вместимостью 3-5 л из термостойкого стекла и к нему очень осторожно приливают (под тягой) небольшими порциями (по 50-100 мл) 1 л концентрированной серной кислоты (плотностью 1,84). После каждого прибавления Н 2 SO 4 раствор осторожно перемешивают, дают немного охладиться и только после этого добавляют следующую порцию кислоты. Когда вся кислота добавлена, раствор закрывают стеклом, оставляют стоять для полного охлаждения до следующего дня, затем переносят в склянку с притертой пробкой и хранят в темном месте;
2) 0,2 н. раствор соли Мора (NH 4 ) 2 SO 4 · FeSO 4 · 6H 2 O. 80г соли мора растворяют в 600-700 мл дистиллированной воды, к которой прибавлено 20 мл концентрированной серной кислоты (плотностью 1,84). Раствор фильтруют через складчатый фильтр, доводят водой в колбе вместимостью 1 л до метки и хорошо перемешивают. Раствор хранят в закрытой бутыли (кислород воздуха окисляет соль Мора);
3) раствор дифениламина C 12 H 11 N. 0,5 г дифениламина помещают в химический стакан и приливают при постоянном помешивании стеклянной палочкой 100 мл серной кислоты плотностью 1,84. После этого осторожно добавляют 20 мл дистиллированной воды, в результате чего происходит разогревании раствора, что способствует растворению индикатора;
4) концентрированная серная кислота;
5) 85-процентный раствор ортофосфорной кислоты H 3 PO 4 (плотностью 1,7).
Пояснения к заданию . Общее количество гумуса в почве определяют косвенным путем по количеству углерода в почве (прямых методов определения общего количества гумуса в почве нет). Сущность этого метода заключается в окислении углерода органического вещества (гумуса) 0,4 н. раствором двухромокислого калия (K 2 Cr 2 O 7 ), приготовленного на разведенной в воде (1:1) серной кислоты. Количество окислителя, израсходованного на окисление углерода перегноя, определяют по разности между количеством хромовой смеси, взятой на окисление, и количеством ее, оставшимся неизрасходованным (устанавливают титрованием остатка хромовой смеси солью Мора). По количеству израсходованного окислителя вычисляют процентное содержание гумуса.
Установлено, что среднее содержание углерода в перегное 58%. Поэтому при пересчете углерода на гумус процентное содержание углерода умножают на коэффициент 1,724. Обратный пересчет гумуса на углерод проводят по формуле
% С = % гумуса ·0,58. (25)
1) из смешанного образца почвы взять 5-10 г;
2) взятую пробу поместить на стекло с подложенной под него белой бумагой (для фона) и тщательно отобрать корешки (под лупой), раздавливая комочки почвы пинцетом. Если мелких корешков много, то при отборе их можно пользоваться наэлектризованной (натертой шерстяной или суконной тканью) эбонитовой или стеклянной палочкой (мелкие корешки притягиваются палочкой, если быстро пронести ее над распределенной тонким слоем почвой). Слишком близко к почве палочку подносить нельзя, так как к ней прилипают и минеральные частицы почвы;
3) почву, отделенную от корешков, просеять через сито с отверстиями 0,25 мм. Если на сите останется минеральный остаток, растереть его в ступке, просеять и присоединить к просеянной раньше почве. Почву тщательно перемешать;
4) отвесить на аналитических весах 0,05-0,5 г почвы (чем больше гумуса содержит данная почва, тем меньше должна быть навеска. Одновременно берут навеску почвы около 5 г для определения коэффициента гигроскопичности) и поместить ее в коническую колбу вместимостью 100 мл;
5) прилить из бюретки точно 10 мл 0,4 н. раствора K 2 Cr 2 O 7 , приготовленного в разбавленной серной кислоте (приливать медленно, чтобы раствор полностью стекал со стенок бюретки);
6) содержимое колбы осторожно взбалтывать круговым движением. При этом следить за тем, чтобы частицы почвы не оставались на стенках колбы;
7) в горло колбы вставить маленькую воронку, служащую холодильником, и поставить на этернитовую плитку, песочную баню или газовую горелку с асбестовой сеткой;
8) содержимое колбы кипятить 5 мин. Отсчет времени начать с момента появления первого относительно крупного пузырька газа (СО 2 ). Нельзя допускать сильного кипения и выделения пара из воронки (пузырьки газа должны быть хотя и обильными, но по величине не больше зерна проса). При нагревании идет окисление углерода перегноя до СО 2 на которое затрачивается некоторая часть двухромовокислого калия по схеме:
2K 2 Cr 2 O 7 +8H 2 SO 4 + 3C (гумуса) = 2K 2 SO 4 + 2Cr 2 (SO 4 ) 3 + 8H 2 O + 3CO 2
При сильном кипении часть хромовой кислоты разрушается, что отрицательно сказывается на точности анализа. Если хромовая кислота будет израсходована полностью, о чем можно судить по зеленой окраске раствора, то определение следует повторить, уменьшив навеску почвы или увеличив количество бихромата;
9) по окончании кипячения колбу снять с плитки, охладить до комнатной температуры и перенести ее содержимое дистиллированной водой в колбу вместимостью 500 мл.(Сначала вынимают и обмывают дистиллированной водой воронку, а затем несколько раз ополаскивают водой маленькую колбу, выливая ее содержимое в большею колбу). Объем жидкости в колбе довести до 250 мл (приблизительно), прибавить 2 л 85-процентного раствора фосфорной кислоты и восемь капель дифениламина в качестве индикатора 1 . Оттитровать содержимое колбы 0,2 н.раствором соли Мора до перехода темно-бурой окраски раствора через фиолетовую и синюю в грязно-зеленоватую. При появлении синего цвета титровать следует очень осторожно, прибавляя раствор соли мора по одной капле и все время перемешивать энергичным взбалтыванием;
10) записать объем (мл) раствора соли Мора, пошедший на титрование содержимого колбы;
11) произвести холостое определение (установить соотношение между K 2 Cr 2 O 7 и солью Мора), т.е. определить, сколько соли Мора идет на титрование 10 мл раствора хромовокислого калия в серной кислоте. Для этого взять примерно 0,2 г прокаленного песка (для равномерного кипения), поместить в коническую колбочку вместимостью 100 мл, прилить из бюретки 10 мл 0,4 н. раствора K 2 Cr 2 O 7 , закрыть маленькой воронкой и кипятить на плите точно 5 мин, охладить, добавить индикатор и оттитровать;
12) найти количество соли Мора, которое соответствует хромовой кислоте, израсходованной на окисление гумуса (по разности между количеством раствора Мора, пошедшим на титрование при холостом опыте, и количеством соли Мора, пошедшим на титрование остатка бихромата после окисления углерода перегноя);
13) вычислить процентное содержание гумуса по формуле
(а- b ) · 0,0010362 · N ·100 · K
где а – объем раствора соли Мора, затраченный на холостое титрование 10 мл хромовой смеси (пункт 11), мл;
b – объем раствора соли Мора, затраченный на титрование содержимого колбы после окисления гумуса (пункт 10), мм;
N – поправка к титру соли Мора;
K – коэффициент гигроскопичности почвы (пересчет на сухую почву);
с – навеска воздушно-сухой почвы, взятая для анализа, г;
100 – коэффициент пересчета на 100 г почвы;
1 В.Н. Симаков в качестве индикатора вместо дифениламина рекомендует прибавлять 5-8 капель 0,2 процентного раствора фенилантраниловой кислоты.
0,0010362 – коэффициент для пересчета на перегной (показывает, что 1 мл 0,2 н. раствора соли Мора соответствует такому количеству хромовой кислоты, которое окисляет 0,0010362 г гумуса или 0,0006 г углерода).
Например, для определения содержания перегноя взята навеска 0,2123 г воздушно-сухой почвы. Содержание гигроскопической воды в почве – 5,01%.
При установке соотношения между 10 мл K 2 Cr 2 O 7 и солью Мора (холостой опыт) израсходовано 21,9 мл 0,2042 н. раствора соли Мора, на титрование избытка хромовой кислоты после окисления затрачено 12,8 мл того же раствора. Поправка на нормальность раствора соли Мори равна 0,2042 : 0,2 + 1,021. Следовательно, на окисление гумуса израсходовано такое количество хромовой кислоты, которое соответствует 21,9 – 12,8 = 9,1 мл раствора соли Мора.
Количество гумуса в пересчете на сухую почву будет равно:
(21,9 – 12,8) · 0,0010362 · 1,021 ·100 · 1,05 : 0,2123 = 5,34%;
14) вычислить процентное содержание азота в почве.
% N = % гумуса · 0,05. В нашем примере % N = 5,34 · 0,05= 0,267%;
15) вычислить процентное содержание углерода перегноя.
% С = % гумуса · 0,58. В нашем примере % С = 5,34 · 0,58 = 3,097%;
16) вычислить запасы гумуса в верхнем 20-сантиметровом слое почвы, если содержание гумуса в нем 5,34% от массы сухой почвы, а объемная масса – 1,4 г/см 3 . Вычисляем, что запасы гумуса равны
20 · 1,4 · 5,34 = 149,5 т/га.
Задание 2 Определение подвижного калия в карбонатных почвах по методу П.В. Протасова
Материалы и оборудование: пламенный фотометр, технохимические весы с разновесами, образцы почвы, просеянной через сито с ячейками 1 мм, колбы вместимостью 250 мл.
Таблица 1.10.1 — Обеспеченность почв обменным калием (в мг К 2 О на 100 г почвы)
Источник
9 способов определения кислотности почвы на участке

Содержание статьи:
Почвенная реакция сильно варьирует от грядки к грядке, кроме того, на неё влияют смена сезонов, уборка урожая и так далее. Поэтому измерения лучше проводить с помощью проб с разных мест на огороде и дважды — в начале сезона и по его завершении.
Ниже представлена таблица различных культур, которые распределены по группам согласно требованиям к кислотности грунта.
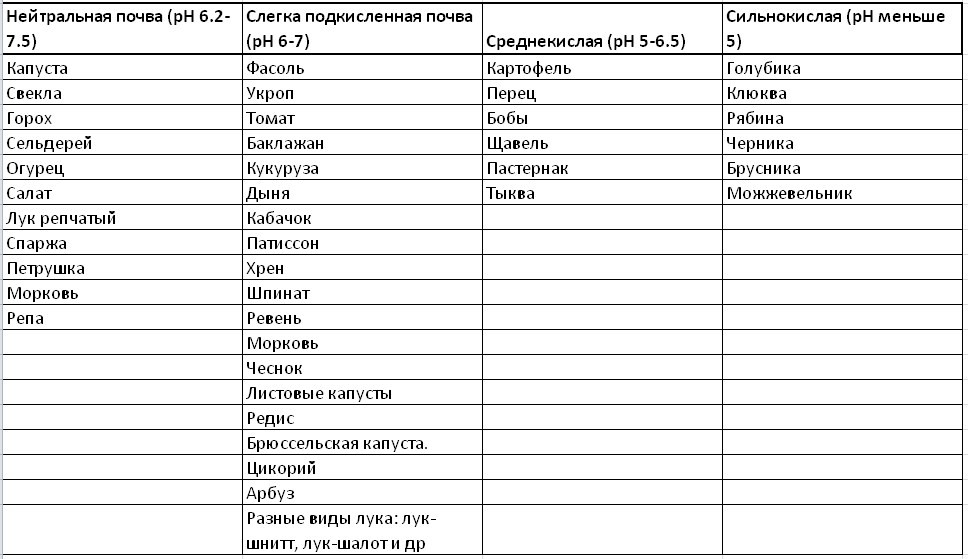
Далее я хотела бы перейти непосредственно к методам проверки кислотности почвы в домашних условиях.
Способ № 1. Лакмусовая бумажка
Этот простой анализатор кислотности продаётся в садоводческих магазинах, аптеках, специализированных магазинах для химиков и через интернет. Он состоит из некоторого количества полосок, обработанных особым реагентом, который изменяет цвет в зависимости от реакции среды. Все необходимые данные по соответствию полученного цвета и уровня pH есть в наборе.
Порядок ваших действий следующий:
- Возьмите пробы земли с разной глубины и с разных грядок. Если вам хочется посчитать среднее значение кислотности по даче, просто выбираете грунт с разных мест в произвольном порядке. Только учтите, что по законам статистики среднее значения будет достоверным только если количество проб будет не менее 30. Десять проб — это самый минимум, хотя тогда будет серьёзная погрешность.
- Отобранный грунт заверните в трёхслойную марлю и опустите в баночку с чистой дистиллированной водой. Её нужно приобрести отдельно в аптеке.
- Тщательно взболтайте баночку с жидкостью и затем опускаете лакмусовую бумажку в воду на пару секунд, пока она не изменит цвет.
- Определяете кислотность по вкладышу в наборе и повторяете эту процедуру для остальных взятых проб.
Способ № 2. Прибор Алямовского
Устройство представляет собой набор реактивов для анализирования водных и солевой вытяжки земли. При его использовании требуются такие же манипуляции, что и описаны в предыдущем методе.
Способ № 3. Измеритель почвы
Сейчас современному огороднику доступна целая линейка многофункциональных приборов. Они позволяют точно определять реакцию почвы, её влажность, температуру, освещённость и другие параметры.
Плюс таких гаджетов состоит в том, что они приобретаются раз и на всю жизнь, а жирным минусом является кусачая цена.
Способ № 4. Химическая лаборатория
Пожалуй, это наиболее точный способ, но и самый затратный, ведь анализ почвы нужно провести многократно в разных местах участка.
Способ № 5. Уксус или соляная кислота
Далее я опишу несколько народных способов измерения pH почвы. Они не настолько достоверны, как различные покупные приспособления и тем более лабораторные анализы, но зато дешёвы и быстры в исполнении.
При этом методе нужно горстку земли с огорода слегка полить крепко разведённой соляной кислотой или обычным уксусом. Если смоченная земля начинает «закипать», то есть на её поверхности появятся небольшие пузырьки, значит, показатель pH для этой пробы является нормальным. Если же вы так и не дождались никакой реакции, то почве требуется известкование.
Способ № 6. Листья смородины (вишни, черёмухи)
В ёмкость из стекла поместите листья одного из растений и залейте кипятком (на 1 стакан нужно использовать 4-5 листочков). После остывания воды бросьте в полученный отвар приготовленный образец почвы. Если вода поменяет цвет на красный — почва кислая, на синий — слабокислая, на зелёный — нейтральная.
Способ № 7. Виноградный сок

Способ № 8. Мел
Метод посложнее предыдущих, но считаю нужным упомянуть и его для полноты картины.
Вам понадобятся: две полные столовые ложки огородного грунта, пять столовых ложек воды комнатной температуры, одна чайная ложка мела.
Всё это добро засыпают в бутылку, на горлышко которой надевают напальчник (для шитья), предварительно избавленный от воздуха. Бутылку помещают в бумагу, чтобы нагрев от ваших рук не исказил результаты эксперимента.
Если почва на вашем участке имеет недостаточно извести (то есть она кислая), то в процессе химической реакции в бутылке будет появляться углекислый газ. Он начнёт стремительно заполнять напальчник и тот выпрямится. Если грунт имеет слабокислую реакцию, то напальчник выпрямится только наполовину, при нейтральной — не распрямится вовсе.
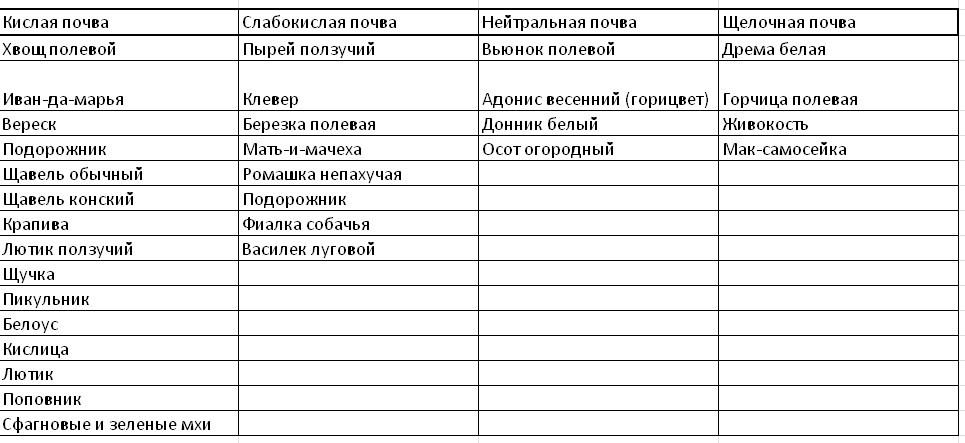
Способ № 9. Сорняки на участке
Наиболее простой индикатор кислотности почва — это сорные растения, облюбовавшие вашу дачу. Единственно, здесь нужно анализировать с умом и смотреть только на самые распространённые сорняки. Ведь завезённые с рассадой или случайные гости не могут служить достоверной основой для надёжных выводов.
В таблице ниже я привела список сорняков, разбитых в группы по характеру предпочитаемых ими почв.
В табличку закралась ошибка — крапива на участке сигнализирует о нейтральной, а не о кислой почве!
Это далеко не исчерпывающий список методов, как определить кислую почву. На своём участке для тестирования кислотности почвы я применяю лакмусовую бумагу Garden Show. Набор включает в себя 80 полосок, которых мне хватает на три года — измерения обычно провожу два раза в год, весной и осень. При этом каждый раз трачу по 10-12 полосок на огород в 5 соток.
Поделитесь, если у вас есть какие-либо свои методы или наработки по этой теме и я обязательно дополню ими эту статью.
О народных методах измерения pH огородной почве подробно и интересно рассказано в видео.
Источник