Основы технологии фосфорных удобрений



К фосфорным удобрениям относятся природные фосфаты и продукты их переработки. В отличие от других видов минеральных удобрений фосфорные удобрения обладают различной растворимостью, по которой они подразделяются на: водорастворимые (группа I); растворимые в органических кислотах или усвояемые (группа II); нерастворимые или растворимые только в сильных минеральных кислотах (группа III). По содержанию питательного элемента фосфорные удобрения делятся на концентрированные (более 30% Р2О5) и неконцентрированные (менее 30% Р2О5).
Методы переработки фосфатного сырья существенно зависят от состава руды и могут быть механическими и химическими.
Механической обработкой (измельчением) получают простейшее фосфорное удобрение — фосфоритную муку.
Задачей химической переработки природных фосфатов в фосфорные удобрения является превращение исходного фосфорсодержащего сырья в такие соединения фосфора, которые легко усваиваются растениями и являются высококонцентрированными, то есть содержат возможно больше Р2О5 в усвояемой форме при минимальном количестве балласта и вредных примесей.
Важнейшими представителями фосфорных удобрений являются простой и двойной суперфосфат, которые выпускаются в виде порошка или гранул.
Простой суперфосфат получают камерным методом при разложении природных фосфатов (апатитового концентрата или фосфоритной муки) серной кислотой.
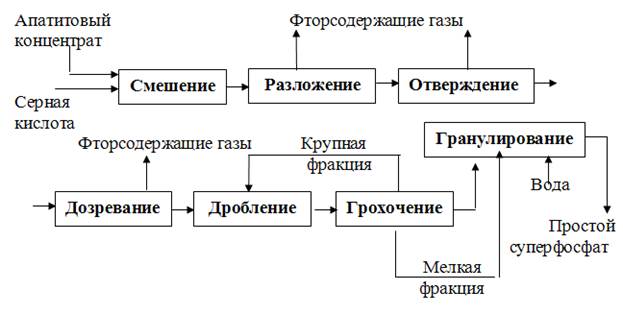
Основными стадиями в производстве простого суперфосфата являются (рис. 4):
— смешение апатитового концентрата или фосфоритной муки с серной кислотой;
— разложение сырья при химическом взаимодействии исходных компонентов с образованием суперфосфата и фосфогипса;
— отверждение получаемой суспензии в суперфосфатной камере;
— дозревание полученного в камере суперфосфата на складе дообработки;
— дробление простого суперфосфата;
-грохочение (отделение крупных и мелких фракций);
— гранулирование простого суперфосфата.
Рис. 4. Принципиальная схема производства простого суперфосфата
Существенным недостатком технологии производства простого суперфосфата является образование побочных продуктов — фосфогипса СаSО4, а также выделение очень вредного газообразного фтористого водорода (НF) на всех стадиях производства, при этом содержание Р2О5 в простом суперфосфате не превышает 20%.
Таблица 4 – Физико-химические свойства простого суперфосфата в соответствии с действующими ГОСТ и ТУ
| № п/п | Показатели | Суперфосфат из апатитового концентрата | Суперфосфат из фосфоритов Каратау | |||
| Гранулиро-ванный (ГОСТ 5956-78) | Порошко- видный, сушеный, нейтрализо-ванный (ТУ 6-08-340-74) | Порошко-видный (ТУ 6-08-277-73) | Гранулиро- ванный, аммонизи- рованный (ГОСТ 17790-78) | Аммонизиро- ванный, сушеный ( ТУ 6-08-327-75) | ||
| 1. | Содержание усвояемой Р2О5, % | 20±1 | 20±1 | 20±1 | 15±1 | 15±1 |
| 2. | Содержание свободной Н3РО4 в пересчёте на Р2О5, % | 1-2,5 | Не более 2,5 | Не более 5,0 | Не более 0,5 | Не более 0,5 |
| 3. | Содержание влаги, %, не более | 4,0 | 5.0 | 12,0 | 3,0 | 3,0 |
| 4. | Механическая прочность гранул на раздавливание, МПа (КГС/см 2 ) не менее | 1,0 (10) | — | — | 1,5(15) | — |
| 5. | Гранулометрический состав. Содержание гранул размером: · (1-4)мм, % не менее · (4-6) мм, %, не более · менее 1 мм, % не более | — — — | — — — | — — — |
Двойной суперфосфат, как более концентрированное удобрение, получают путем разложения природных фосфатов фосфорной кислотой, при этом производство двойного суперфосфата осуществляется двумя методами: камерным (не отличается от схемы получения простого суперфосфата) и поточным (бескамерным).
К недостаткам камерного способа относится наличие длительного складского дозревания продукта, сопровождающегося неорганизованными выделениями вредных фтористых соединений в атмосферу, и необходимость применения концентрированной фосфорной кислоты (50-55% Р2О5).
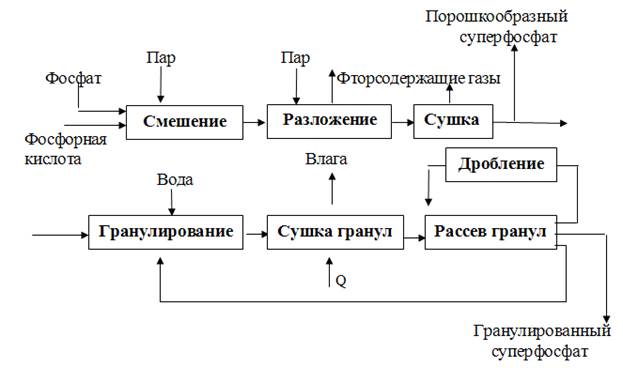
Основными стадиями в производстве двойного суперфосфата поточным методом являются (рис. 5):
— смешение апатитового концентрата или фосфоритной муки с 32% фосфорной кислотой;
— разложение фосфатного сырья (0,5-1 ч при температуре 95 0 С) в реакторе-смесителе с образованием пульпы готового продукта;

— сушка в распылительной сушилке и получение порошкообразного удобрения;
— гранулирование части порошкообразного суперфосфата в грануляторе-смесителе;
— сушка гранул в барабанной сушилке;
— рассев гранул на грохоте и получение товарной фракции двойного суперфосфата (размеры частиц 1-4 мм).
Рис. 5. Принципиальная схема производства двойного суперфосфата
После рассева гранул суперфосфата на грохоте крупная фракция с частицами размером более 4 мм измельчается на молотковой дробилкеи снова поступает на грохот; мелкая, так называемый ретур, (размер частиц менее 1 мм) возвращается в гранулятор-смеситель.
В себестоимости производства суперфосфата наибольшую долю (93. 96 %) составляет стоимость сырья, при этом себестоимость гранулированного двойного суперфосфата выше, чем порошкообразного. Однако гранулирование способствует значительному улучшению качества и агрохимических свойств удобрений. Себестоимость двойного суперфосфата на 10. 13% выше, чем простого, но это превышение компенсируется экономией труда на его транспортировку и внесение в почву.
Таблица 5 – Физико-химические свойства двойного суперфосфата в соответствии с ГОСТ 16306-80
Источник
Фосфорные удобрения
Фосфорные удобрения – удобрения, содержащие в качестве основного питательного элемента фосфор. Различают три группы: водорастворимые, цитратно-лимоннорастворимые, труднорастворимые фосфорные удобрения. Применяются они в основной прием, при припосевном внесении и при подкормках. Основное сырье для производства – природные фосфаты (апатиты и фосфориты различных месторождений). [5]
Содержание:
Классификация фосфорных удобрений
Водорастворимые фосфорные удобрения
К этой группе относятся суперфосфаты. По способу производства и содержанию P2O5 суперфосфаты делятся на простые и двойные (тройные), по консистенции – на гранулированные и порошковидные. [2]
- Суперфосфат простой(СаН2РО4)2 х Н2О + 2СаSО4 х 2Н2О в порошковидной форме содержит 19 % усвояемого фосфора, а гранулированный – не менее 20 %. Кроме того, удобрение содержит 50–55 % СаSО4. Наличие серы благоприятно сказывается на урожайности культур, положительно реагирующих на серу (рапса, капусты, брюквы, турнепса и др.), а также картофеля. [1]
- Суперфосфат двойной Са(Н2РО4)2 х Н2О производится в гранулированном виде, содержит 43 и 49% P2O5, в зависимости от марки. Свободная кислота в составе удобрения не превышает 2,5–5 %. Положительно влияет на рост и развитие всех сельскохозяйственных культур. [1]
- Суперфос – удобрение фосфорное концентрированное. Содержание P2O5 – 38–40 %. Половина соединений фосфора находится в водорастворимой форме. Получают путем химического воздействия на фосфоритную муку смеси серной и фосфорной кислот. Выпускается в гранулированном виде. По агрономической эффективности превосходит суперфосфаты. [2]
Цитратно- и лимоннорастворимые фосфорные удобрения
- Преципитат СаНРО4 х 2Н2О содержит 27–38 % Р2О5. Внешне это порошок светло-серого или белого цвета. Получают путем нейтрализации фосфорной кислоты известковым молоком либо мелом и как отход желатинового производства. Растворим в лимоннокислом аммонии и хорошо усваивается растениями. Применяется для основного внесения. [5] Используется для добавки в корма. [5]
- Термофосфаты Nа2О х 3СаО х Р2О5 + SiО2 содержат 20–30 % фосфора в лимоннорастворимой форме. К этой группе удобрений относят томасшлак, мартеновский шлак, обесфторенный фосфат. Возможно производство из природных фосфатов, не пригодных для внесения в почву и трудно поддающихся химическому воздействию, с целью получения водорастворимых фосфорных удобрений.
Термофосфаты распространены в Западной Европе. В Германии это ренаний–фосфат, содержащий 25–30 % Р2О5. Получают спеканием фосфоритов с содой (20 %) и добавкой доменного шлака. Во Франции фоспаль (27–29 % Р2О5). Это плавленый фосфат. Получается из сенегальского алюмокальций фосфата при прокаливании при относительно невысоких температурах (550–600°C). [1]
Труднорастворимые
- Фосфоритная мука – тяжелый порошок темно-серого цвета. Получают путем размола фосфоритов. Выпускается четыре марки. Содержание Р2О5 – 20, 23, 26 и 29 %. Диаметр частиц – не более 0.18 мм. Это медленно действующее удобрение применяется при основном внесении и фосфоритовании почвы. [1]
- Вивианит (болотная руда) Fe3(РО4)2 х 8 Н2О – мелкий порошок. Удобен для рассеивания. В чистом виде содержит 28 % Р2О5, с примесью торфа (торфовивианит) – 12–26 % Р2О5. Залежи вивианита встречаются в виде небольших гнезд или прослоек массы белесого цвета. На воздухе синеет. После добычи массу проветривают и подсушивают. [1]
Сахар
Суперфосфат используют для получения сахара
Применение
Сельское хозяйство
Фосфорные удобрения применяют для повышения плодородия почвы, в частности, для увеличения содержания фосфора и доступных растениям фосфорных соединений. Кроме того, преципитат, обесфторенный фосфат, костную муку применяют для минеральной подкормки животных. [5]
Промышленность
Суперфосфат используют в дрожжевой и сахарной промышленности (фото). В строительстве он применяется для огнезащитного покрытия древесины.
Двойной суперфосфат используют в химической промышленности в качестве источника фосфора и для приготовления тукосмесей. [3]
Побдробнее о фосфоре читайте в статье Фосфор.
Поведение в почве
Поведение фосфорных удобрений в почве зависит не только от вида удобрения, но и от физико-химических процессов, проходящих в самой почве.
При внесении они растворяются, и фосфат-ион постепенно переходит в различные соединения, присущие данному типу почв. Процесс этот медленный. Частично внесенные фосфатные удобрения (гранулированные, полурастворимые и нерастворимые) длительно сохраняются в почве в неизменном виде.
Виды фосфорных удобрений
Трансформация фосфора удобрений обусловлена следующими процессами:
- Обменным (коллоидно-химическим) поглощением фосфора твердой фазой почвы.
Этот процесс наблюдается на поверхности гидратов полуторных оксидов (положительно заряженных коллоидных частиц) или на положительно заряженных участках отрицательно заряженных коллоидов (минералов каолинитовой и монтмориллонитовой групп, гидрослюд, коллоидов белковых групп). Обменное поглощение сильнее выражается в условиях кислой среды. Реакция среды вызывает изменение электрического потенциала почвенных коллоидов. Подкисление почвенного раствора благотворно влияет на большее поглощение анионов. Подщелачивание приводит к обратному результату. В почвах со слабокислой и нейтральной реакцией обменное поглощение выражено гораздо слабее.
Обменно-поглощенные ионы путем десорбции легко вытесняются в раствор другими анионами минеральных и органических кислот. Данные вещества всегда присутствуют в почвенном растворе, и недостатка в них не испытывает ни один тип почвы. Это и определяет высокую подвижность обменно-поглощенных фосфатов в почвах и, как следствие, их доступность растениям.
По своей доступности обменно-поглощенные фосфаты приравниваются к водорастворимым. [5]
Поглощением фосфора катионами кальция, магния, оксидами и гидроксидами железа, алюминия, марганца и титана по типу химического связывания.
Химическому поглощению в почвах подвергаются и водорастворимые фосфат-ионы удобрений, и фосфат-ионы, перешедшие в раствор из обменно-поглощенного состояния в результате десорбции. Ход и тип химического поглощения обусловливается типом почвы и степенью ее кислотности.
Величина кислотности почвы определяет растворимость солей различных металлов (магния, алюминия, кальция, железа, титана и др.). Взаимодействуя с растворимыми фосфат-ионами, эти соли переводят их в труднорастворимые соединения. Установлено, что наименьшее связывание фосфатов и их максимальная подвижность наблюдаются в интервале pH5,0–5,5. На более кислых почвах фосфат-ионы поглощаются оксидами железа и алюминия, на менее кислых – кальция и магния.
На почвах с нейтральной реакцией среды водорастворимые фосфорные удобрения в результате химического поглощения превращаются в двузамещенные фосфаты кальция и магния (CaHPO4 x 2H2O или MgHPO4 и долгое время остаются именно в таком доступном для растений виде. В дальнейшем ион водорода постепенно замещается кальцием или магнием и образуются трехзамещенные фосфаты этих элементов (Ca3(PO4)2 или Mg3(PO4)2. С течением времени образуются и более основные фосфаты типа октакальцийфосфата (Ca4H(PO4)3 x 3H2O) – это еще менее растворимое соединение. Однако данные соли, находясь в свежеосажденном аморфном состоянии, сохраняют свойство растворяться в слабых кислотах и остаются частично доступными для растений. По мере ретрограции (старения) и перехода из аморфного в кристаллическое состояние фосфаты становятся недоступными для большинства растений.
В дерново-подзолистых почвах с кислой и слабокислой средой основными компонентами химического связывания фосфат-ионов из водорастворимых удобрений являются полуторные оксиды:
Опытным путем установлено, что ранее не использованный («остаточный») фосфор хорошо доступен растениям. В почве фосфаты удобрений не закрепляются намертво в значительных количествах. Более того, при дефиците фосфорных удобрений происходит мобилизация фосфатных ресурсов почвы. При этом происходит постепенная трансформация труднорастворимых фосфатов в более растворимые. [5]
Биологическим поглощением фосфора растениями и микрофлорой почвы.
Биологическое поглощение фосфора растениями возможно только из солей ортофосфорной кислоты. Ортофосфорная кислота является трехосновной и может отдиссоциировать три аниона: H2PO4 — , HPO4 2- и PO4 3- . В условиях слабокислой реакции среды, в которой чаще всего и растут растения, наиболее доступным является первый из перечисленных ионов, второй – в меньшей степени, третий практически не доступен.
Все соли ортофосфорной кислоты и одновалентных катионов (NH4+, Na+, K+), а также однозамещенные соли двухвалентных катионов (Ca(H2PO4)2 и Mg(H2PO4)2) растворимы в воде и легко усваиваются растениями и микрофлорой почвы. [5]
Применение на различных типах почв
Особенности применения фосфорных удобрений для различных почв зависят от растворимости фосфорных соединений:
- Фосфаты, растворимые в воде, применяются на всех почвах, под все культуры и в разные приемы.
- Эффективность применения фосфатов, растворимых в слабых кислотах (цитратно- и лимоннорастворимые фосфорные удобрения), на кислых почвах сильнее.
- Труднорастворимые удобрения эффективны на почвах с кислой реакцией. К ним относятся почвы нечерноземной зоны и северные черноземы (деградированные и выщелоченные). [2]
Источник