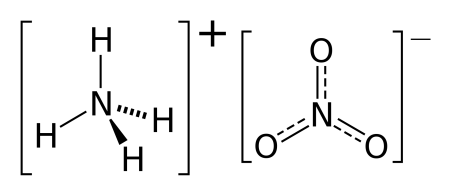Аммиачная селитра — состав и нормы внесения удобрения
Хороший грунт – залог отличного урожая. Со временем земля нуждается в подпитке. Для увеличения ее плодородности применяют удобрения. Магазины предлагают широкий ассортимент удобрений. Не последнее место в этом списке занимает нитрат аммония.
Аммиачная селитра в пакетах 3 и 1 кг
Аммоний азотнокислый применяется как садоводами, так и крупными аграрными хозяйствами. Основные преимущества нитрата аммония:
- немедленное действие на грунт;
- эффективность, даже при замерзшей почве (позволяет вносить удобрение ранней весной);
- избавляется от бактерий и грибков, находящихся в грунте;
- способен повысить иммунитет растений, укрепить их защитные функции;
- предотвращает развитие грибков и бактерий на растениях;
- увеличивает урожайность.
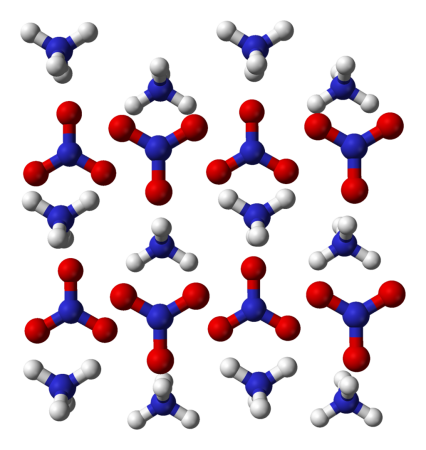
Аммиачная селитра – соединение с химической формулой NH4NO3, имеет гранулированную структуру. Размер частиц не превышает 4 мм, они белого цвета с желтым, розовым или серым оттенком.
Азот – основной действующий элемент для развития растений. Входит в состав нуклеиновых кислот, которые, в свою очередь, являются составляющими практически всех важных клеток растения (отвечающих за дупликацию материала, дыхания, синтез белка). Количество его в составе удобрения варьируется от 25 до 36%. Помимо азота, в составе содержится сера (улучшает усвоение азота), ее концентрация может колебаться от 4 до 15%.
Нитрат аммония может иметь искусственное и природное происхождение. В первом случае – извлечение происходит химическим способом. При природном – извлечение осуществляется путем нейтрализации азотной кислоты. Производители выпускают удобрения с применением различных элементов в качестве добавок. Это осуществляется с целью подстроить продукт под различные типы, качества грунта.
В связи с этим можно выделить несколько основных видов нитрата аммония:
- Аммиачная селитра простая – является базовой для большинства удобрений. Применяется для восполнения количества азота в растениях.
- Марка Б подходит для хранения и применения в домашних условиях. Продается в виде 1 и 2 сорта, расфасованная по 1кг. Может применяться для комнатных растений (после зимы), для подпитки рассады.
- Индийская селитра (аммиачно–калийная) используется для обогащения почвы калием. Для плодовых деревьев применяется в качестве подкормки ранней весной, для улучшения вкуса томатов вносится перед посевом.
Аммиачная селитра: применение в садоводстве
Особенности применения селитры аммиачной
Перед применением аммонийной селитры необходимо учесть тип почвы, климатические условия, вид растений.
Подкормку необходимо производить весной. В климатических зонах с повышенной влажностью эту процедуру нужно повторять и осенью. Это удобрение может применяться на всех видах почв, но с некоторыми особенностями.
Кислая почва
Для усиления действия аммония азотнокислого и устранения временного эффекта подкисления необходимо произвести нейтрализацию удобрения. Это можно осуществить, используя удобрение с известью или доломитом, в равных соотношениях.
Кислая дерново-подзолистая почва
Для достижения положительного эффекта должно осуществляться либо использование нитрата аммония с известью, либо регулярная нейтрализация повышенной кислотности.
Аммиачная селитра как удобрение
Серозем, чернозем
За счет наличия в составе почвы оснований, она не подкисляется. При введении удобрения образуется кальциевая или магниевая селитра.
Как рассчитать количество удобрения?
Количество используемого нитрата аммония зависит от плодовитости почвы. Если она плодовита, то необходимо использовать в пределах 25 г/кв. м, в противном случае дозировку необходимо увеличить до 40 г/кв. м. Внесение удобрения под рассаду можно как в сухом виде (5 г на лунку), так и в растворенном (около 35 г/10 л).
При посадке овощей селитра аммиачная может вводиться через 21 день после всходов, по 15 г/кв. м. При первичной обработке почвы количество может быть увеличено.
Для удобрения садовых растений нитрат аммония необходимо засыпать под ствол (20 г/кв. м).
Деревья удобряют сразу после цветения, а потом через 30 дней. После появления листьев можно использовать нитрат аммония в сухом виде. Для обработки приствольных кругов деревьев раствором (25 г/10 л) их необходимо избавить от листьев и веток.
Несмотря на то что нитрат аммония благоприятно влияет на растения и недорог, он имеет ряд недостатков:
- У кислых грунтов после введения удобрения кислотность еще повышается, что может повлечь за собой уменьшение урожайности.
- Возможно аккумулирование нитратов. По этой причине некоторые культуры (салат, зеленый лук) запрещено обрабатывать нитратом аммония. А такие овощи, как огурец, кабачок, салат, тыква, дыня и арбуз, удобрять не позднее рассадного периода.
- Водный раствор аммонийной селитры следует лить напуском или под корень. При попадании сухого или растворенного удобрения на листву возможны появления ожогов.
Удобрение Аммиачная селитра 1 кг
Хранение аммонийной селитры
Хранить удобрение необходимо в герметичной упаковке, дабы азот не испарился, и удобрение не потеряло своих положительных свойств.
Место для хранения должно быть сухим, хорошо проветриваемым, температура не должна превышать 30 градусов. Рядом не должны располагаться легкогорючие материалы. Следует избегать резкого перепада температуры, чтобы избежать процесса перекристаллизации. Нужно также предотвратить прямое попадание солнечных лучей (при нагревании нитрат аммония может непроизвольно взрываться).
Источник
Аммонийно-нитратные удобрения
Аммонийно-нитратные удобрения содержат азот сразу в двух формах: аммонийной и нитратной. Относятся к азотным удобрениям. Применяются во всех почвенно-климатических зонах, под любые культуры для основного, припосевного внесения и подкормок.
Содержание:
Получают аммонийно-нитратные удобрения на основе взаимодействия азотной кислоты с газообразным аммиаком.
Виды аммонийно-нитратных удобрений
К группе аммонийно-нитратных удобрений относится аммиачная селитра (NH4NO3), сульфо-нитрат аммония (NH4)2SO4*2NH4NO3+(NH4)SO4, известково-аммонийная селитра (NH4NO3*CaCO3). [5]
Аммиачная селитра
Аммиачная селитра
Для устранения этого нежелательного явления ее гранулируют, предварительно добавив тонкоразмолотую фосфоритную муку, гипс, каолинит, нитрат магния и другие вещества. [5] (фото)
Известково-аммонийная селитра
Сульфо-нитрат аммония (NH4)2SO4*2NH4NO3+(NH4)2SO4) (сульфат-нитрат аммония, монтан-селитра, лейна-селитра). Содержит 25–27 % азота, из них в аммонийной форме 18–19 % и в нитратной 7–8 %. Внешне сульфат аммония – сероватое мелкокристаллическое или гранулированное вещество. Хорошо растворим в воде, гигроскопичность меньше, чем у аммонийной селитры. При хранении в сухом помещении сохраняет рассыпчатость.
По действию на растения и поведению в почве близок к сульфату аммония, однако обладает значительной потенциальной кислотностью, поэтому при применении на кислых почвах необходимо проводить предварительное известкование или нейтрализацию самого удобрения. [5]
Виды аммонийно–нитратных удобрений
Применение
Сельское хозяйство
Аммонийно-нитратные удобрения применяются в качестве минеральных удобрений для повышения плодородия почв. [3]
Промышленность
Аммонийно-нитратные удобрения находят применение в различных отраслях промышленности. Так, аммиачная селитра применяется для производства взрывчатых веществ и в атомной энергетике. [4]
Поведение в почве
При внесении в почву аммонийно-нитратные удобрения быстро растворяются в почвенном растворе и диссоциируют на катионы и анионы.
Аммонийная составляющая удобрений (NH4 + ) вступает в обменные реакции с ионами твердой фазы почвы и в дальнейшем трансформируется так же, как и азот аммонийных удобрений. [3]
Нитратная составляющая – анион NO — 3 – в теплое время года сразу поглощается корневой системой растений. Осенью, зимой и весной он свободно мигрирует в почве с грунтовыми водами и может вымываться из корнедоступного слоя. Поведение нитратной группы в почве аналогично нитратным удобрениям. [3]
Сера в составе сульфо-групп(SO4 2- ) легкодоступна растениям и быстро поглощается из почвенного раствора корневыми системами. [2]
Известь CaCO3 известна как идеальное средство нейтрализации кислотности почв и обеспечения их кальцием. [5]
Применение на различных типах почв
Аммонийно-нитратные удобрения с некоторыми нюансами используются в различных почвенно-климатических условиях.
Источник
Нитрат аммония
наименование
210 °C