Глава 12 ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ В ПОЧВАХ
Одним из факторов фазовых переходов веществ в почвах являются окислительно-восстановительные процессы. Многие из них обратимы, и соединения элементов с переменной зарядностью многократно переходят из одной фазы в другую.
Окислением (Ох) в химии называется процесс отдачи электронов химическими элементами, а восстановлением (Red) — их приобретение:
Ox 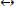
Окисление одного элемента, отдающего электроны, обязательно сопровождается восстановлением другого элемента, приобретающего их. Поэтому говорят об окислительно-восстановительных реакциях или процессах.
Главным окислителем в почвах является кислород почвенного воздуха и растворенный в почвенной влаге. В качестве восстановителей выступают органическое вещество, водород и сероводород. Некоторые реакции окисления, как, например, органических веществ, необратимы. Гумификация и минерализация органических остатков при достаточном доступе кислорода воздуха — процесс окислительный — необратимый.
Многие окислительно-восстановительные процессы имеют обратимый характер: химические элементы многократно могут переходить из окисленного в восстановленное состояние и обратно. Широко распространены обратимые процессы окисления и восстановления железа (Fe 3+ 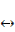
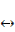
В обратимых окислительно-восстановительных процессах один и тот же элемент в зависимости от степени ионизации и условий среды (кислородной О2, бескислородной глеевой СН4, сероводородной H2S) является или окислителем, или восстановителем.
Состояние окислительно-восстановительных условий в почве
характеризуется особым показателем — окислительно-восстановительным потенциалом (ОВГ1) атомов или ионов относительно какой-либо стандартной окислительно-восстановительной реакции, потенциал которой приравнивается к нулю. В качестве такой реакции принято считать переход водорода из газообразного состояния в состояние иона:
Потенциал окислительно-восстановительной системы (в данном случае почвы) по отношению к нормальному водородному электрону обозначается индексом Eh; Eh = Е0 +0,0291g 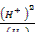
низких значениях Eh, чем в кислой (рис. 12.1). Кислотно-щелочные
условия окислительно-восстановительных реакций учитываются введением показателя гН2:
гН2 = 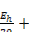
Значения Eh колеблются от 600—750 мВ в хорошо аэрируемых почвах с окислительным режимом до 150—200 мВ в почвах переувлажненных с восстановительными условиями; в резко восстановительной сероводородной обстановке Еh опускается ниже нуля и приобретает отрицательные значения.
Окислительно-восстановительные процессы зависят от кислотно-основных условий (рН), в частности, эти условия влияют на степень растворимости продуктов окисления или восстановления, активность микроэлементов и др. (см. рис. 12.1). Поэтому для сопоставления окислительно-восстановительных условий в почвах с различным значением рН пользуются показателем rН2. При значениях rН2 27—30 — условия окислительные, в интервале 27—20 — восстановительные,
По характеру протекающих окислительно-восстановительных процессов А.И. Перельман выделил три ряда почв:
1) почвы с преобладанием окислительной среды;
2) почвы с восстановительной глеевой обстановкой;
3) почвы с резковосстановительной сероводородной обстановкой.
И.С. Кауричев и Д.С. Орлов дали в соответствии с окислительно-восстановительным режимом и его динамикой более детальную группировку почв.
1.Почвы с абсолютным господством окислительной обстановки — автоморфные почвы степей, полупустынь и пустынь.
2.Почвы с господством окислительных условий при возможном проявлении восстановительных процессов в отдельные влажные годы или сезоны — автоморфные почвы таежно-лесной зоны, влажных субтропиков и широколиственных лесов.
3.Почвы с контрастным окислительно-восстановительным режимом (полугидроморфные почвы различных зон):
а) с развитием сезонных восстановительных процессов в верхних горизонтах;
б) с развитием оглеения в нижних горизонтах;
в) с контрастной сменой окислительной и восстановительной обстановок по всему профилю.
4.Почвы с господством восстановительных условий по всему профилю:
а) с господством глеевой обстановки;
б) с господством сероводородной обстановки.
Окислительно-восстановительный режим в почвах имеет большое значение в почвообразовании и плодородии почв. С ним связаны скорость и направление разложения органических остатков, гумификация и минерализация органических веществ.
Окислительно-восстановительные процессы контролируют фазовые переходы в почвах. Многие химические соединения элементов с переменной зарядностью при смене окислительно-восстановительных условий многократно переходят из твердой фазы в жидкую, из жидкой в газовую и обратно. В почвах гумидных областей с периодическим переувлажнением широко распространены реакции окисления и восстановления железа (Fe 3+ 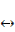
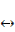
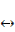
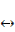
В зависимости от водно-теплового режима, режима кислотно — щелочных условий и биологической активности рассмотренные выше процессы фазовых превращений веществ в почвах приобретают определенный ритм: суточный, сезонный и многолетний.
В своей совокупности они характеризуют современную динамику почв. Изучение динамики почв имеет большое практическое значение, так как является научной основой для регулирования почвенных процессов и управления ими в целях повышения плодородия почв.
Источник
Окислительно-восстановительные процессы в почвах



Окислительно-восстановительные процессы в почве широко развиты.
Процессами окисления называются:
1) присоединение кислорода
2) отдача водорода
3) отдача ẽ без участия кислорода и водорода:
Обратные процессы называются восстановлением.
Обычно считают, что окисление процесс отдачи ẽ, а восстановление – присоединение.
— окисление тирозина и других ароматических аминокислот;
— окисление смол и соединений непредельного ряда;
— окисление дубильных веществ, сахаров и аминокислот.
Гумификация в целом процесс тоже окислительный.
Большинство реакций окисления органических веществ почвы относятся к группе необратимых.
Обратимыми окислительно-восстановительными реакциями являются широко развитые в почве реакции окисления и восстановления железа (Fe 3+ D Fe 2+ ), марганца (Мn 4+ D Mn 2+ ) и азота (N 5+ D N 3+ ).
В почве происходит окисление и восстановление кислорода, водорода и серы (О D О 2- ; Н D Н + )
Условия, определяющие интенсивность и направленность окислительно-восстановительных процессов:
1. Состояние увлажнения и аэрации почв.
2. Содержание в них органического вещества;
3. Температура, при которой протекают биохимические реакции;
4. Наличие и интенсивность в них микроорганизмов.
Для количественной характеристики окислительно-восстановительного состояния почвы используют окислительно-восстановительный потенциал. Он отражает суммарный эффект разнообразных окислительно-восстановительных систем почвы в данный момент. Обозначается Еh.
Для получения сравнимых данных по окислительно-восстановительным условиям в средах с различной величиной рН был введен показатель чН2. Он представляет собой отрицательный логарифм давления молекулярного водорода
Таким образом, количественная характеристика окислительно-восстановительного состояния почвы может быть выражена через Еh в милливольтах или через условную величину чН2.
Для гидроморфных почв типична некоторая гетерогенность окислительно-восстановительного состояния при преобладании восстановительных условий.
В полугидроморфных почвах с грунтовым дополнительным увлажнением характерен низкий окислительно-восстановительный потенциал для нижних оглеенных горизонтов.
Многие автоморфные почвы характеризуются пониженными показателями окислительно-восстановительного потенциала в верхних гумусовых горизонтах с постепенным их увеличением вниз по профилю. Такой тип распределения окисления-восстановления обусловлен тесной связью окислительно-восстановительных процессов с микробиологической деятельностью и особой ролью органического вещества как фактора микробиологической активности.
Окислительно-восстановительные процессы оказывают большое влияние на почвообразовательный процесс и плодородие.
С этими процессами тесно связаны превращения растительных остатков, темпы накопления и состав образующихся органических веществ, а, следовательно, и формирование почвенного профиля.
Избыточное увлажнение и низкие значения окислительно-восстановительного потенциала замедляют разложение растительных остатков, способствуют образованию наиболее подвижных и активных форм органических веществ, переходу гуминовых кислот в фульвокислоты.
С развитием окислительно-восстановительных процессов связано также превращение соединений азота, серы, фосфора, железа, марганца в почвах.
Знание окислительно-восстановительного потенциала почв позволяет судить об общей направленности окислительно-восстановительных процессов. Так, оптимальные условия для нитрификации Еh + 350 – 500 мВ, при резком падении потенциала развивается денитрификация.
Источник
Потенциалопределяющие системы в почвах.
Почвы содержат большой набор окислительно-восстановительных систем: Fe 3+ ↔ Fe 2+ , Mn 2+ ↔ Mn 3+ ↔ Mn 4+ , Cu + ↔ Cu 2+ , Co 2+ ↔ Co 3+ , NO3‾ ↔NO2‾ ↔ NН3‾, S 6 ‾ ↔ S 2 ‾.
Различают обратимые и необратимые окислительно-восстановительные системы. Обратимыми являются такие системы, которые в процессе изменения окислительно-восстановительного режима не меняют суммарный запас компонентов. Необратимые системы в процессе изменения окислительно-восстановительного режима утрачивают часть веществ. Эти вещества переходят в газообразное состояние или выпадают в осадок. Как правило, в почвах преобладают необратимые системы.
К обратимым окислительно-восстановительные системам относятся:
Система Fe 3+ ↔Fe 2+ . Эта система занимает особое место среди обратимых систем. Она чутко реагирует на малейшие изменения окислительно-восстановительной обстановки. Растворимость и подвижность соединений двухвалентного железа тем больше, чем ниже рН и ОВП. Растворимость соединений трехвалентного железа крайне низкая. Ионы окисного железа могут появляться в почвенных растворах только при рН меньше 3. Однако на растворимость соединений железа влияют не столько кислотно-щелочные, сколько окислительно-восстановительные условия. При Eh 860 мв 99% ионов железа находится в окисной форме, при Eh 640 мв — 99% представлено закисными формами. Увеличение Eh почвы на 5-6 мв уменьшает концентрацию ионов железа примерно в 2 раза.
Миграция соединений железа возможна главным образом в форме соединений двухвалентного железа в условиях повышенной кислотности и пониженного Eh.
Система Mn 2+ ↔Mn 4+ . Данная система является крайне чуткой к изменению ОВП. Соединения четырехвалентного марганца нерастворимы в условиях, характерных для почвенных горизонтов. Обменный марганец представлен двухвалентным катионом. Концентрация ионов двухвалентного марганца при повышении кислотности и понижении Eh возрастает в десятки тысяч раз. Возрастание Eh до 500-600 мв вызывает быстрый переход двухвалентного марганца в четырехвалентный и его уменьшение в растворе практически до следов. Изменение Eh на 5-6 мв приводит к увеличению растворимости марганца в 2 раза.
Миграция соединений марганца в ходе почвообразовательных процессов в вертикальном и горизонтальном направлениях сходна с миграцией соединений железа.
Миграция и аккумуляция соединений железа и марганца происходит при почвообразовании одновременно. Однако их соотношение в растворах и осадках в зависимости от рН и ОВП сильно меняется. В нейтральной и слабокислой среде при низком значении Eh в растворах преобладает марганец, в осадках – железо. В кислой среде при высоком Eh железо удерживается в растворе, марганец выпадает в осадок.
К необратимым окислительно-восстановительным системам относятся:
Система NO3 → NO2 → NО → N. Процессы нитрификации и денитрификации, протекающие под воздействием микроорганизмов, регулируются условиями Eh и концентрацией водородного иона. Процесс нитрификации и накопления нитратов происходит в условиях окислительного режима и при высоких Eh 400-500 мв. Увлажнение почвы снижает Eh и способствует развитию процессов денитрификации. Снижение Eh до 340 мв вызывает переход нитратов в нитриты, дальнейшее снижение приводит к образованию газообразных окислов азота и их исчезновение из почвы.
Система сульфаты ↔ сульфиды. Данная окислительно-восстановительная система играет большую роль во всех почвах, где присутствуют сернокислые соли. При участии микроорганизмов система сульфаты – сульфиды в присутствии органического вещества и недостатке кислорода сдвигается в сторону сульфидов. Происходит процесс восстановления сульфатов до сернистых металлов:
Под действием присутствующей в почве углекислоты сернистые металлы легко разлагаются и образуют бикарбонаты и карбонаты щелочных и щелочно-земельных металлов. При этом происходит процесс восстановления сульфатов:
Образующийся сероводород уходит в атмосферу. При этом развивается процесс десульфирования или десульфации почвенного раствора. Сернокислые соли постепенно исчезают, хлористые соли остаются в неизменном состоянии. В результате процессов десульфирования хлоридно-сульфатные растворы превращаются в хлоридные или карбонатно-хлоридные.
Однако в почвенном растворе содержание элементов с переменной валентностью достаточно мало. Поэтому почвенный раствор обладает невысокими ОВ-емкостью и буферностью, а величина Eh неустойчива.
Более существенное влияние на ОВ-процессы в почвах оказывает растворенный в почвенном растворе кислород, почвенная микрофлора и вода.
Почти все почвенные реакции происходят в водной среде, а сама вода может выступать и в качестве окислителя, и в качестве восстановителя. Именно это свойство воды определяет пограничные уровни проявления окислительно-восстановительных реакций. Предел окислительных условий – это окисление воды до молекулярного кислорода. Оно описывается уравнением:
Нижняя граница устойчивости воды обусловлена реакцией восстановления до водородного иона:
При рН 7 устойчивость воды определяется интервалом величин ОВП от +0,8 до – 0,3 В. Он характерен для природных почв. Значения выше + 0,8 и ниже — 0,3 могут быть созданы только искусственно при внесении больших доз окислителей или восстановителей. Вода в почвах служит ОВ-буфером с очень большой емкостью, ограничивающим диапазон встречающихся в почвах окислительно-восстановительных потенциалов.
Источник