Биотехнология
Это использование биологических систем и процессов в сельском хозяйстве и промышленности. Изначально биотехнологией называли микробиологическое производство – промышленное культивирование бактерий и грибов для получения продуктов их жизнедеятельности (например, антибиотиков). Сейчас биотехнология включает в себя генную и клеточную инженерию.
Генная инженерия
Это перенос генов в клетки другого организма (получение трансгенных организмов). Техпроцесс:
1) Получение гена. Из клетки выделяют иРНК, затем получают из них ДНК путем обратной транскрипции.
2) Получение рекомбинантной плазмиды. Плазмида – небольшая кольцевая молекула ДНК, характерная для прокариот. В неё вставляют ген, который необходимо перенести.
3) Перенос. Бактерии, например, сами поглощают ДНК из окружающей среды. В природе это является одним из механизмов изменчивости у бактерий.
4) Отбор. Отбирают организмы, в которых пересаживаемый ген содержится и работает.
Примеры использования генной инженерии:
- Инсулин получают из бактерии кишечной палочки с пересаженным человеческим геном инсулина.
- В культурное растение пересаживают ген устойчивости к гербициду, при обработке поля гербицидом все сорняки погибают, а культурное растение – нет.
- В культурное растение пересаживают ген яда, убивающего некоторые виды насекомых. Поле, засеянное этими растениями, не нужно обрабатывать инсектицидами.
- В рапс пересажен ген устойчивости к засолению почвы из другого растения.
Клеточная инженерия
Это конструирование новых клеток (с новыми свойствами). Примеры:
1) Клонирование. Ядро соматической клетки животного пересаживают в яйцеклетку и выращивают новый организм, при этом полностью сохраняются все наследственные признаки донора ядра.
2) Соматическая (клеточная) гибридизация. Например, сливают две клетки – В-лимфоциты, вырабатывающие антитела, и раковые клетки, способные неограниченно делиться – получают гибридные клетки, выделяющие антитела.
3) Культура клеток (тканей). Ткани и органы можно выращивать «в пробирке» на питательной среде. Например, гормон эритропоэтин получают из культур клеток хомяков.
4) Микроклональное размножение. У растений и грибов целый организм можно вырастить из одной или нескольких соматических клеток. Так можно получить посадочный материал, не содержащий вирусов.
Источник
Донорство митохондрий в клинической практике
Законодательство, принятое палатой лордов в 2015 году, позволило проводить пересадку митохондрий на территории Соединенного Королевства с целью предотвращения тяжелых митохондриальных заболеваний. Регулирование этой процедуры было поручено управлению по репродукции и эмбриологии человека, которое в 2017 году предоставило свою первую лицензию объединению больниц Фонда национальной службы здравоохранения (NHS) Ньюкасла-апон-Тайн. В настоящее время услуги по пересадке митохондрий (или «дети от трех родителей», как эту технологию называют в СМИ) в Англии и Уэльсе оказывает NHS.
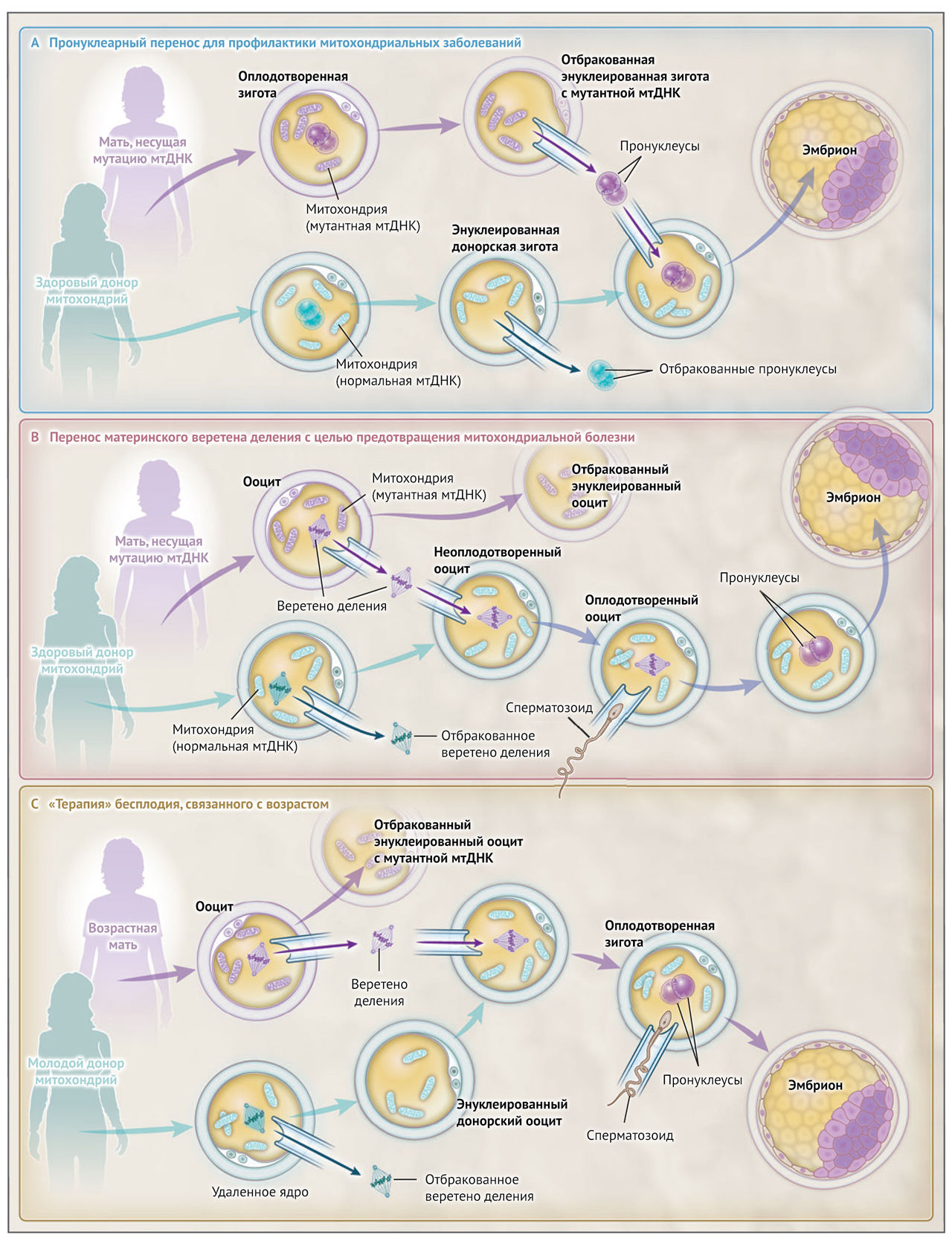
В 2016 году сообщалось, что женщина из Мексики родила здорового мальчика после пересадки веретена ооцитов, чтобы предотвратить передачу наследственной патологии митохондриальной ДНК (мтДНК) [1]. Однако настораживает, что метод стал применяться для лечения бесплодия во многих центрах репродуктологии по всему миру [2]. Понятие донорства митохондрий объединяет ряд методов, предназначенных для переноса митохондрий из одной клетки в другую. Эти методы включают в себя перенос цитоплазмы (с митохондриями) из донорского ооцита в ооцит или эмбрион реципиента. Перенос, как правило, осуществляется путем добавления или обмена небольшой доли общего цитоплазматического объема, как, например, при процедуре, которая была предложена в качестве лечения связанного с возрастом бесплодия.
Более экстремальная форма донорства митохондрий представляет собой обмен как можно большего объема цитоплазмы. Такая процедура была разработана с целью предотвращения передачи наследственных заболеваний мтДНК. На практике этот процесс достигается путем удаления пронуклеусов или ядерных веретен и помещения их в донорский эмбрион или ооцит (рис. 1). Перенос донорской цитоплазмы в яйцеклетку будущей матери для лечения женского бесплодия не новость, но мы пока располагаем лишь косвенными данными о связи возрастной дисфункции митохондрий с бесплодием. Пока нельзя со всей уверенностью утверждать, что митохондриальные дефекты, которые наблюдаются в ооцитах, полученных от пожилых женщин, увеличивают риск бесплодия, или же они являются просто случайным побочным эффектом процесса старения.
Более того, неизвестно, улучшает ли фертильность перенос митохондрий сам по себе. Описанная в литературе польза от этой процедуры, если она реальна, может быть связана с переносом цитоплазматического содержимого, которое неизбежно сопровождает любую форму митохондриального донорства. Эти опасения лежат в основе недавнего моратория, предложенного Европейским обществом репродукции человека и эмбриологии (ESHRE) на основе рекомендации группы экспертов, которые пришли к выводу, что «применение переноса митохондрий в качестве средства для лечения бесплодия остается сомнительным и недоказанным». Группа также сделала заявление о безопасности этой процедуры: «На данном этапе, и до тех пор, пока эта технология не доказала свою эффективность и безопасность, ESHRE настоятельно не рекомендует использовать донорство митохондрий для терапии бесплодия».
Такое заявление привлекло внимание к новым данным о взаимодействии между митохондриями и ядром клетки [2] и указало на возможность возникновения осложнений. Должно ли беспокойство о последствиях влиять на нашу позицию о донорстве митохондрий в целом, включая его применение для предотвращения редких наследственных заболеваний мтДНК? В конце концов, будущая мать с патогенной мутацией в мтДНК с такой же вероятностью захочет иметь здорового ребенка, как и мать с бесплодием. До 2015 года некоторые свидетельства, что митохондриальный перенос может оказывать неблагоприятное воздействие, основывались на экспериментальной работе по изучению инбредных линий лабораторных мух и мышей, у которых низкий уровень гетерозиготности создает совершенно иную ситуацию, чем в гетерогенной человеческой популяции. У людей мтДНК и ядерная ДНК, по-видимому, свободно комбинируются без каких-либо последствий для организма. Однако в трех лабораториях наблюдался непредвиденный возврат к исходному генотипу мтДНК приблизительно у 15 % клонов эмбриональных стволовых клеток, полученных от эмбрионов человека после переноса митохондрий.
Эти возвраты включали в себя тяжелую патогенную мутацию мтДНК, которая вызывает болезнь Лея (подострая некротизирующая энцефаломиопатия), неврологическое расстройство, которое обычно диагностируется в первые годы жизни [3–5]. Риск реверсии можно снизить с помощью традиционных методов диагностики как до, так и после имплантации, но причины возвратов в исходное состояние неизвестны. В настоящее время есть доказательства того, что митохондрии это не просто клеточные «блоки питания», которые можно заменить, когда они исчерпали свой ресурс. У мышей обмен мтДНК между здоровыми, хотя и инбредными, лабораторными линиями привел к несоответствию между ядерным и митохондриальным геномами, которые не могут сосуществовать в одной и той же линии. Такое несоответствие может привести к кардиометаболическим фенотипам, которые проявляются у мышей только в пожилом возрасте [5].
Тем не менее несколько обезьян, рожденных с использованием этого метода, кажутся здоровыми, что дает некоторую надежду. Не существует объективных доказательств эффективности митохондриального переноса для лечения бесплодия, поэтому его не следует использовать в обычной клинической практике. И будет ли клиническое испытание этого метода этически приемлемым, если есть неопределенность в отношении побочных эффектов? Как это часто бывает в медицине, новые методы лечения сначала тестируются при более тяжелых заболеваниях. Могут ли митохондриальные заболевания стать полигоном для проверки? В отличие от донорства митохондрий с целью лечения бесплодия, использование данного метода для предотвращения митохондриальных заболеваний имеет четкое научное обоснование его преимуществ, но что мы знаем о рисках? Обычно приводится аргумент, что риск возникновения тяжелой неизлечимой болезни мтДНК уравновешивает теоретические риски экспериментального лечения.
Однако предотвращение митохондриальных заболеваний это не то же самое, что лечение митохондриальных заболеваний. До митохондриального переноса ребенка еще нет. Риски для ребенка возникают из-за самого лечения, и основное его преимущество заключается в том, чтобы дать будущим родителям возможность зачать ребенка, который с одной стороны наследует их ядерный геном, а с другой стороны не несет патогенную мутацию мтДНК. В Великобритании управление репродукции человека и эмбриологии разумно обосновало необходимость долгосрочного мониторинга состояния здоровья всех детей, родившихся в результате донорства митохондрий. Поскольку развитие гипотетических побочных эффектов может занять годы, если не десятилетия [6], полное прояснение этих вопросов займет некоторое время. Причина, по которой в настоящее время приемлемо предлагать донорство митохондрий в одном контексте, но не в другом, зависит исключительно от научного обоснования процедуры, а не от риска побочных эффектов. В том случае, если будет установлен механизм предотвращения бесплодия посредством донорства митохондрий, можно будет рассматривать возможность проведения клинического испытания донорства митохондрий для лечения бесплодия, когда все другие варианты потерпели неудачу. До тех пор, пока не будут проведены такие испытания, лечебные центры, предлагающие эту процедуру сегодня, должны прекратить это делать, и врачи должны предупреждать пациентов об отсутствии доказанной эффективности.
Источник
Трое в лодке: о легализации замены митохондрий
12 февраля 2015
Трое в лодке: о легализации замены митохондрий
Автор
Редактор
Недавно появилась надежда, что дети в Соединенном королевстве смогут иметь трех родителей: члены палаты общин парламента Великобритании проголосовали за легализацию процедуры замещения митохондрий. Идея одобренной технологии состоит в экстракорпоральном оплодотворении, в котором принимает участие материал от трех разных доноров, что позволяет предотвратить передачу наследственных митохондриальных заболеваний от матери ребенку.
Митохондриальная ДНК и ее «поломки»
Как известно, митохондрии — органеллы, отвечающие за энергоснабжение клетки, — несут собственную генетическую информацию, записанную в митохондриальной ДНК (мтДНК)*. Число генов в мтДНК обычно намного меньше, чем в «основной» ДНК клетки. Так, у человека мтДНК содержит последовательности 37 генов, из которых белок-кодирующими являются 13 (остальные последовательности кодируют рибосомальные и транспортные РНК) [1].
* — Несмотря на долгую ко-эволюцию, эта молекула по-прежнему немножко чужак для нашего организма: «Митохондриальная ДНК как иммуноген» [2]. Даже считываться и копироваться «по-людски» она так и не научилась: «Исследован переключатель процессов транскрипции и репликации в митохондриях» [3] — Ред.
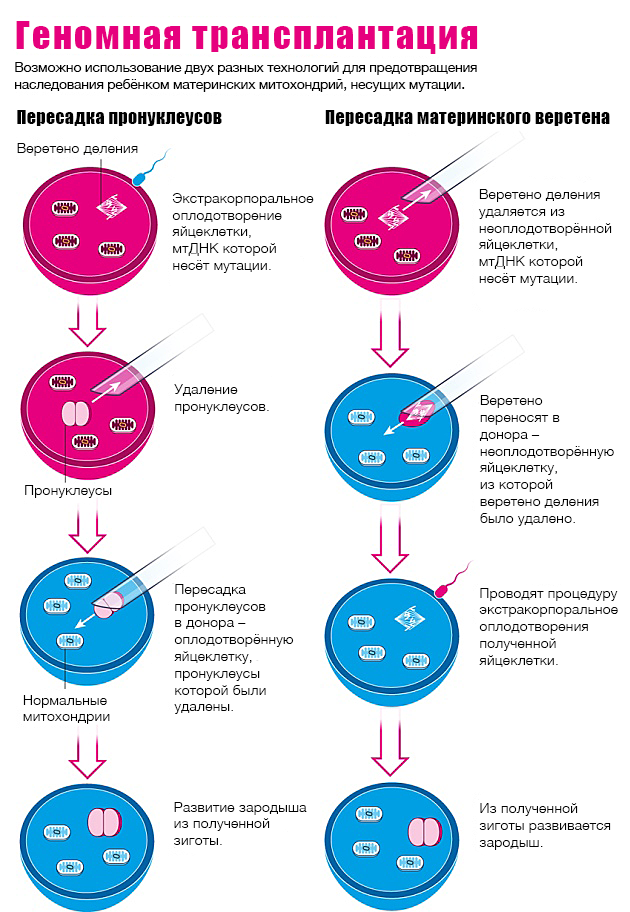
Рисунок 1. Геномная трансплантация: эксперименты по замене митохондрий. Инфографика из [5], адаптирована для русскоязычной аудитории.
Конечно, как и любая другая, митохондриальная ДНК подвержена накоплению мутаций, что может в конечном итоге приводить к тяжелым заболеваниям. Как правило, в первую очередь нарушаются функции тканей, потребляющих наибольшее количество энергии, — мозга, сердца, мышц. Cиндром Барта, синдром Лея, митохондриальная энцефаломиопатия, особая миоклоническая эпилепсия — это лишь малая часть длинного списка заболеваний, обусловленных повреждениями митохондрий [4].
В ходе оплодотворения именно материнские митохондрии (митохондрии яйцеклетки) передаются особи следующего поколения. Значит, накопленные в мтДНК матери мутации будут переданы ребенку. По оценкам, 1 из 5000 детей рождается с заболеваниями, вызванными такими мутациями [5]. И очень часто «семейные лодки» разбиваются о тяжелейший быт, связанный с воспитанием больного ребенка.
Замена митохондрий: истребляем недуг в зародыше
Предотвратить наследование губительных мутаций можно с помощью незамысловатой — на словах — процедуры, в основе которой лежит использование митохондрий от «третьего родителя». Разумеется, это можно сделать только при проведении экстракорпорального оплодотворения (ЭКО) [6]. Сначала готовят два набора клеток: яйцеклетки матери, содержащие дефектные митохондрии, и яйцеклетки женщины-донора с митохондриями, ДНК которых не несет опасных мутаций. Затем исследователи извлекают ядра материнских яйцеклеток и заменяют ими ядра яйцеклеток-доноров мтДНК. Альтернативным способом является пересадка пронуклеусов — мужского и женского — из оплодотворенной яйцеклетки. Обе технологии геномной трансплантации изложены в форме инфографики (рис. 1).
Заключительное слово
28 января 2015 года в журнале The New England Journal of Medicine было опубликовано письмо исследователей из университета Ньюкасла, в котором авторы отметили, что процедура замены митохондрий сможет помочь более чем двум тысячам британских женщин — по оценке ученых, именно столько представительниц прекрасного пола в Соединенном королевстве несет опасные мутации мтДНК [7].
Принятое решение можно без сомнения считать триумфом ученых, ведь удалось изменить закон, разрешающий эксперименты по геномной трансплантации исключительно в исследовательских целях.
Однако до безоговорочной победы еще далеко: палате лордов предстоит вынести свое решение по вопросу легализации применения технологии в клинической практике. Если закон будет одобрен палатой лордов, в силу он вступит только в октябре текущего года. Более того, клиникам, желающим предоставлять обсуждаемый вид генной терапии, будет необходимо получить специальное разрешение от Управления по оплодотворению и эмбриологии человека Великобритании (HFEA). И все же вероятно, что путь новой технологии до «клиники» и общественного признания не будет столь тернист, как это случилось с методом ЭКО, разработчики которого десятилетиями отбивались от «богоугодников» [6].
Исследователи надеются, что принятое палатой общин парламента Великобритании решение послужит толчком к принятию подобных решений правительствами других стран.
Источник
Молекулярное клонирование, или как засунуть в клетку чужеродный генетический материал
30 октября 2011
Молекулярное клонирование, или как засунуть в клетку чужеродный генетический материал
Клонирование овечек имеет лишь самое опосредованное отношение к молекулярному клонированию. На фоне овечки Долли показана плазмида phMYT1L-N106.
коллаж автора статьи
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Огромное количество биологических исследований начинается с того, что в клетку вносится чужеродный генетический материал. Это действие называется молекулярным клонированием. С его помощью можно получить генетически модифицированные организмы, включить и выключить отдельные гены или определить роль конкретного белка в каком-нибудь процессе. Можно сказать, что молекулярное клонирование — это краеугольный камень, основа основ, фундамент, без которого множество замечательных методик было бы неосуществимо. Однако засунуть в клетку «неродную» ДНК не так-то просто: это длинный, трудоемкий и многоэтапный процесс. Молекулярному клонированию посвящены толстые книги, но, тем не менее, я попробую хотя бы немного рассказать о том, что это такое, и что нужно для того, чтобы все получилось.
«Био/мол/текст»-2011
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2011 в номинации «Лучшая обзорная статья».
Вставка
Раз мы собираемся вставлять в клетки какой-то ген, то самый первый, очевидный шаг, который нам нужно сделать, — этот ген как-нибудь получить, причем желательно в больших количествах (поскольку все методики несовершенны, бóльшая часть копий этого гена бесследно пропадет по дороге нецелевым способом). Чужеродный ген, вносимый в клетку, называется «геном-вставкой» или просто «вставкой». Получить его можно несколькими способами.
Во-первых, мы можем просто выделить его из того генома, к которому он принадлежит. Допустим для простоты, что наша вставка — это какой-нибудь ген слона. Тогда нам нужно:
- получить образец тканей слона;
- извлечь из этого образца ДНК;
- вычленить из этой ДНК интересующий нас ген и получить его в больших количествах (для этого используется ПЦР ). [Заметим в скобках, что получение гена с помощью ПЦР возможно, только если мы знаем его нуклеотидную последовательность или хотя бы последовательность его начала и окончания (для того, чтобы можно было синтезировать праймеры). Если же все это нам неизвестно, то придется сначала анализировать слоновий геном.]
Подробнее с методом ПЦР и другими основными молекулярно-биологическими методиками можно ознакомиться в статье «Важнейшие методы молекулярной биологии и генной инженерии»; с геномными исследованиями — в статье «Геном человека: как это было и как это будет». — Ред.
Во-вторых, вполне возможно, что нужный нам ген уже был выделен из генома слона и присутствует в библиотеке генов. Тогда нашу вставку можно будет получить оттуда (с этим, на самом деле, тоже придется повозиться, но меньше, чем в первом случае).
И наконец, в-третьих, не обязательно использовать в качестве вставки уже существующий ген. Если исследователь собирается работать с каким-нибудь геном, который является плодом его фантазии и не встречается в природе, то он может синтезировать его искусственно.
Вектор
Запускание в клетку «одинокой» вставки (то есть, гена самого по себе, безо всякого сопровождения) — дело совершенно бесперспективное. В клетке плавает множество расщепляющих ДНК ферментов (нуклеаз), которые с радостью набросятся на беззащитную вставку и разрежут ее на кусочки, в результате чего она бесславно исчезнет, не успев совершить ничего полезного, а клонирование провалится.
Поэтому, чтобы защитить вставку, ее встраивают в специальное «транспортное средство», которое называется вектором. В самом элементарном случае вектор — это просто последовательность ДНК, в которую вшивается наша вставка, и которая помогает ей не пропасть в клетке и выполнить свое предназначение. Существует несколько видов векторов, но среди исследователей самой большой (и заслуженной) любовью пользуется один из них — плазмиды. С них-то мы и начнем.
Плазмида
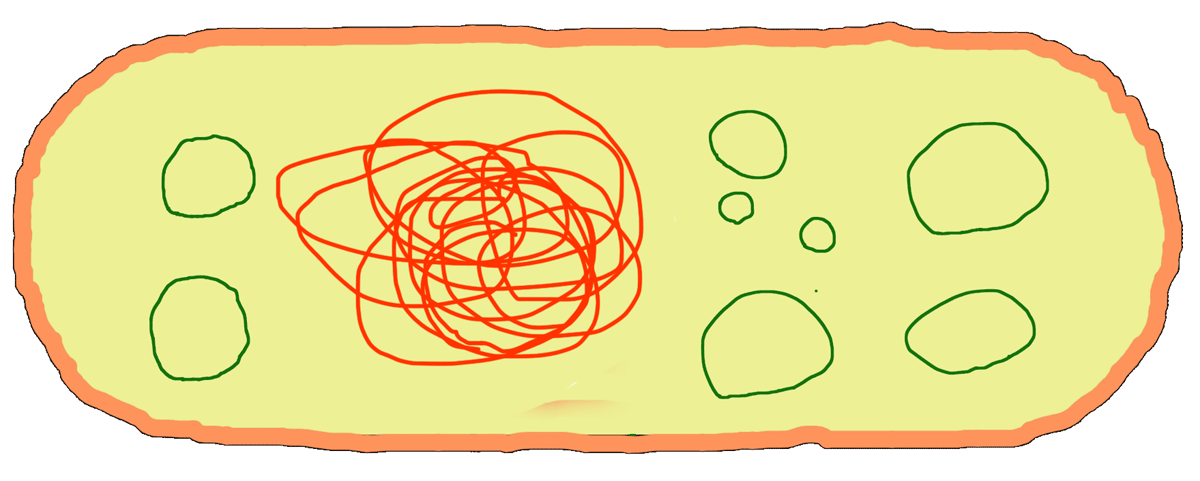
Плазмида — это довольно короткая и обычно кольцевая молекула ДНК, которая плавает в цитоплазме бактериальной клетки (зеленые кружочки на рис. 1). Плазмиды не связаны с бактериальной хромосомой, они могут реплицироваться независимо от нее, могут «выплевываться» бактерией в окружающую среду или, наоборот, из этой окружающей среды «проглатываться». С помощью плазмид бактерии обмениваются друг с другом генетической информацией, — например, передают соседям устойчивость к какому-нибудь антибиотику.
Рисунок 1. В бактериальной клетке наряду с бактериальной хромосомой плавает еще и множество плазмид.
рисунок автора статьи
Плазмиды существуют внутри бактерий в естественных условиях, поэтому никто не может помешать исследователю искусственно синтезировать плазмиду, которая будет обладать нужными для него свойствами, вшить в нее вставку (или несколько) и запустить в клетку. Плазмида — это, можно сказать, «болванка» для молекулярного биолога. Поэтому плазмиды стараются сделать как можно более универсальными и подходящими для всех случаев жизни.
Для того, чтобы из плазмиды получился рабочий вектор, она должна обладать некоторыми важными характеристиками.
Размножение
Прежде всего, плазмида обязательно должна в клетке размножаться, реплицироваться, потому что иначе она быстро подвергнется деградации, а вместе с ней исчезнет и ген-вставка. Для этого в ней должна быть специальная последовательность под названием «точка начала репликации», с которой и начинается удвоение ДНК. У разных видов живых существ эти точки имеют разную нуклеотидную последовательность. Поэтому, если мы хотим создать плазмиду, которая бы реплицировалась сразу в двух видах клеток (например, и в дрожжевых, и в бактериальных), то нам надо вставить в нее две точки начала репликации.
Разрезание
Кроме того, в ДНК плазмиды должны быть участки, в которых ее можно будет разрезать, чтобы вшить туда вставку. В качестве «ножниц» используются особые ферменты — рестриктазы. Они прекрасны тем, что режут ДНК не где попало, а в строго определенных местах, которые называются сайтами рестрикции (каждая рестриктаза распознает только свой сайт и только в нем (или возле него) разрезает ДНК). Обычно в плазмиду ставят множество разных сайтов рестрикции, расположенных в разных точках, — благодаря этому ее можно будет разрезать в нужном месте нужной рестриктазой. Участок ДНК, на котором собрано несколько сайтов рестрикции, называется полилинкером.
Селекция
Процесс, при котором бактерия «глотает» плазмиду, именуется трансформацией. В естественных условиях трансформироваться может в каждый момент времени не вся популяция бактерий, а только ее часть — компетентные клетки. Существуют лабораторные методы, с помощью которых можно искусственно увеличить количество компетентных клеток (некоторые из них описаны ниже в главе «Как засунуть вектор в клетки»), однако, все равно, стопроцентная компетентность для бактериальной культуры — вещь недостижимая.
Так что, добавляя плазмиду к бактериям, мы заранее должны смириться с тем, что бóльшая часть бактериальных клеток так и останется бесплазмидной, нетрансформированной. Поэтому нам придется отделять зерна от плевел, — то есть, трансформированные клетки от всех остальных. Для этого используется простой, но остроумный прием.
Допустим, мы встроили в нашу плазмиду ген устойчивости к какому-нибудь антибиотику (такой ген называется селективным маркером). Теперь клетки, которые «съели» плазмиду, будут неуязвимы для этого антибиотика и смогут спокойно жить в его присутствии. В результате, чтобы выделить из всех бактерий, к которым мы добавили плазмиду, те, которые смогли эту плазмиду использовать по назначению, нам достаточно будет добавить к бактериальной культуре соответствующий антибиотик. Те клетки, которые нам нужны, смогут существовать и делиться в присутствии этого антибиотика, а остальные этого делать не смогут.
Существуют и другие способы провести селекцию. Можно, например, поместить сайт рестрикции не внутрь гена антибиотика, а внутрь какого-нибудь «заметного» гена (скажем, такого, в присутствии которого бактериальные культуры меняют цвет). В результате можно будет отличить нужные колонии от ненужных просто на глаз, безо всяких манипуляций. По такому принципу работает, например, очень модная сейчас система бело-голубой селекции.
Если мы собираемся работать только на бактериях, то всем вышесказанным дело и ограничится. Однако если конечная наша цель — засунуть вектор в эукариотические клетки (например, клетки млекопитающих), то нам предстоит еще один этап селекции.
Дело в том, что в большинстве эукариотических клеток плазмиды живут недолго и быстро подвергаются деградации. Поэтому, даже если мы заставили клетку «съесть» плазмиду, не стоит питать надежды, что наша вставка теперь останется в этой клетке навсегда. Скорее всего, она успеет только немного поэкспрессироваться, прежде чем содержащий ее вектор будет пойман нуклеазой и разрезан на кусочки. Однако если вектор случайно смог встроиться в геном (это событие очень редкое, но не невероятное), то наша вставка, можно сказать, пустит в этой клетке корни — причем не только в ней самой, но и во всех ее потомках. И для того, чтобы выделить из всех клеток те, которые имеют вектор в своем геноме, нам понадобится еще один селективный маркер — ген устойчивости к какому-нибудь эукариотическому антибиотику (потому что бактериальные антибиотики, как правило, на клетки эукариот не действуют). Добавив соответствующий антибиотик (например, генетицин) к среде, в которой культивируются клетки, мы через некоторое время получим популяцию только тех клеток, в геноме которых сидит наш вектор.
Промоторы
Перед каждым рабочим геном находится короткий участок ДНК под названием промотор. Именно сюда прикрепляется фермент РНК-полимераза, который синтезирует РНК на матрице ДНК, что является первым и абсолютно необходимым этапом в экспрессии гена. Если у гена нет промотора, его экспрессию запустить невозможно, и он так и останется «молчащим». Можно сказать, что ген без промотора — это все равно, что машина без педали газа. Поэтому в нашей плазмиде обязательно должен быть хотя бы один промоторный участок, под контроль которого можно будет поставить ген-вставку.
А промоторы бывают разные.
Во-первых, они различаются по своей силе. Некоторые вызывают бурную транскрипцию подконтрольного гена, другие — совсем вялую.
Во-вторых, у прокариот и эукариот промоторы отличаются. Прокариотические промоторы не работают в эукариотических клетках и наоборот. Поэтому будет Ужасной Ошибкой поставить тот ген, который должен, экспрессироваться в бактериальных клетках, под эукариотический промотор — это все равно, что оставить его без промотора вообще.
В-третьих, у эукариот есть несколько типов РНК-полимеразы — они обеспечивают синтез различных видов РНК. И каждый тип РНК-полимеразы распознает только свои промоторы и «не видит» чужие. Поэтому, в зависимости от того, какую именно РНК кодирует наша вставка (например, матричную или, наоборот, шпилечную, а может, и вовсе рибосомальную), нам нужно подбирать и тип промотора, который мы будем ставить в плазмиду.
И, наконец, в-четвертых, разные промоторы включаются по-разному. Некоторые активны постоянно. Другие активизируются только при определенных условиях — например, при повышении окружающей температуры или появлении в клетке каких-то веществ. К тому же, у многоклеточных организмов в каждой ткани включены одни промоторы и выключены другие. Можно, например, подобрать такой промотор, который будет активен только в нейронах. Или только в нейронах головного мозга. Или только в нейронах головного мозга, относящихся к одному из подкорковых ядер. Или только в крохотной субпопуляции нейронов головного мозга, относящейся к одному из подкорковых ядер. И сужать этот круг можно почти до бесконечности.
Знание всего этого дает исследователю удивительную свободу. Подобрав в плазмиду подходящий промотор, он сможет творить с экспрессией гена-вставки почти все, что ему заблагорассудится. Ну, скажем, сделать так, чтобы он экспрессировался сильно, только в мышечных клетках и только в ответ на повышение температуры.
Трансляция белка
Засовывая вектор в клетку, ученый может хотеть двух разных вещей:
- чтобы происходила только транскрипция гена-вставки (то есть, синтез РНК на матрице ДНК — например, этого достаточно, если в клетку вносится какая-нибудь некодирующая РНК);
- чтобы происходила и транскрипция, и трансляция гена-вставки (то есть, экспрессия кодируемого вставкой белка).
В первом случае вектор называется транскрипционным, во втором — экспрессионным. Экспрессионные векторы обычно немного сложнее транскрипционных, потому что в них присутствуют:
- Консенсусная последовательность Козак. Это длинное имя носит короткий (примерно в 10 нуклеотидов) фрагмент в самом начале молекулы матричной РНК, который через белки-посредники обеспечивает связывание этой мРНК с рибосомой (без чего, как нетрудно догадаться, синтез белка невозможен). Последовательность Козак характерна только для эукариот, причем у представителей разных видов она немного отличается. Поэтому, создавая экспрессионный вектор, надо вставлять в него последовательность, которая характерна именно для того живого существа, в клетки которого мы собираемся вставлять вектор. Кроме того, последовательность Козак бывает сильной и слабой — то есть, приводящей к синтезу большого или малого количества белка. У прокариот роль последовательности Козак выполняет последовательность Шайна-Дальгарно, которая непосредственно (в смысле — без посредников, в отличие от последовательности Козак) соединяется с рибосомой, после чего и начинается синтез белка;
- Последовательность Козак находится перед вставляемым геном. А после него должны находиться еще несколько коротких участков, к которым присоединяются белки, выполняющие полиаденилирование — пришивание к концу свежесинтезированной РНК полиаденинового хвоста. Этот хвост выполняет несколько функций, в том числе, обеспечивает экспорт РНК в цитоплазму и помогает организации трансляции — то есть, если мы хотим обеспечить синтез белка на основе нашей РНК, нам без него не обойтись;
- мРНК, которая служит матрицей для синтеза белка, может быть транскрибирована только и исключительно РНК-полимеразой II типа. Поэтому нам нужно вставить в плазмиду именно тот промотор, который работает с этой РНК-полимеразой.
Итак, мы подобрали все необходимые для плазмиды кусочки. Но мало просто соединить их вместе — огромную роль играет их взаимное расположение. Например, сайты рестрикции должны быть не только многочисленны и разнообразны, но и находиться в «правильных» местах. При этом надо стараться, чтобы итоговая плазмида была как можно компактней, поскольку, во-первых, так она будет стабильнее, а во-вторых, охотнее «проглотится» клеткой. Одним словом, вы уже, наверное, поняли, что дизайн хорошей плазмиды — это тонкое и филигранное искусство (рис. 2).
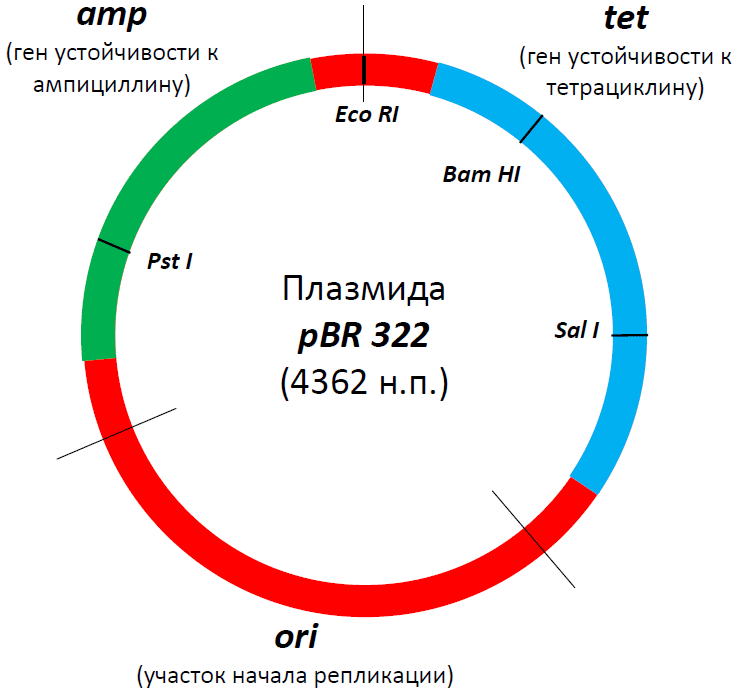
Рисунок 2. Структура знаменитой плазмиды PBR322. В свое время это была, пожалуй, самая популярная плазмида во всем научном мире, а потом она стала основой для множества плазмид нового поколения. В ней есть участок начала репликации (ori), благодаря которому она может размножаться в клетках бактерии E. coli, гены устойчивости к двум антибиотикам — ампициллину (amp) и тетрациклину (tet), а также множество сайтов рестрикции (на самом деле их больше сорока, но здесь представлены только четыре — EcoRI, SalI, PstI, BamHI). Промоторные участки, к сожалению, не показаны, но они, разумеется, тут тоже есть. Некоторые сайты рестрикции находятся в генах устойчивости к ампициллину или тетрациклину, в результате чего и тот и другой сайт можно использовать в качестве второго селективного маркера. Например, если мы разрежем ген устойчивости к ампициллину с помощью рестриктазы PstI и вошьем в это место вставку, то тетрациклин будет первым селективным маркером, ампициллин — вторым, а селекция будет выглядеть так:
- Трансформируем бактерии, выращиваем их на среде с тетрациклином и выбираем только хорошо растущие клоны.
- Переносим эти клоны на среду с ампициллином и выбираем те, рост которых угнетается.
Если же мы вошьем вставку внутрь гена устойчивости к тетрациклину (разрезав его с помощью рестриктаз BamHI или SalI), то нам надо будет, наоборот, сначала посадить их на среду с ампициллином, а потом — с тетрациклином.
Плазмидные базы данных
За те несколько десятилетий, что существует методика молекулярного клонирования, были синтезированы тысячи разнообразных плазмид, из которых созданы базы данных (например, AddGene). В этих базах есть плазмиды на все случаи жизни — с разными типами точек начала репликации, разными полилинкерами, разными селективными маркерами и промоторами и так далее. Есть те, в которые можно вшить не одну вставку, а несколько, а есть даже такие, которые уже несут в себе некоторые особенно популярные вставки. Поэтому, как правило, исследователи не синтезируют плазмиду для клонирования самостоятельно, а покупают уже готовую. При необходимости купленную плазмиду можно «довести до ума», вставив или убрав определенные участки (а потом эту модифицированную плазмиду тоже добавить в базу данных). Иными словами, часто задача ученого сводится просто к тому, чтобы подобрать подходящую плазмиду.
Другие векторы
Плазмида — прекрасный вектор для относительно небольших вставок. Если ген-вставка слишком велик, то плазмида утрачивает стабильность, потому что ее участки начинают «перетасовываться» друг с другом и теряться при репликации, из-за чего она постепенно укорачивается. Поэтому в качестве вектора для длинных вставок используются более устойчивые конструкции. Например:
- Космида — гибрид плазмиды и фага (вируса, который заражает бактерии). По сути дела, это просто плазмида, в которую добавлены сайты для связывания с белками оболочки фага (они называются cos-сайтами, и именно благодаря им космиды получили свое название). Белковая оболочка делает космиду стабильнее, благодаря чему в нее можно загружать более длинные вставки;
- Искусственные хромосомы (человеческие, бактериальные, дрожжевые) — это сложные и крупные конструкции, являющиеся по сути микрохромосомами. Они относительно стабильны и при этом обладают гигантской емкостью: в них можно вставлять сразу несколько генов. Однако из-за огромных размеров их гораздо труднее засунуть в клетку;
- И, наконец, есть еще один вид векторов — вирусные. Этот вид настолько важен, что ниже ему будет посвящен целый раздел.
Вставляем ген в плазмиду
Допустим, исследователь подобрал подходящую плазмиду и получил нужную вставку. Теперь нужно соединить одно с другим, чтобы затем засунуть в клетки. Для этого достаточно совершить несколько простых действий.
Как уже говорилось, в плазмиде существует несколько сайтов рестрикции — то есть, участков, в которых ее может разрезать нужная рестриктаза. Нам нужно выбрать подходящий сайт, который будет находиться в том месте, куда мы собираемся вшивать вставку, а затем обработать плазмиду соответствующей рестриктазой.
После этого той же рестриктазой нужно обработать вставку, поскольку рестриктазы обычно оставляют выступающие концы на одной из нитей ДНК, и эти концы должны быть совместимы у вставки и плазмиды, чтобы они согласились соединиться. Если на кончиках вставки нет нужных сайтов рестрикции, то можно приделать к нему короткие ДНК-фрагменты с нужными сайтами рестрикции на концах.
И наконец, нам нужно соединить в одной пробирке плазмиду и вставку (предварительно очищенные от рестриктаз) и добавить к ним ДНК-лигазу, которая умеет лигировать (то есть, сшивать воедино) две молекулы ДНК. Конечно, в результате мы получим не только желанный вектор, в котором плазмида соединена со вставкой (назовем его чеширским котом с улыбкой), но и целый коктейль побочных продуктов — пустую плазмиду (кота без улыбки), замкнутую вставку (улыбку без кота), несколько сшитых между собой вставок (много улыбок) и так далее. В ходе селекции эти ненужные продукты отсеются, и у нас в руках останется только вектор.
Выделяем вектор
Итак, вначале мы проводим селекцию.
- Увеличиваем компетентность бактерий, добавляем к ним «коктейль», полученный в результате лигирования, а потом высеваем эти бактерии на среду с антибиотиком, который является нашим первым селективным маркером;
- Выбираем те бактериальные клоны, которые растут на среде с антибиотиком — они смогли съесть плазмиду со вставкой или хотя бы просто плазмиду (кота — с улыбкой или без);
- Проводим с этими клонами второй этап селекции, в зависимости от того, какой ген мы использовали в качестве второго селективного маркера. Например, если этот ген — устойчивость к другому антибиотику, то мы переносим бактерии на среду с этим антибиотиком и выбираем те клоны, рост которых угнетается, — они ухитрились проглотить не просто плазмиду, а плазмиду, в которую была вшита вставка (кота с улыбкой);
- Выращиваем полученную культуру бактерий.
И вот мы получили ее — бактериальную культуру, в которой живет созданный нами вектор. Вполне возможно, что это и было нашей конечной целью, и теперь мы, спокойные и счастливые, можем, например, включить в бактериях экспрессию гена-вставки и пожинать урожай синтезированных в результате белков.
Но если нам нужен чистый вектор, который можно будет потом засовывать в другие клетки, то у нас появляется проблема, которая кажется неразрешимой. Как вызволить вектор из бактерий? Ведь даже если мы выделим из этих бактерий ДНК, то помимо вектора получим еще и совершенно ненужную нам бактериальную хромосому.
Тут можно воспользоваться тем, что плазмидная ДНК имеет важные отличия от хромосомной: она, во-первых, гораздо меньше по размеру, а во-вторых, гораздо больше суперскручена. Поэтому можно подобрать такие условия, в которых бактериальные хромосомы будут осаждаться, в то время как плазмиды останутся плавать в растворе. Достаточно будет отцентрифугировать получившийся осадок (чтобы вся бактериальная ДНК прочно «упала на дно»), а затем уже из надосадочной жидкости выделить нашу плазмиду (обычно для этого используются специальные колонки, которые очень облегчают и ускоряют работу).
Как засунуть вектор в клетки
И вот наступил желанный миг. Исследователь держит в руке пробирку, в которой плещется прозрачная жидкость — столькими трудами полученный вектор. И тут перед ним встает преграда. Клетки, в которые он собирается засунуть свой вектор, отказываются его глотать.
Дело в том, что липидная мембрана, которой окружены клетки, обладает избирательной проницаемостью — то есть, она пропускает через себя одни частицы и не пропускает другие. Крупные заряженные молекулы (а именно таковой и является ДНК) через эту мембрану самопроизвольно пройти не могут. И если бактерии, например, умеют проглатывать плазмиды из внешней среды (как уже было сказано выше), то, скажем, клетки животных к этому совершенно не склонны. Поэтому для того, чтобы засунуть в клетку вектор, исследователю приходится прибегать ко множеству хитростей, о которых и будет сейчас рассказано. Но сначала — немного терминов.
Для внесения в клетку вектора есть несколько обозначений в зависимости от того, какой используется вектор и в какие клетки он вносится.
- Трансформация (о которой уже было немного рассказано) — это внесение плазмид (и других невирусных векторов) в бактерии, а также клетки растений и грибов;
- Трансфекция — то же самое, что и трансформация, но только в применении к клеткам животных;
- И, наконец, трансдукция — это внесение в любые клетки вирусного вектора.
Эти термины, в общем, не очень строгие. Например, даже в некоторых солидных статьях трансдукцию иногда называют вирусной трансфекцией (а то и просто трансфекцией).
Вещества-проводники
Самый простой и очевидный путь внесения в клетку генетического материала — соединить вектор с каким-нибудь переносчиком, у которого нет проблем с проникновением через мембрану, и позволить получившемуся комплексу пролезть внутрь клетки. Это не отнимает много времени и не требует дорогостоящего оборудования. Такой способ обычно называют химической трансфекцией. В этом случае события развиваются по следующему сценарию:
- Вектор соединяется с переносчиком;
- Получившийся комплекс проглатывается клеткой и оказывается в цитоплазме;
- В цитоплазме комплекс разваливается и вектор высвобождается;
- Вектор проникает в ядро и выполняет свое предназначение (скажем, с него начинает транскрибироваться мРНК).
К сожалению, почти на каждом из этих этапов возникают трудности. Во-первых, клетки захватывают далеко не все плавающие вокруг них комплексы. Во-вторых, не факт, что, оказавшись внутри клетки, вектор отделится от переносчика — вполне возможно, что они так и будут в обнимку плавать в цитоплазме, пока не подвергнутся деградации. В-третьих, даже если какой-то редкий комплекс умудрился проникнуть в клетку и там развалиться, это означает, что помимо вектора в клетке оказывается еще и переносчик, который может быть токсичен, вызывать побочные эффекты и вообще «замыливать» результаты экспериментов. И, наконец, в-четвертых, только небольшая часть вектора, оказавшегося внутри клетки, сможет проникнуть в ядро. Иными словами, комплексы вектора с переносчиком надо добавлять к клеткам в огромном избытке, чтобы хотя бы маленькая часть из них выполнила свое предназначение.
Утешает то, что среди производителей веществ-переносчиков огромная конкуренция, и поэтому на рынке постоянно появляются новые составы с улучшенными свойствами, которые минимизируют вышеописанные трудности. У каждого из составов есть какая-то своя «фишка», которая дает ему преимущество в конкурентной борьбе — некоторые образуют с вектором такие компактные комплексы, которым гораздо легче пробраться внутрь клетки; другие эффективнее отделяются от вектора, оказавшись в цитоплазме; третьи более универсальны и работают на огромном количестве типов клеток; четвертые, наоборот, славятся своей избирательностью и проникают только в те клетки, которые, например, экспрессируют какой-то специфический рецептор. Одним словом, если исследователь решил засунуть вектор внутрь клетки с помощью химической трансфекции, то ему просто надо выбрать из множества составов, представленных на рынке, тот, который будет лучше работать в данном конкретном случае.
Дырки в мембране
Но некоторые клетки так привередливы и капризны, что в принципе не соглашаются глотать комплексы ДНК с переносчиком (таким скверным характером славятся, например, первичные клетки — то есть, те, которые не выращивались в культуре, а были получены непосредственно от живого организма). Чтобы ввести в эти клетки генетический материал, ученому приходится прибегать к грубой силе — продырявливать мембрану и засовывать ДНК в образовавшиеся отверстия. Этот жестокий подход называется физической трансфекцией; он очень травматичен для клеток, и только некоторые из них переживут столь неделикатное обращение. Поэтому применять данную методику стоит, только если вы точно уверены, что обладаете достаточным количеством клеток и можете пожертвовать бóльшей частью из них. Ну и к тому же, вам потребуется довольно дорогое оборудование.
Наверное, самый распространенный способ продырявливания мембраны называется электропорацией. Дело в том, что у клеток, попавших в электрическое поле, в мембране возникают отверстия (которые получаются тем больше, чем сильнее приложенное к клеткам поле). Если эти отверстия малы, то клетка сможет «залечить» их; если же они слишком велики, то клетка погибнет из-за необратимого нарушения целостности мембраны. Поэтому эмпирическим путем можно подобрать оптимальную величину поля для того, чтобы клетки, с одной стороны, продырявились, а с другой — остались в живых. А когда клетки продырявлены, то добавленный к ним вектор проникает сквозь отверстия и оказывается в цитоплазме.
Кроме электропорации, есть еще несколько способов — экзотических и не очень — сделать в мембране дырки. Например, с помощью:
- Ультразвука (это называется сонопорация);
- Лазера (оптическая трансфекция);
- Нанопроволоки с пришитым к ней вектором, которая физически прокалывает мембрану (импалефекция);
- Магнитных взаимодействий (магнитофекция или магнитная трансфекция). В этом случае вектор присоединяется к магнитным наночастицам, которые транспортируются внутрь клетки с помощью магнитного поля.
Ну и наконец, для самых непокорных клеток, которые не поддаются никакой из вышеописанных методик, существует прибор под названием «генная пушка». Генная пушка расстреливает упрямые клетки частичками металла (обычно используется золото) с присоединенным к ним вектором. (Источником вдохновения для изобретателей этого прибора послужил пневматический молоток.) Генная пушка подходит практически для всех типов клеток, включая растительные, окруженные твердой клеточной стенкой, которая является практически непреодолимой преградой для большинства других методик.
А вообще, почти все вышеописанные методики дают более-менее похожие результаты на большей части типов клеток, а приборы для них стоят дорого. Поэтому, как правило, лаборатория покупает прибор для какой-то одной методики, и дальше уже по этой методике и доставляет генетический материал в клетки.
Овечки в волчьей шкуре
Зачем придумывать новые и трудные пути засовывания в клетку нуклеиновых кислот, если можно воспользоваться теми элегантными способами, которые за время долгой эволюции изобрели существа (или, возможно, вещества; нельзя точно сказать, живые они или нет), для которых транспортировка своего генетического материала внутрь клетки является необходимой фазой жизненного цикла? Все, наверное, уже догадались, что речь идет о вирусах.
Вирусы — это молекулы ДНК или РНК, упакованные в белковую оболочку (а иногда завернутые в липидный слой со встроенными в него вирусными белками). Именно оболочка играет главную роль в проникновении вируса через клеточную мембрану. Поэтому если засунуть в эту оболочку невирусную нуклеиновую кислоту, то она, будто вирус, тоже сможет попасть в клетку — как овечка, одетая в волчью шкуру. На этом принципе и основано использование вирусных векторов. Пожалуй, вирус — это самое эффективное транспортное средство для доставки в клетку генетического материала. Но приготовление вирусных векторов очень хлопотно, долго и трудоемко. Да вы сейчас и сами увидите.
Итак, чтобы сделать вирусный вектор, нужно для начала подобрать подходящий вирус. Идеальный кандидат:
- Стабилен — то есть, не склонен к спонтанным геномным перестройкам;
- Ёмок — то есть, может вместить в себя даже самую большую вставку;
- Не влияет на жизнедеятельность клетки;
- Не вызывает иммунного ответа;
- Встраивает свой геном не в первое попавшееся место генома хозяина (это может привести к непредсказуемым последствиям и вообще «замылить» результаты экспериментов), а в какую-нибудь определенную точку (а еще лучше — в точку, заданную самим исследователем);
- И обладает другими симпатичными чертами.
К сожалению, идеал недостижим, и ученым приходится выбирать из того, что есть. А именно:
Ретро
Ретровирусы долгое время были самой популярной основой для векторов. Это РНК-содержащие вирусы, которые, оказавшись в клетке, синтезируют ДНК на основе своей РНК с помощью ревертазы (собственно, поэтому они и называются «ретро», ведь синтез ДНК на основе РНК — это, в каком-то смысле, шаг назад). Ретровекторы хорошо выполняют свое предназначение, то есть, стабильно доставляют в клетку заключенный в них генетический материал, но у них есть несколько недостатков, из-за которых работать с ними неудобно.
Во-первых, они все (за одним исключением, о котором скоро будет рассказано) способны инфицировать только делящиеся клетки. Поэтому если исследователь, например, собрался изучать нейроны, которые не склонны к делению, ему надо забыть о ретровекторах и начать искать что-нибудь другое.
Во-вторых, ретровирусы встраиваются в самые непредсказуемые участки генома, каждый раз разные, и это приводит к самым непредсказуемым последствиям. Для начала, из-за этого нарушается воспроизводимость экспериментов — но это еще ладно. Беда в том, что ретровектор может вклиниться в середину какого-нибудь важного гена, из-за чего этот ген выключится, а в клетке начнутся патологические изменения, которые могут довести ее до гибели. Или, наоборот, ретровектор может случайно включить какой-нибудь совершенно ненужный ген, например, онкоген, что также приведет к очень печальным результатам (особенно если исследования проводятся не на культуре клеток, а на живом организме, и особенно если этот организм — человеческий).
Эти недостатки отвратили сердца ученых от ретровекторов и заставили их искать что-нибудь более подходящее. И найти кое-что замечательное удалось прямо внутри ретровирусного семейства.
Ленти
Лентивирусы — это род ретровирусов, который отличается от прочих представителей своего семейства некоторыми приятными с точки зрения молекулярного клонирования чертами.
Прежде всего, лентивирусы умеют заражать не только делящиеся, но и неделящиеся клетки. Эта особенность ужасна с точки зрения врача, который лечит вызванное лентивирусом заболевание, и прекрасна с точки зрения молекулярного биолога, который делает на основе лентивируса лентивектор. Ведь работая с таким вектором, ученый сможет использовать гораздо более широкий ассортимент клеточных типов, а значит, сделать гораздо больше великих открытий.
Плюс к тому, лентивекторы довольно емкие, то есть, они способны вместить в себя крупные вставки. Отчасти это связано с тем, что из их генома в целях безопасности выкидывается бóльшая часть, и в результате освобождается куча места. Ну и кроме того, лентивирусы встраиваются в чуть менее непредсказуемые участки генома, чем прочие ретровирусы, а это тоже очень здорово.
«Ленти» по латыни значит «медленный». Это слово очень точно отражает характер лентивирусов — они вызывают заболевания с необычайно длинным инкубационным периодом. Вирус СПИДа — это тоже, кстати, лентивирус.
Адено
Аденовирусы, наряду с ретровирусами, долго были самой популярной основой для векторов, но теперь потихоньку сдают свои позиции. Аденовирусы способны заражать не только делящиеся, но и неделящиеся клетки; ассортимент клеточных типов, которые они заражают, довольно широк. Но они не встраиваются в хозяйский геном, и поэтому подходят не для всех экспериментов. Кроме того, аденовирусы часто вызывают сильный иммунный ответ. Поэтому все чаще они используются не в базовых исследованиях, а для всяких прикладных целей — например, для создания вакцин.
И наконец, относительно недавно на сцене появился новый персонаж, который сразу расположил к себе ученых множеством чудесных качеств. Зовут его аденоассоциированный вирус (AAV).
AAV ведет себя настолько тихо, скромно и ненавязчиво, насколько этого вообще можно ждать от вируса. Практически единственное, что он делает, оказавшись в клетке, — это встраивается в хозяйский геном, причем почти всегда не в первое попавшееся, а в строго определенное место. Он, судя по имеющимся сейчас данным, не вызывает никаких заболеваний, поэтому и иммунный ответ на него очень слабый. К тому же, он способен заражать и делящиеся, и неделящиеся клетки. Одним словом, AAV — просто идеальная основа для вектора, хотя и он не лишен некоторых недостатков. И главный его недостаток — малая емкость. В AAV-вектор могут влезть только совсем небольшие вставки, и в этом он очень проигрывает, например, лентивекторам.
Кроме того, AAV — дефективный, несамостоятельный вирус. Он может размножаться только в клетках, которые уже заражены аденовирусом (что и отражено в его названии). Это совсем неплохая черта, если мы хотим заразить нашим вектором культуру клеток; но если мы собираемся делать вектор для генной терапии (методики лечения генетических (и не только) заболеваний, при которой организм заражается вирусным вектором, несущим необходимые этому организму гены), то такая дефективность будет нам очень мешать, потому что вирусы не смогут как следует распространяться по организму. Однако сейчас эта проблема решена, и разработаны AAV-векторы, которые способны размножаться сами по себе, безо всякой помощи.
Но вот подходящий вирус подобран. Теперь начинаются игры с его геномом.
- Вначале нам нужно освободить в этом геноме место — то есть, выкинуть из него какие-то гены. Обязательно нужно оставить те участки, на которые налипает оболочка (чтобы наш вектор был полноценным, «одетым» вирусом), и те гены, которые обеспечивают встраивание вирусного генома в геном хозяйской клетки (чтобы он мог выполнить свое предназначение); при этом от других областей — например, генов белков оболочки — мы можем с чистой совестью избавиться;
- Из получившегося «огрызка» генома делается плазмида — вставляются фрагменты, о которых уже было рассказано выше (точки начала репликации, селективные маркеры и так далее). В принципе, такие плазмиды уже есть в плазмидных базах данных, и, как правило, задача исследователя сводится к тому, чтобы подобрать подходящую;
- В эту плазмиду вшивается необходимая вставка (со всеми прелестями многоэтапной селекции, которые были описаны выше).
Теперь у нас возникает небольшая проблема. Даже засунув эту плазмиду в клетку, никаких вирусов мы не получим, потому что мы уже выкинули (в пункте 1) те гены, которые нужны для их создания. Поэтому нам придется пойти на маленькую хитрость.
Мы засунем в клетки не одну плазмиду, а две. Первая, основная (назовем ее Пу), — это та, которую мы получили в пункте 3. А вторая, вспомогательная (назовем ее Ме), будет нести гены, которые мы выкинули в пункте 1. Обе плазмиды начнут размножаться в хозяйской клетке. Плазмида Ме будет экспрессировать свои белки — например, белки оболочки и белки, необходимые для самосборки вирусов. Поскольку на Пу есть участки для налипания белков оболочки, то эти белки на нее и налипнут, и в результате мы получим вирус с необходимыми генами внутри, чего мы и добивались.
Итак, наш план действий таков:
- Подбираем какие-нибудь клетки, которые хорошо поддаются трансфекции (такая линия клеток называется «упаковывающей»; обычно это линия эмбриональных клеток человеческой почки НЕК293) и засовываем в них сразу две плазмиды — Пу и Ме, основную и вспомогательную;
- Ждем некоторое время (около двух дней), чтобы успели образоваться вирусы. После этого собираем среду, в которой живут клетки, — вирусы плавают в ней;
- Очищаем полученные вирусы (как правило, для этого используется центрифугирование и фильтрация) и.
- Используем их по назначению, то есть, заражаем ту линию клеток, на которой собираемся проводить эксперименты.
Это, конечно, только общая схема, у каждого конкретного вектора есть свои нюансы. Например, бывает, что вместо одной вспомогательной плазмиды используют две или даже три. При создании некоторых AAV-векторов упаковывающие клетки нужно заразить аденовирусом. А если мы создаем вектор для генной терапии, который должен уметь размножаться в хозяйской клетке и заражать ее соседей, то нам придется гораздо аккуратнее обращаться с вирусным геномом и расчищать в нем место с большой осторожностью, чтобы не нарушить способность вирусов к самостоятельному размножению. И так далее.
Последний шаг
Итак — ура! — тем или иным способом мы все-таки умудрились засунуть вектор в клетки. Нам остается последний шаг — нужно выбрать из всех клеток те, которые встроили векторную ДНК в свой геном.
Собственно, для этого мы и добавили в вектор последний селективный маркер — ген устойчивости к антибиотику, работающему на эукариотических клетках. Мы просто будем постоянно добавлять этот антибиотик в среду, в которой находятся наши клетки, — в результате останутся в живых и смогут делиться только те, которые имеют в геноме этот ген и всю нашу векторную ДНК впридачу.
Все! Клонирование завершено. Мы получили линию генетически модифицированных клеток, в геноме которых присутствует наша вставка. Пришло время проводить с этими клетками необходимые эксперименты.
Источник