Почвы азотфиксации у растений
Фиксация азота
Одной из важнейших задач биохимиков, заинтересованных в увеличении продуктивности сельского хозяйства, является повышение эффективности азотфиксации, так как рост растений чаще всего лимитирует недостаточное снабжение их фиксированным азотом. Азот в форме стабильной молекулы N2 составляет 80% атмосферы. Перед фиксацией (восстановлением азота до аммиака) эта молекула должна каким-то образом дестабилизироваться и расщепиться. Образующийся при фиксации аммиак (NH3) может поглощаться корнями растений как таковой или после его окисления почвенными микроорганизмами до нитратов (NO3 — ). В большинстве почв образование NO3 — из NH3 происходит настолько быстро, что большая часть азота поглощается корнями в виде NO3 — .
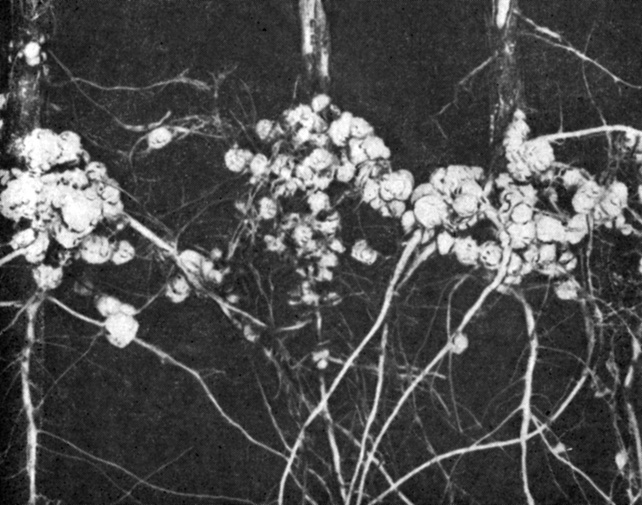
Фиксация азота осуществляется главным образом некоторыми свободно живущими бактериями, потребляющими органическое вещество почвы. К ним относятся, например, аэробная форма Azoiobacter и анаэробная — Clostridium. Бактерии рода Rhizobium, которые тоже участвуют в фиксации азота, живут в корневых опухолях или клубеньках определенных видов растений (рис. 7.3). Растение-хозяин принадлежит обычно к семейству бобовых, включающему горох, бобы, сою, люцерну* клевер и вику. Недавно проведенные исследования показали, что азотфиксирующие бактерии рода Spirillum окружают корни тропической травы Digitaria. Эта слабая ассоциация корней травы и бактерий в ризосфере, возможно, представляет промежуточную эволюционную стадию между свободноживущим азотобактером и локализованным в клубеньках ризобиумом. Растение «привлекает» бактерии с помощью органических корневых выделений. Микроорганизмы ризосферы в свою очередь снабжают растения фиксированным азотом. Некоторые сине-зеленые водоросли (такие, как Anabaena и Nostoc) и фотосинтезирующие бактерии (Rhodospirillum) могут фиксировать атмосферный азот, энергетически сопрягая этот процесс с фотосинтезом. Указанные организмы являются наиболее выраженными автотрофами биологического мира, хотя некоторые штаммы Anabaena живут и эффективно фиксируют азот лишь в ассоциации с особыми «карманчиками» водяного папоротника Azolla. Причины этого явления не выяснены.
Рис. 7.3. Клубеньки на корнях сои. (С любезного разрешения компании по производству нитрагина.)
Взаимовыгодная ассоциация двух организмов называется симбиозом. Так как ни Rhizobium, ни растение-хозяин в отдельности не способны фиксировать и восстанавливать атмосферный азот, биологический комплекс в клубеньке нужно рассматривать как симбиотическую ассоциацию бактерий и растения-хозяина. Каждый тип растения-хозяина имеет свой собственный симбиотический Rhizobium. Взаимное узнавание растения-хозяина и бактерий осуществляется путем прикрепления особого белка (лектина), находящегося на поверхности клеток корневого волоска, к специфической бактерии. После прикрепления к хозяину вторгающийся организм проникает в клетки необычно искривленных корневых волосков, которые, очевидно, деформируются под влиянием выделяемых бактериями ростовых гормонов группы ауксина (см. гл. 9). Внутри клетки-хозяина бактерии делятся, и образовавшееся потомство изменяет свою форму превращаясь в бактероиды, содержащиеся в инфекционной нити, которая проходит от верхушки клеточной стенки корневого волоска через центр клетки (рис. 7.4). Окончательным результатом такого проникновения бактерий является чрезвычайно сильное разрастание клеток корня, приводящее к образованию бородавчатых выпуклостей, называемых клубеньками. Ризобиум способен эффективно фиксировать азот, лишь находясь в клубеньках такого типа.
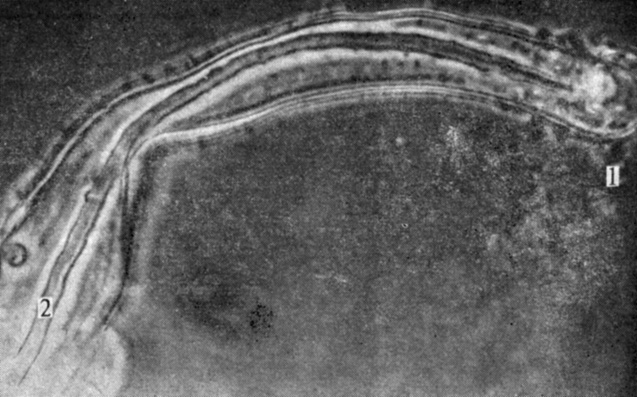
Рис. 7.4. Заражение белого клевера бактериями Rhizobium trifolii происходит через клетки корневых волосков. Обратите внимание на значительное накопление клеток ризобиума (1) на кончике корневого волоска и преломляющую свет инфекционную нить (2) внутри корневого волоска. Отдельные бактериальные клетки своими концами прикреплены к продольным сторонам клеточной стенки корневого волоска. (С любезного разрешения F. B. Dazzo, Michigan State University.)
Ассоциация между Spirillum и его растением-хозяином тоже относится к симбиотической, но она ограничена поверхностью корней. Это менее прочный тип ассоциации, так как Spirillum можно выращивать отдельно от хозяина при наличии достаточного количества питательных веществ. Поэтому ученые изучают возможность крупномасштабного культивирования этих бактерий в качестве источников фиксированного азота. Было также показано, что иногда данные бактерии живут в ассоциации с кукурузой. Это открывает возможность выведения штаммов, способных к фиксации азота на тех видах растений, которые обычно не имеют азотфиксирующих бактерий.
Фиксация азота осуществляется Fe 2+ — и Mo — -содержащим ферментом нитрогеназой. Растения, живущие в ассоциации с азотфиксирующими бактериями и зависящие от этого фермента, не реагируют на добавление азотсодержащих удобрений, так как аммиак (NH3), присутствующий в них или образованный из внесенного азотсодержащего материала, подавляет активность генов, управляющих синтезом нитрогеназы. Поэтому попытки повысить уровень азотфиксации включают поиски азотфиксирующих бактерий, лишенных способности регулировать синтез нитрогеназы по принципу «обратной связи». В регулируемый механизм, очевидно, вовлечен фермент глутаминсинтетаза, поскольку синтез нитрогеназы происходит лишь при высоком содержании глутаминсинтетазы. Недавно были найдены мутантные бактерии, содержащие большое количество глутаминсинтетазы. Они продолжают синтезировать нитрогеназу даже в присутствии NH3. Таким образом, поиск бактерий с высокой эффективностью азотфиксации кажется многообещающим.
Кроме нитрогеназы, которая связывается с молекулой N2 и дестабилизирует ее, для восстановления N2 до NH3 необходимы сильный восстановитель и АТР. Ферредоксин — переносчик электронов, участвующий также и в фотосинтезе, — служит главным восстанавливающим агентом. При симбиотической азотфиксации АТР поставляется растением-хозяином и количество фиксированного азота часто ограничивается скоростью фотосинтеза. Поэтому «удобряя» растение, например сою, двуокисью углерода, в принципе можно повысить общую фиксацию азота благодаря увеличению количества метаболитов, образующихся при фотосинтезе. Однако это трудно осуществить на практике при возделывании полевых культур.
Все азотфиксирующие системы можно отравить даже следовыми количествами кислорода. Это означает, что фермент нитро- геназа даже в аэробных клетках должен содержаться в основном в анаэробных условиях. В корневых клубеньках бобовых это достигается с помощью леггемоглобина (LHb) — красноватого железосодержащего аналога животного пигмента. Подобно гемоглобину крови и миоглобину мышц, леггемоглобин может связываться с кислородом:
Такое связывание обеспечивает эффективное удаление кислорода, находящегося поблизости от нитрогеназы, и оптимальные скорости азотфиксации. Кислород, связанный с леггемоглобином, может быть также использован для образования АТР в процессе дыхания. Это имеет очень большое значение, так как для фиксации азота необходимы значительные количества АТР. Как правило, чем краснее клубенек, тем активнее в нем идут процессы азотфиксации. В азотфиксирующей сине-зеленой водоросли Nostoc нитрогеназа. очевидно, локализована в гетероцистах, специальных нефотосинтезирующих анаэробных клетках (рис. 7.5). Эта структурная организация служит также для изоляции азотфиксирующей системы от кислорода, выделяющегося в процессе фотосинтеза.
Некоторые микроорганизмы, обитающие в почве, могут окислять аммиак (NH3) до нитратов (NO3 — ). Большинство растений предпочитают поглощать и использовать азот, внесенный в виде нитрата, хотя такой азот в итоге включается в растительный материал в форме высоковосстановленных аминогрупп (-NH2). Фермент нитратредуктаза восстанавливает нитраты обратно до аммония с помощью восстановленных дыхательных переносчиков, таких, KaKNADPH. Нитратредуктаза, вероятно, содержит молибден в своем активном центре, и это, возможно, является главной метаболической ролью молибдена в растениях. Восстановление NO3 — до NH3 может, очевидно, происходить через такие промежуточные соединения, как азотистая кислота (HONO) и гидроксиламин NH2OH).
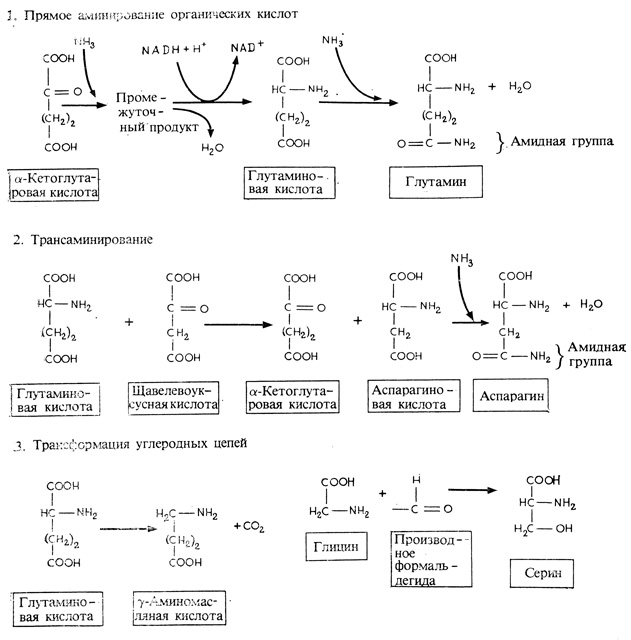
Аммиак токсичен для растительных клеток, поэтому он не должен накапливаться в них в больших количествах. Аммиак обычно превращается в аминокислоты, вступая в реакцию α-кетоглутаровой кислотой (метаболит цикла Кребса), в результате чего образуется глутаминовая кислота, а при дальнейшем добавлении аммиака — глутамин, амид глутаминовой кислоты (рис. 7.6). Другие аминокислоты синтезируются в ходе ферментативного процесса переаминирования, при котором глутаминовая кислота взаимодействует с другими кетокислотами, предшественниками новых аминокислот, перенося на них свою аминогруппу и превращаясь вновь в α-кетоглутаровую кислоту. Аспарагиновая кислота является одним из первых продуктов реакции переаминирования. В этом случае рецептором аминогруппы служит щавелевоуксусная кислота. При дополнительном связывании аммиака с аспарагиновой кислотой образуется аспарагин — амид аспарагиновой кислоты. Преимущественно в форме этих четырех компонентов — глутаминовой кислоты, глутамина, аспарагиновой кислоты и аспарагина — и транспортируется фиксированный азот от клеток корня по всему растению * . Некоторые аминокислоты образуются путем модификации углеродного остова пред существующей аминокислоты.
* ( В клубеньковых растениях из сем. бобовых главной формой органического азота, двигающегося вверх по ксилеме, являются замещенные производные мочевины (урейды).)
Рис. 7.6. Три способа образования аминокислот
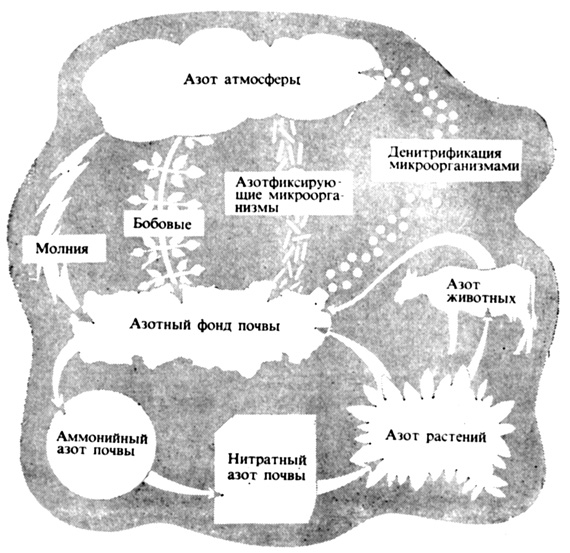
Таким образом, общий круговорот азота в природе представляет собой обратимый переход его свободной газообразной формы в атмосфере в фиксированную форму в почве или биологической системе. В растительных клетках поглощенные нитраты вновь восстанавливаются до аммиака, который затем связывается с определенными органическими кислотами, в результате чего образуются аминокислоты, а затем белки. Эти вещества перевариваются животными и превращаются в животные белки и азотистые продукты обмена — мочевину и мочевую кислоту. В конечном счете все животные и растения отмирают и разлагаются в почве с образованием простых азотистых веществ, таких, как аммиак. Эти вещества постоянно рециркулируют через биологические системы, создавая круговорот азота (рис. 7.7). Благодаря действию денитрифицирующих бактерий фиксированный азот в виде свободного молекулярного азота возвращается в атмосферу, откуда он опять может фиксироваться бактериями. Денитрификация — довольно расточительный процесс.. Его можно теперь замедлить ,в почве с помощью химических соединений, специально предназначенных для этой цели. Их применение должно оказать существенную помощь сельскому хозяйству.
Рис. 7.7. Круговорот азота. Азот почвы, живых существ и атмосферы находится в состоянии постоянного круговорота
Фермент нитрогеназа, который связывается с молекулой N2 (N=N) и восстанавливает ее до аммиака (NH3), может также присоединять ацетилен (HC=CH) и восстанавливать его до этилена (HC=CH). Обнаружение этой активности лежит в основе метода, с помощью которого азотфиксирующую активность растения можно определить непосредственно в поле. Определенное количество ацетилена в виде газа вносится в корнеобитаемую среду растения и через некоторое время удаляется. Количество ацетилена, превращенное в этилен, служит показателем азотфиксирующей способности корней данного растения. Поскольку как ацетилен, так и этилен являются газами, даже незначительные их количества можно анализировать методом газовой хроматографии, позволяющим без больших затрат быстро получать точные данные. Используя этот метод, физиологи растений исследовали азотфиксирующую способность растений сои в онтогенезе и изучили физиологические факторы, влияющие на эффективность процесса. Это важно для выявления путей дальнейшего повышения продуктивности растений.
Источник
Сельское хозяйство | UniversityAgro.ru
Агрономия, земледелие, сельское хозяйство
Home » Агрохимия » Азот в жизни растений
Популярные статьи
Азот в жизни растений
Азот — химический элемент, инертный газ без цвета и запаха, открыт французским химиком Лавуазье во второй половине XVIII в., является основным компонентом атмосферного воздуха (78,08%). Название означает «нежизненный», так как не поддерживающий горение и дыхание. Однако, дальнейшие исследования показали огромную роль азота в жизни растений и всего органического мира.
Азот входит в состав:
- белков, пептидов и аминокислот, которые являются составной частью протоплазмы и ядра растительных клеток;
- нуклеиновых кислот (ДНК и РНК) — носителей наследственных свойств живых организмов и участвующих в обмене веществ;
- молекул хлорофилла;
- ферментов;
- фосфатидов;
- гормонов;
- большинство витаминов.
Азотное питание растений
Все ферменты — белковые вещества, поэтому при недостаточном снабжении растений азотом синтех ферментов замедляется, что приводит к нарушениям в процессах биосинтеза, обмена веществ, в итоге, к снижению урожая.
Регулирование азотного питания растений, можно влиять на урожайность сельскохозяйственных культур с учетом других факторов жизни. Максимальный урожай достигается при достаточном обеспечении растений всеми условиями их роста. Академик Д.Н. Прянишников писал, что вся история земледелия в Западной Европе говорит о том, что главным условием, определяющим среднюю высоту урожаев в разные эпохи, была степень обеспеченности сельскохозяйственных растений азотом.
Оптимальное азотное питание способствует синтезу белковых веществ, растения образуют мощные стебли и листья с интенсивной зеленой окраской. Мощный ассимиляционный аппарат позволяет накапливать большее количество продуктов фотосинтеза, повышая урожайность и, как правило, его качество.
Одностороннее избыточное питание азотом, особенно во второй половине вегетационного периода, приводит к задержке созревания растений; образуется большая вегетативная масса, урожай репродуктивных органов но не успевает сформироваться.
Недостаток азота приводит к сильному замедлению роста растений. Прежде всего сказывается на развитии вегетативной массы: листья становятся мелкими, светло-зелеными, раньше желтеют, стебли тонкие, слабо ветвятся. Снижается формирование репродуктивных органов, урожай резко снижается. Азотное голодание у злаковых культур приводит к ослаблению кущения, уменьшается количество зерен в колосе, снижается белковость зерна.
Содержание азота в растениях
По химическому составу, на долю азота в растениях приходится 0,5-5,0% воздушно-сухой массы, основное количество приходится на семенах. Содержание белка четко коррелирует с количеством азота в растениях. В вегетативных органах содержание азота ниже: в соломе бобовых 1,0-1,4%, в соломе злаковых 0,45-0,65%. Еще меньше азота накапливается в корне-, клубнеплодах и овощных культурах: картофель (клубни) 0,32%, сахарная свекла (корни) 0,24%, капуста 0,33% сырого вещества.
Содержание азота в растениях зависит от возраста, почвенно-климатических условий, питательного режима, в частности обеспеченности питательными элементами.
Таблица. Содержание белка и азота в семенах различных культур, % 1
| Культура | Белок | Азот |
|---|---|---|
| Соя | 29 | 5,8 |
| Горох | 20 | 4,5 |
| Пшеница | 14 | 2,5 |
| Рис | 7 | 1,2 |
Содержание азота в молодых вегетативных органах выше. По мере старения азотистые вещества мигрируют в появляющиеся листья и побеги.
Таблица. Содержание азота в вегетативной массе зерновых культур по фазам развития, % на воздушно-сухое вещество 2
| Культура | Фаза развития | |||
|---|---|---|---|---|
| кущение | трубкование | колошение | цветение | |
| Озимая пшеница | 5,0-5,4 | 3,0-4,5 | 2,1-2,5 | 2,0-2,4 |
| Яровая пшеница | 4,5-5,5 | 3,0-4,4 | 2,5-3,0 | 1,8-2,5 |
| Овес | 5,5-5,9 | 2,9-3,9 | 2,2 | 1,3-1,7 |
Поступление и трансформация азота в белковые вещества
Темпы накопления органических веществ растениями опережают поступление азота и других питательных веществ. Происходит «ростовое разбавление» содержания питательных элементов. При созревании отмечается выраженное передвижение азота в репродуктивные органы, где они накапливаются в виде запасных белков.
В основном азот поступает в растения в нитратной и аммонийно форме, но также способны усваивать некоторые растворимые органические соединения, например, мочевину, аминокислоты, аспарагин.
Из поступающих из почвы в растения соединений азота только аммиак непосредственно используется для синтеза аминокислот. Нитраты и нитриты включаются в синтез аминокислот только после восстановления в тканях растений.
Редукция нитратов до аммиака начинается уже в корнях с помощью флавиновых металлоферментов:
При избытке, часть нитратов поступает в неизменном видо в листья, где восстанавливается по той же схеме.
Образование аминокислот (аминирование) происходит в результате взаимодействия аммиака с кетокислотами: пировиноградной, щавелевоуксусной, кетоглутаровой и др., образующиеся в процессе окисления углеводов. Аминирование регулируется ферментами. Так, при взаимодействии пировиноградной кислоты с аммиаком образуется аланин:
Аналогично взаимодействие аммиака с щавелевоуксусной кислотой приводит к образованию аспарагиновой кислоты (СООН-СН2-СНNН2-СООН), с кетоглутаровой кислотой — глутаминовая кислота (СООН-СН2-СН2-СНNН2-СООН).
В аминокислоты азот входит в виде аминогруппы (—NH2). Процессы образования аминокислот происходит в корнях и в надземной части растений.
Опыты с использованием меченых атомов показывают, что уже через несколько минут после подкормки растений аммиачными удобрениями, в тканях могут обнаруживаться аминокислоты, синтезированные из внесенного в подкормку аммиака. При этом первой образующеся аминокислотой является аланин, затем аспарагиновая и глутаминовая кислоты.
Нитратный азот может накапливаться в растениях в больших количествах, без причинения им вреда. Аммиак в свободном виде в тканях содержится в незначительных количествах. Его накопление, особенно при недостатке углеводов, приводит к аммиачному отравлению растений.
Однако растения имеют способность связывать избыток свободного аммиака: его часть вступает во взаимодействие с синтезированными аспарагиновой и глутаминовой аминокислотами, образуя соответствующие амиды — аспарагин и глутамин:
Образование аспарагина и глутамина позволяет растениям защитить себя от аммиачного отравления и создать резерв аммиака, кроме того, амиды участвуют в синтезе белков.
В 1937 г. биохимиками А.Е. Браунштейном и М.Г. Крицманом была открыта реакция переаминирования, заключающаяся в переносе аминогруппы с аминокислоты на кетокислоту с образованием других амино- и кетокислот. Реакция катализируется ферментами трансаминазами или аминоферазами.
Так, присоединение к пировиноградной кислоте аминной группы от глутаминовой кислоты, приводит к образованию аланина и кетоглутаровой кислоты:
Благодаря переаминированию синтезируется значительное число аминокислот. В растениях наиболее легко переаминируются глутаминовая и аспарагиновая кислоты.
Аминокислоты являются составными частями полипептидов и белков. В построении белковых молекул участвуют 20 аминокислот, аспарагин и глутамин в различных соотношениях и пространственной ориентации, что обуславливает огромное разнообразие белков. В настоящее время известно более 90 аминокислот, около 70 из них присутствуют в растениях в свободном виде и не входят в состав белков.
Растения синтезируют аминокислоты, которые не могут образовываться в организме человека и высших животных, но являются незаменимыми для их жизни. К ним относятся: лизин, гистидин, фенилаланин, триптофан, валин, лейцин, изолейцин, треонин и метионин.
На долю небелкового органического азота в растениях приходится 20-26% от общего количества. В неблагоприятных условиях, например, при дефиците калия или недостаточном освещении, количество небелковых азотистых соединений возрастает.
В тканях растений белки находятся в динамичном равновесии с небелковыми азотистыми соединениями. Одновременно с синтезом белков и аминокислот протекает процесс их распада: отщепление аминогруппы от аминокислоты с образованием кетокислот и аммиака. Этот процес называется дезаминированием. Высвобождающаяся кетокислота используется растениями для синтеза углеводов, жиров и иных веществ; аммиак повторно вступает в реакцию аминирования других кетокислот, образуя новые аминокислоты, при его избытке — аспарагин и глутамин.
Таким образом, весь цикл превращений азотистых соединений в растениях начинается (аминирование) и заканчивается (дезаминирование) аммиаком.
«Аммиак есть альфа и омега в обмене азотистых веществ у растений».
За все время вегетации растения синтезируется большое количество белковых соединений, причем в разные периоды роста обмен азотистых веществ происходит по-разному.
При прорастании семян, клубней, луковиц наблюдается распад запасных белков. Продукты распада расходуются на синтез аминокислот, амидов и белков в тканях проростков до выхода их на поверхность почвы. В Затем, по мере формирования корневой системы и листового аппарата, синтез белков протекает за счет минерального азота, поглощаемого из почвы.
В молодых растениях преобладает синтез белков. В процессе старения растений начинает преобладать распад белков. Продукты распада из стареющих органов мигрируют в молодые, интенсивно растущие органы, где используются для синтеза новых белков в точках роста. По мере созревания растений и формирования репродуктивных органов, белковых веществ распадаются в вегетативных частей, продукты распада перемещаются в репродуктивные органы, где используются для образования запасных белков. К этому моменту поступление азота в растения из почвы существенно замедляется или полностью прекращается.
Особенности аммонийного и нитратного питания растений
В конце XIX в. в агрономической науке ведущую роль занимала теория нитратного питания растений, роль аммиака как источника минерального питания отрицалась.
Причинами этому послужили:
- опыты в водных культурах: отмечалось хорошее развитие растений на фоне нитратных солей, на фоне аммонийных солей развитие было плохим;
- открытие процесса нитрификации в почве; что стало основанием считать: при внесении в почву аммонийных удобрений они переходят в нитратную форму, которая усваивается растениями;
- внесение чилийской селитры (NaNO3) заметно повышало урожайность культур.
Однако в конце века П.С. Коссович в опытах со стерильными культурами показал, что растения могут также усваивать аммиачный азот без окисления в нитратную форму. К такому же выводы пришел и французский исследователь Мазе в 1900 г. После этого были изучены условия и особенности питания аммонийными и нитратными формами азота. Фундаментальные исследования по этому вопросу провел Д.Н. Прянишников. Он показал, что эффективность использования различных форм азота зависит от реакция среды: в нейтральной реакции лучше поглощается аммонийный азот, при кислой — нитратный.
В начальные фазы роста существенное значение имеют биологические особенности. При прорастании семян с небольшим запасом углеводов, например, у сахарной свеклы, а, следовательно, органических кетокислот, избыточное поступление аммония в растения оказывает негативное действие. Аммонийный азот не успевает использоваться для синтеза аминокислот, накапливается в тканях растения и вызывает их отравление. В данном случае используют нитратные формы азотных удобрений, так как они также накапливаться в тканях растений, но не причиняют вреда. Семена и посевной материал с большим запасом углеводов, например, картофель, используют аммонийный азот для синтеза аминокислот без ограничений. Поэтому для таких культур аммонийная и нитратная формы в начальные стадии роста равноценны.
На поглощение нитратного и аммонийного азота влияет обеспеченность другими элементами питания. Повышенное содержание в почве калия, кальция и магния способствует поглощению аммония. При нитратном питании значение имеет обеспеченность растений фосфором и молибденом. Дефицит молибдена приводит к задержке восстановления нитратов до аммиака и способствует накоплению нитратов в тканях растений.
Учитывая, что аммонийная форма азота при поступлении в растения может сразу использоваться для синтеза аминокислот, тогда как нитратная только после восстановления до аммиака, аммоний более энергетически экономной формой.
Источник