Показатель pH почвы (как определить кислотность почвы)
Большинство растений предпочитают слабокислые и нейтральные почвы. Но если грунт сильнокислый или щелочной, выращивать на нем даже неприхотливые растения сложно. Для определения кислой, нейтральной или щелочной среды почвы используют показатель pH.
Содержание
Показатель pH — специальный показатель, отражающий кислотно-щелочной баланс почвы. В этом материале даны понятия что такое показатель pH, какие типы почвы (от слабокислой до сильнощелочной) соответствуют численным значениям показателя рН, а также способы для его определения или измерения.
ЧТО такое показатель pH почвы
Кислотность показывает концентрацию ионов водорода, определяющих кислотно-щелочной баланс грунта. Для этого есть показатель pH. Показатель, отражающий кислотно-щелочной баланс почвы, раствора или другой среды. Измеряется в единицах от 0 до 14 (см таблицу):
| Значение показателя pH | Характеристика |
| 0 … 6,9 | среда кислая (преобладают кислоты) |
| 7,0 | среда нейтральная (кислоты и щелочи нейтрализуют друг друга). |
| 7,1 … 14 | среда щелочная (преобладают щелочи). |
| Примечание: а) чем больше pH: тем меньше кислотность почвы; тем больше щелочность почвы. б) чем меньше pH: тем больше кислотность почвы; тем меньше щелочность почвы. |
Показатель pH почвы (его численное значение) чаще всего колеблется в диапазоне 3,5-8,5.
Типы почвогрунтов, в зависимости от показателя pH принято разделять на следующие типы (см. таблицу):
| Значение показателя pH | Тип почвы |
| менее 4 | сильнокислая |
| 4 … 5 | среднекислая |
| 5 … 6 | слабокислая |
| 6 … 7 | нейтральная |
| 7 … 8 | слабощелочная |
| 8 … 8,5 | среднещелочная |
| более 8,5 | сильнощелочная |
Также принято различать два типа кислотности — актуальную кислотность (отражает реальное состояние, сколько сейчас в почве есть ионов водорода) и потенциальную кислотность (потенциально возможное состояние):
- АКТУАЛЬНАЯ определяет присутствие в почве ионов водорода: чем их больше, тем выше кислотность (соответственно, тем меньше значение pH).
- ПОТЕНЦИАЛЬНАЯ определяет присутствие в почве обменно поглощенных ионов водорода и других частиц – марганца, железа, алюминия.
Всем садоводам и огородникам следует ориентироваться ТОЛЬКО на актуальную кислотность, которая измеряется химическими индикаторами, приборами и другими способами. Далее рассмотрим как определить показатель pH почвы.
КАК определить показатель pH почвы (кислотность почвы)
Способов определения множество – это и «народные» (с использованием уксуса или лакмусовой бумаги), и современные (с применением электронных приборов pH-метров/ кислотомеров).
Самые распространенные способы определения кислотности почвы:
- Лакмусовой бумагой;
- Измерительные приборы pH-метры;
- Визуальный способ (по растениям-маркерам);
- С помощью уксуса;
- Заказ исследование почвы в лаборатории.
а) Лакмусовая бумага
Показатель pH почвы определяется по цвету бумаги. Лакмусовая бумага есть в продаже в любом садовом центре.

б) Измерение pH-метром (кислотомером)
Для определения кислотности разработаны и внедрены в производство целый ряд pH-метров (кислотомеров) – специальных портативных приборов, позволяющих определять не только кислотность, но и другие ключевые показатели почвы – влажность, температуру, освещённость и пр.
pH-метр — это прибор для измерения водородного показателя, характеризующего активность ионов водорода в растворах/средах (почва, вода, пищевая продукция и сырье, объекты производственных системах, в том числе в агрессивных средах). Действие pH-метра основано на измерении величины ЭДС электродной системы, которая пропорциональна активности ионов водорода в растворе — pH (водородному показателю).
Для использования в ЛПХ и в сельскохозяйственном производстве выпускается широкий ряд простых в применении электронных или электронно-механических pH-метров. Популярность их из года в год растет. Это самый точный и актуальный на сегодня способ определения кислотности почвы.

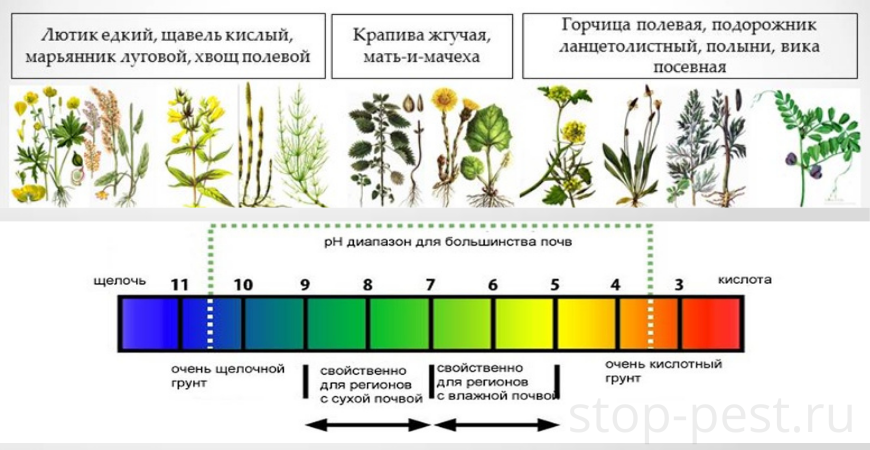
в) Визуальный способ
В данном случае речь идет по определению кислотности почвы по растениям – маркерам. Например, если на участке хорошо растет щавель и хвощ, то почва кислая, а если мак и вьюнок – щелочная.
| Значение pH | Тип почвы | Растения-маркеры |
| менее 4 | сильнокислая | растений нет, на верхнем слое бархатистый зеленый налет |
| 4 … 5 | среднекислая | подорожник, дикий щавель, мята дикая, хвощ, фиалка и др. |
| 5 … 6 | слабокислая | папоротник, ромашка, пырей, одуванчик, сныть обыкновенная, клевер, мать-и-мачеха и др. |
| 6 … 7 | нейтральная | мокрица, лебеда, пастушья сумка, |
| более 7 | щелочная | мак, вьюнок, дрема белая |
г) С помощью уксуса
В плоскую емкость помещается небольшое количество почвогрунта. Затем заливается 6% раствором уксуса. По реакции определяем кислотность почвы:
- реакции нет, то почва кислая;
- реакция слабая (мало пузырьков) — почва слабокислая или близкая к норме;
- реакция бурная — значит, щелочная среда.
д) Заказать исследование почвы в лаборатории
Раскисление почвы
Раскисление почвы – единственный способ поднять ее рН до нужной отметки (т. е. до 5,0 и выше). Раскисление почвы процесс не сложный, но требует определенных знаний. Процесс не быстрый, около полугода. Осень самое благоприятное время, чтобы к весне кислотно-щелочной баланс почвы был на оптимальном уровне.
Для раскисления используют следующие способы/материалы:
Источник
Показатели и методы оценки кислотно-основных свойств почв



Контрольные вопросы.
1. Что понимают под подвижностью химических элементов в почве?
2. Показатели, позволяющие определить подвижность: фактор интенсивности, фактор емкости, потенциальная буферная способность.
3. Методы оценки подвижности фосфатов. Почему подвижность фосфатов оценивают обычно фактором емкости?
4. Методы оценки подвижности калия. Почему подвижность калия оценивают обычно фактором интенсивности?
Кислотно-основные свойства почв характеризуют специфическим набором показателей. Универсальным показателем, который определяют во всех почвах, независимо от их свойств и используют практически при решении любых проблем, является рН (вспомнить, что это такое).
Величина рН позволяет дать сравнительную оценку активности Н + и ОН — ионов в жидких фазах исследуемых почвенных систем – реальных почв, паст, почвенных суспензий. В почвоведении кислотность, которая характеризуется величиной рН, часто называют актуальной кислотностью. В таком же понимании можно использовать термин актуальная щелочность, связанный с активностью гидроксил-ионов (рН +рОН=14). Но величины рН и рОН не дают сведений о количестве содержащихся в почве кислотных и основных компонентах, которые определяют уровни этих показателей. Такие сведения получают, определяя потенциальную кислотность и общую щелочность.
Для удобства использования в практических целях потенциальную кислотность можно рассматривать как показатель почвенной кислотности, характеризующий количество кислотных компонентов в почве, а общую щелочность – как показатель щелочности, характеризующий количество основных компонентов в почве.
Принято считать, что потенциальная кислотность связана главным образом с обменными катионами ППК, которые проявляют свойства кислот – ионами Н + и Al 3+ . Методы определения потенциальной кислотности основаны на обработке навески почвы растворами солей. В результате такой обработки эти катионы вытесняются из ППК вследствие ионного обмена. Их количество определяют титрованием щелочью.
Щелочность почв в основном связывают с анионами слабых кислот, которые проявляют свойства оснований вследствие гидролиза и присутствуют в почвах в составе различных солей – легко-, средне- и труднорастворимых. В соответствие с растворимостью эти соли переходят из твердых фаз почвы в почвенный раствор. Поэтому определение таких компонентов основано на анализе почвенных растворов, фильтратов из насыщенных водой почвенных паст, водных вытяжек. Количество извлеченных из почвы анионов-оснований определяют титрованием сильной кислотой и находят величину общей щелочности (ее иногда называют титруемой или титровальной). Кроме общей, определяют конкретные виды щелочности – карбонатную, боратную и др.
Таким образом, для оценки кислотности и щелочности используют две группы показателей. Первую группу составляют величины рН различных почвенных систем, вторую группу – потенциальная кислотность и общая щелочность. Эти показатели характеризуют разные аспекты кислотно-основных свойств почвы и не всегда взаимозаменяемы. Часто величину рН рассматривают как интенсивный показатель кислотно-основных свойств почвы ( фактор интенсивности), а потенциальную кислотность и общую щелочность – как экстенсивные показатели (факторы емкости).
(см.таблицу 15 стр210).
Способы оценки актуальной кислотности почв.
рН почвы прежде всего зависит от способности присутствующих в почве кислот к диссоциации. Чем сильнее выражена эта способность, чем большими константами диссоциации, или константами кислотности, характеризуются компоненты, тем большее влияние при прочих равных условиях они оказывают на рН.
С позиции теории кислот и оснований Бренстеда-Лоури аквакомплексы металлов рассматриваются как кислоты. Они вытесняют из воды ионы Н + . Однако однозарядные катионы щелочных металлов и двухзарядные катионы щелочно-земельных металлов проявляют очень слабые кислотные свойства и как кислоты практически не влияют на рН растворов. Кислотные свойства в воде проявляют двух- и особенно трехзарядные катионы переходных металлов. Например,

Для сравнения вспомним, что отрицательный логарифм константы кислотности уксусной кислоты (pKa 0 ) равен 4,75. Следовательно, аквакомплекс железа более сильный донор протонов, чем аквакомплекс алюминия и даже более сильный, чем уксусная кислота.
Измерение рН непосредственно в почве проводят довольно редко. Обычно рН измеряют в почвенных суспензиях, приготовленных из воздушно-сухих почвенных проб. Это технически довольно удобно и позволяет стандартизовать условия проведение анализа.
Определение рН проводят потенциометрическим методом. Одним из осложняющих факторов такого определения является суспензионный эффект. Он связан с наличием в системе твердых фаз, несущих на своей поверхности электрический заряд. Суспензионный эффект проявляется в различии значений рН, измеренных в суспензии и в ее фильтрате и возникает при использовании электрода сравнения с жидкостным контактом. Вследствие различной скорости диффузии ионов через границу раздела жидкостного соединения электрода сравнения и анализируемой среды возникает разность потенциалов, или диффузный потенциал. Он возникает и при анализе истинных растворов. Для уменьшения диффузного потенциала резервуар электрода сравнения заполняют раствором хлорида калия, т.к. ион K + и Cl — обладают практически одинаковой химической подвижностью. Однако, в почвенных суспензиях в присутствии заряженных коллоидов, подвижность K + и Cl — становится различной, что приводит к возникновению суспензионного эффекта. Чтобы уменьшить его влияние рекомендуют проводить измерение рН после отстаивания суспензии, при этом индикаторный электрод опускают в суспензию, а электрод сравнения
— в надосадочную жидкость. Величина суспензионного эффекта уменьшается с уменьшением концентрации твердых частиц, поэтому при измерении рН стандартизируют соотношение почвы и воды в суспензии.
В России в качестве стандартных условий используют соотношение почва- вода равное 1:2,5 при заполнении электрода сравнения 1М раствором хлорида калия.
Для оценки актуальной кислотности часто измеряют рН в солевых вытяжках с низкой концентрацией электролита (0,01М CaCl2). В них значительно снижается суспензионный эффект, быстрее устанавливается равновесие. Кроме того, концентрация соли в такой суспензии близка к концентрации электролитов в почвенном растворе, а кальций преобладает среди обменных оснований ППК. Значение рНCaCl2 обычно на 0,5 единиц ниже рНН2О. В этом случае в качестве показателя актуальной кислотности используют известковый потенциал:
Эта величина мало зависит от разбавления и концентрации солей, она достаточно стабильна и характеристична для почв. Однако нужно помнить, что в кислых почвах возможен обмен ионов кальция на ионы алюминия, т.е. этот процесс обязательно окажет влияние на величину актуальной кислотности.
Результаты измерения рН зависят от условий приготовления суспензии, в частности , от времени ее настаивания. В разных методиках это время различно ( от 5минут до 1 часа). В солевых суспензиях равновесие наступает быстрее, чем в водных. Независимо от свойств почв, для приготовления вытяжек используют воду, не содержащую СО2 !
Способы оценки потенциальной кислотности почв.
Потенциальная кислотность позволяет получить представление об общем содержании в почвах кислотных компонентов. В рамках потенциальной кислотности выделяют два вида почвенной кислотности: обменную и гидролитическую (рН-зависимую).
Обменная кислотность обусловлена относительно сильными кислотными компонентами – главным образом ионами Н + и Аl 3+ , которые компенсируют постоянные (перманентные) отрицательные заряды ППК. Ее определяют, обрабатывая навеску почвы небуферным раствором нейтральной соли (KCl,NaCl). Вытеснение обменных катионов при этом происходит при значениях рН, обусловленным кислотно-основными свойствами почвы. Таким образом, обменная кислотность является той частью почвенной кислотности, которая может проявиться в реальной почве, например при внесении удобрений. В России обменную кислотность определяют при исследовании любых кислых почв. Почву обрабатывают однократно 1М раствором КСl при отношении почва-раствор 1:2,5. Количество кислотных компонентов определяю титрованием аликвоты вытяжки раствором NaOH по фенолфталеину. Так как однократная обработка навески в таком узком отношении почва – раствор не позволяет полностью вытеснить из ППК обменные ионы водорода и алюминия, результат иногда умножают на 1,75.
Гидролитическая кислотность связана с переменными (рН-зависимыми) зарядами ППК. В сущности, переменные заряды ППК или переменная емкость ионного обмена часто обусловлены компонентами, которые обладают свойствами слабых кислот. К ним относят гидроксокомплесы алюминия различного состава, аллофаноподобные вещества, закрепленные на поверхности и в кристаллической решетке минералов, функциональные группы органических соединений и пр. Слабые кислоты диссоциируют при довольно высоких значениях рН, часто не свойственных самой почве. При диссоциации в жидкой фазе почвы появляются ионы водорода, а ППК приобретает дополнительный отрицательный заряд.
РН-зависимую кислотность в России определяют, используя раствор гидролизующейся соли (1М раствор ацетата натрия), поэтому ее называют гидролитической. Однако при этом определяется суммарное значение рН-зависимой и обменной кислотности.
Таким образом, общепринятыми показателями потенциальной кислотности почв являются: обменная кислотность, характеризующая количество наиболее сильных кислотных компонентов, которые компенсируют перманентные отрицательные заряды ППК и вытесняются из ППК при значениях рН, свойственных реальным кислым почвам (фактор интенсивности); рН-зависимая кислотность, характеризующее общее количество кислотных компонентов, включая компоненты, обуславливающие обменную кислотность, и те, которые вытесняются из рН-зависимых позиций ППК; эта кислотность проявляется при более высоких, чем обменная, значениях рН. Разница показателей рН- зависимой и обменной кислотности может служить фактором емкости при оценке потенциальной кислотности почв.
Щелочность почв. Способы оценки.
Щелочность почв связывают с анионами слабых минеральных (S 2- , PO4 3- , CO3 3- , HSiO3 — , H2BO3 — , HS — , HPO4 2- , HCO3 — ) и относительно более сильных, главным образом, органических кислот. Эти анионы проявляют свойства акцепторов протонов или оснований; при взаимодействии с водой они принимают от нее протон и в растворе появляются свободные гидроксил –ионы.(разобрать) В слабозасоленных почвах акцептором протонов может быть обменный натрий ППК, который взаимодействует с водой подобно соли слабой кислоты.(разобрать)
Актуальная щелочность и ее оценка.
Активность ОН — — ионов в жидких фазах почв, или актуальную щелочность, оценивают, измеряя рН различных почвенных систем: почвенных растворов, насыщенных водой почвенных паст, водных почвенных суспензий(1:1; 1:2,5; 1:5; 1;10). В России традиционно это рН суспензий 1:2,5. Однако при анализе засоленных почв методом водной вытяжки возможно использование суспензии 1:5 (ГОСТ 26423 – 85). Часто при анализе столь различных систем получают различные значения рН. Это связано не столько с суспензионным эффектом, сколько со смещением карбонатных равновесий. Ионы СО3 2- и НСО3 2- присутствуют в почвах в виде легкорастворимых солей NaHCO3 и Na2CO3 и в виде малорастворимого СаСО3. В соответствии с растворимостью последнего, карбонатные ионы в естественных условиях могут переходить из твердых фаз почв в жидкую, а при проведении анализа – в жидкие фазы паст и суспензий.
В растворах соотношение СО3 2- и НСО3 2- зависит от парциального давления СО2 в газовых фазах почвенных систем (РСО2):
Уменьшение РСО2 сдвигает равновесие в сторону образования СО3 2- , что приводит к росту рН вследствие того, что СО3 2- является более сильным донором протонов или более сильным основанием, чем НСО3 — , и наоборот, увеличение РСО2 сдвигает равновесие в сторону образования гидрокарбонат-ионов и рН уменьшается.
Определение различных видов щелочности.
Для раздельного определения оснований, обуславливающих щелочность почвенных систем, обычно используют потенциометрическое титрование.
В зависимости от природы оснований кривые их потенциометрического титрования имеют различную форму. (см.рис)
Кривые титрования S 2- и СО3 2- двухступенчаты. На кривой титрования РО4 3- также два скачка – один обусловлен переходом РО4 3- → НРО4 2- , второй – переходом НРО4 2- → Н2РО4 — . Третий скачок не выражен вследствие низкой основности иона Н2РО4 — .
Продукты титрования S 2- и СО3 2- летучи. Если эти продукты удалить и провести обратное титрование раствором NaOH, то кривые титрования будут иметь только один скачок, обусловленный титрованием избытка кислоты, добавленной при прямом титровании. Продукты титрования фосфатов нелетучи, поэтому кривые прямого и обратного титрования их имеют одинаковую форму. Кривые прямого и обратного титрования HSiO3 — , H2BO3 — , Al(OH)4 — имеют одинаковую форму и один скачок.
Анионы органических кислот обладают очень слабыми основными свойствами, поэтому кривые их прямого титрования практически не имеют скачка. Щелочность, обусловленную анионами органических кислот, находят по объему NaOH, израсходованному на обратное титрование анализируемого раствора от рН=4 до рН=7.
В отсутствие сульфидов карбонатную щелочность рассчитывают по уравнению Щкарб = (V1С1(1/z кислоты) – V2C2(1/z щелочи)) V0 100/Val m , ммоль-экв/100г почвы.
где V1 – объем кислоты, пошедший на прямое титрование до рН=4,мл;
С1 – нормальная концентрация раствора кислоты,мол-экв/л;
V2 – объем щелочи, пошедший на обратное титрование до рН=7,мл;
С1 – нормальная концентрация раствора щелочи,мол-экв/л;
V0 – общий объем воды, добавленной к почве,мл;
Val – объем аликвоты вытяжки, взятый на титрование, мл;
m – масса навески почвы, г.
Общее содержание бора и боратную щелочность определяют титрованием в присутствии маннита. Если рН раствора, в котором проводили прямое и обратное титрование, довести до 7 и добавить манит, то в отсутствие бора рН не изменится, а при наличии бора (Н3ВО3 при РН=7) образуется более сильная борно-маннитовая кислота и рН понижается. В этом случае проводят титрование раствором NaOH до рН=7. Боратную щелочность рассчитывают по уравнению:
где z – множитель, учитывающий диссоциацию борной кислоты в зависимости от рН вытяжки (справочные данные,табл.19,стр233)
Сульфидную щелочность можно ожидать в восстановленных почвах, если почвенные пробы хранились при естественной влажности в герметически закрытых сосудах. В таких случаях проводят анализ отдельной порции раствора. Аликвоту раствора подкисляют соляной кислотой до рН=3, переводя карбонаты в угольную кислоту, а сульфиды в сероводород. Газообразные продукты отгоняют с помощью инертного газа в раствор гидроксида бария. СО2 осаждается в виде ВаСО3, осадок отфильтровывают и в растворе определяют содержание сульфидов титрованием кислотой.
Общее содержание бора и боратную щелочность определяют титрованием в присутствии маннита. (табл.20,стр235).
Источник



