Большая Энциклопедия Нефти и Газа
Коагуляция — почвенный коллоид
Коагуляция почвенных коллоидов электролитами и взаимная коагуляция коллоидов имеет большое значение в формировании почвенного горизонта. Эти соли в воде гидролизуются и образуют положительно заряженные коллоидные частицы А1 ( ОН) з, кото — рые, взаимодействуя с коллоидными частицами в воде, заряженными в большинстве случаев отрицательно, приводят к взаимной коагуляции с выпадением коагулированных частиц в осадок. [2]
Оказалось, что главную роль в коагуляции почвенных коллоидов и в создании структуры почвы играет поглощенный кальций; вытеснение Са из поглощенного комплекса натрием приводит к пептизации или переходу в псевдораствор части почвенных коллоидов; видимая структура почвы при этом нарушается и коллоидальная часть почвы ( органическая и неорганическая) переходит в текучее, подвижное состояние и может уноситься промывными водами. Замещение Са в поглощающем комплексе ионами водорода может в естественных условиях происходить под влиянием длительного промывания почвы водой атмосферных осадков. Замена Са ионами водорода ( рост ненасыщенности основаниями) со-прово кдаетея постепенным разрушением поглощающего комплекса. В этом состоит сущность процесса оподзоливания почв. Таким образом, генезис почвенных типов определяется изменениями в составе поглощенных почвенным комплексом катионов. [3]
Высокое содержание нейтральных солей ( хлоридов и сульфатов) вызывает коагуляцию почвенных коллоидов , а присутствие щелочных солей ( соды) приводит к их пептизации. [5]
ОН-ионов, и поэтйму при щелочной реакции эти катионы не могут вызвать коагуляцию почвенных коллоидов . [6]
В этом случае силы притяжения между коллоидными частицами преобладают над силами отталкивания при взаимодействии двойных электрических слоев частиц, что вызывает коагуляцию почвенных коллоидов . Находясь в коагулированном состоянии, почвенные коллоиды не вымываются из верхнего пахотного горизонта, сообщая почве ценные агрономические свойства. [7]
Внесенный в солонцовую почву, гипс устраняет щелочную реакцию ее. Замена поглощенного натрия кальцием сопровождается коагуляцией почвенных коллоидов ; образующийся при разложении растительных остатков деятельный перегной в присутствии кальция склеивает почвенные комки, поэтому почва приобретает прочную комковатую структуру, улучшаются ее физические свойства, водопроницаемость и аэрация, облегчается обработка. [8]
Внесенный в солонцовую почву, гипс устраняет щелочную реакцию ее. Замена поглощенного натрия кальцием сопровождается коагуляцией почвенных коллоидов ; образующийся при разложении растительных остатков деятельный перегной в присутствии кальция склеивает почвенные комки, поэтому почва приобретает прочную комковатую структуру, улучшаются ее физические свойства, водопроницаемость и аэрация, облегчается обработка. Устраняя щелочность и улучшая физические свойства почвы, гипсование создает благоприятные условия для развития и деятельности почвенных микроорганизмов. [9]
С повышением кислотности среды коагулирующее действие катионов повышается, а при щелочной реакции значительно ослабевает. Коагулирующее действие одновалентных катионов оказывается слабее стабилизирующего влияния ОН-ионов, и поэтому при щелочной реакции эти катионы не могут вызвать коагуляцию почвенных коллоидов . [10]
Наряду с этим известкование способствует коагуляции почвенных коллоидов , что способствует предохранению их от разрушения и вымывания. Под влиянием извести улучшается структура почвы, повышается водопроницаемость и аэрация. [11]
Частным случаем коагуляции электролитами является взаимная коагуляция двух гидрофобных золей с различными знаками зарядов. В отличие от обычной электролитной коагуляции при определенном соотношении концентрации смешиваемых золей всегда наступает переразрядка, тогда как при обычной коагуляции переразрядка происходит только при действии многовалентных ионов-коагуляторов. Взаимная коагуляция имеет большое значение как в ряде природных, так и технологических процессов. Коагуляция почвенных коллоидов электролитами и взаимная коагуляция коллоидов имеет большое значение в формировании почвенного горизонта. Эти соли в воде гидролизуются и образуют положительно заряженные коллоидные частицы А1 ( ОН) 3) которые, взаимодействуя с коллоидными частицами в воде, заряженными в большинстве случаев отрицательно, приводят к взаимной коагуляции с выпадением коагулированных частиц в осадок. [12]
Пептизация может быть вызвана действием как электролитов, так и неэлектролитов, растворенных в жидкости. Растворенное вещество вызывает пептизацию в том случае, если его молекулы или ионы адсорбируются на поверхности данных частиц, образуя вокруг них довольно прочную адсорбционно-сольватную пленку или двойной электрический слой. Например, осадок Fe ( OH) 3 пептизируется солями трехвалентного железа ( в частности, РеС13), при действии которых потенциалообразующий ион Fe3 адсорбируется поверхностью частицы. В некоторых случаях пептизация вызывается заменой ионов диффузного слоя другими ионами с меньшей валентностью. В результате такой замены толщина диффузного слоя увеличивается, — потенциал возрастает, толщина гидратной оболочки вокруг частиц увеличивается, что приводит к разрыву связей между ними. Пептизация такого типа, основанная на ионном обмене, имеет место в почвах. В черноземных почвах коллоидные частицы содержат в диффузном слое преимущественно ионы Са2, что обусловливает небольшую величину — потенциала и слабые силы отталкивания. В этом случае силы притяжения между коллоидными частицами преобладают над силами отталкивания при взаимодействии двойных электрических слоев частиц, что вызывает коагуляцию почвенных коллоидов . Находясь в коагулированном состоянии, почвенные коллоиды не вымываются из верхнего пахотного горизонта, сообщая почве ценные агрономические свойства. [13]
Источник
Примеры коагуляции. Образование почв



Мы рассмотрели развитие основных идей, определяющих содержание проблемы устойчивости. Так, одна из важнейших задач заключается в сохранении устойчивого состояния суспензий, эмульсий и других объектов, проходящих в процессе переработки через сложные системы производственных агрегатов. Не менее важной для народного хозяйства является и обратная задача – скорейшего разрушения дисперсных систем: дымов, туманов, эмульсий, промышленных и сточных вод. Ограничимся здесь иллюстрацией многообразия и сложности коагуляционных явлений на примерах, связанных с процессами почвообразования.
Почвы образуются при разрушении горных пород в результате выветривания, выщелачивания, гидролиза и т.д. Эти процессы приводят к образованию окислов: как нерастворимых, типа SiO2, Al2O3, Fe2O3 (точнее – их гидроокисей), так и растворимых, типа RO и R2O (где R – металл). Из-за значительной гидратации нерастворимых элементов почвы и дальнему взаимодействию в процессе взаимной коагуляции образуются структурированные коагуляты, близкие по свойствам к гелям, называемые коагелями. Эти коллоидно-химические процессы определяют все многообразие существующих типов почв.
Например, подзолистые почвы, типичные для северных районов нашей страны, образуются в условиях малого содержания органических остатков (гуминовых веществ) и большой влажности, вымывающей окислы основного характера (RO и R2O). Остающиеся коагели характеризуются высоким содержанием SiO2 и малым количеством питательных веществ, необходимых для растений.
Наоборот, черноземные почвы средней полосы России образуются в условиях малой влажности. В этих условиях ионы Са 2+ и Mg 2+ не вымываются и, взаимодействия с гуминовыми кислотами, образуют нерастворимые высокомолекулярные коллоидные частицы – гуматы Са 2+ и Mg 2+ . В процессе взаимной коагуляции положительно заряженных частиц R2O3 с отрицательно заряженными гуматами и SiO2 возникают структурированные коагели, составляющие основу для образования плодородной почвы. Таким же образом и на основе коагуляционных представлений можно обосновать генезис и других типов почв.
Интересным примером коагуляционных процессов является возникновение иловых почв в дельтах рек. Наиболее примечательна в этом отношении дельта Нила, образующегося в результате слияния двух рек – Белого и Голубого Нила. Воды Белого Нила, берущего начало в болотах центральной Африки, несут большое количество органических (гуминовых) веществ, частично защищающих минеральные частицы. Эта высокодисперсная система является, благодаря защитному действию гуматов, весьма устойчивой, и воды Белого Нила на всем его протяжении характеризуются значительной мутностью.
Голубой Нил, стекая с горных хребтов Эфиопии, содержит (вследствие размывания горных пород) большое количество минеральных солей, вызывающих коагуляцию и осаждение гидрофобных минеральных частиц. Поэтому воды Голубого Нила совершенно прозрачны.
После слияния двух рек, вода Нила продолжает оставаться мутной, т.к. концентрация солей в воде Голубого Нила не достигает порога коагуляции, соответствующего сильно гидрофилизированным частицам, содержащимся в воде Белого Нила. Коагуляция наступает лишь в устье, где речная вода встречается с солеными водами Средиземного моря
и остановка течения способствует седиментации коагулированных агрегатов, приводящей к образованию плодородной дельты.
На этом примере, как в грандиозной панораме, мы видим все многообразие явлений устойчивости дисперсных систем и ее нарушений и можем вполне оценить ту огромную роль, которую играли коагуляционные процессы в создании первых очагов человеческой цивилизации (в дельтах Нила, Евфрата и Тигра, Волги, Дона, Днепра, Амударьи, Дуная и других великих рек).
Источник
Почва и почвообразование (Белицина Галина) — часть 13
заряда почвенных коллоидов и их гидратации (рис. 39). Заме
щение натрия кальцием способствует коагуляции и образованию
Реакция почвы также влияет на состояние коллоидов. Кислая
реакция способствует растворению некоторых коллоидов, напри
мер гидроксида алюминия; щелочная реакция стимулирует выпа
дение в осадок коллоидов полуторных оксидов и переход в со
стояние золя органических и некоторых минеральных коллоидов.
Часть коллоидов в почве находится в свободном состоянии,
часть образует пленки на поверхности более крупных грануло
метрических фракций путем адгезии, под которой понимается
слипание (склеивание) поверхностей каких-либо веществ раз
личного химического состава, соприкасающихся друг с другом.
Таким путем в почве при периодическом высушивании, приво
дящем к дегидратации коллоидов, происходит закрепление гуму
совых кислот и их солей на поверхности коллоидных частиц, а
минеральных, органических и органоминеральных коллоидов —
на поверхности частиц пылеватых и песчаных гранулометри
Особым явлением представляется процесс тиксотропии колло
идов. Она имеет две особенности: 1) образующийся из золя гель
не отделяется от дисперсной среды, а застудневает вместе с ней;
2) полученный гель обратим и может быть переведен в золь
путем механического воздействия (встряхивания, помешивания),
по прекращению которого золь снова с течением времени перехо
дит в гель. В почвах результатом тиксотропии является возник
новение особого рода коагуляционно-тиксотропной микрострук
туры, которая характеризуется образованием рыхлого каркаса
из коллоидных частичек в основном удлиненной формы, внутри
которого находится почвенный раствор. Тиксотропия особенно
развита в криогенных почвах, вызывая их плывунность. Тиксо-
тропные почвы плохо проницаемы для воды и воздуха, в них
часто развиваются восстановительные процессы.
В почве под влиянием различных факторов — периодическое
высушивание, нагревание, увлажнение, промораживание, изме
нение реакции среды и др. — происходит изменение вновь обра
зующихся при выветривании и почвообразовании органических
и минеральных коллоидов. Одним из таких изменений является
процесс старения коллоидов, под которым понимается самопро
извольное уменьшение их свободной поверхностной энергии.
Старение обычно не сопровождается изменением химического
и минералогического состава коллоидов, но при этом резко из
меняются их свойства: они становятся более гидрофобными,
уменьшается их сорбционная способность, связь с дисперсионной
средой, может произойти частичная кристаллизация гелей. Для
некоторых коллоидов причиной старения является окисление ки
слородом воздуха, например переход оксида Fe (II) в оксид
Fе (III). Свет, особенно ультрафиолетовое излучение, ускоряет
Источник
Коагуляция смесью электролитов
В промышленных условиях коагуляцию проводят смесью электролитов. Коагулирующее действие смеси электролитов часто бывает неаддитивным.
Если смеси электролитов требуется больше, чем одного из них, то наблюдается антагонизм электролитов (электролиты мешают друг другу).
Если смесь электролитов эффективнее одного электролита, то такое явление называется синергизмом электролитов (один электролит усиливает действие другого) – в смеси их требуется меньше, чем каждого в отдельности. Синергизм электролитов широко используется на практике для коагуляции больших количеств дисперсных систем.
Для характеристики смеси двух электролитов удобно пользоваться графиком порога коагуляции одного электролита 




Рис. 5.11. Характеристика коагуляции смесью двух электролитов при их аддитивном (1), антагонистическом (2), и синергетическом (3) действии
Синергизм характеризуется кривой 3 (рис. 5.11), т.е. если первый электролит берется в количестве 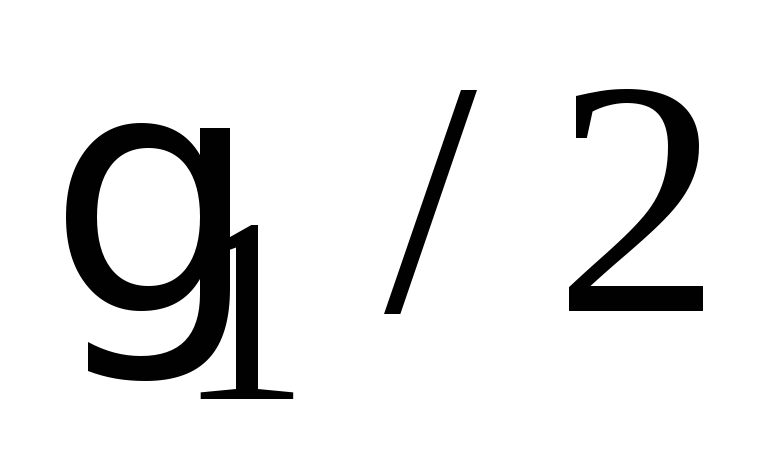
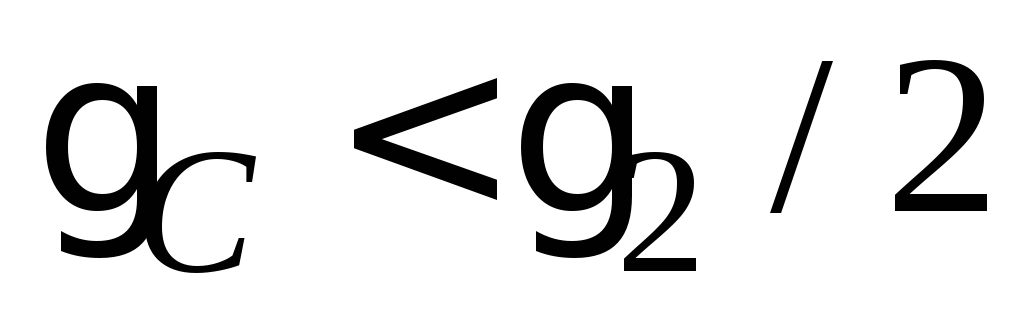
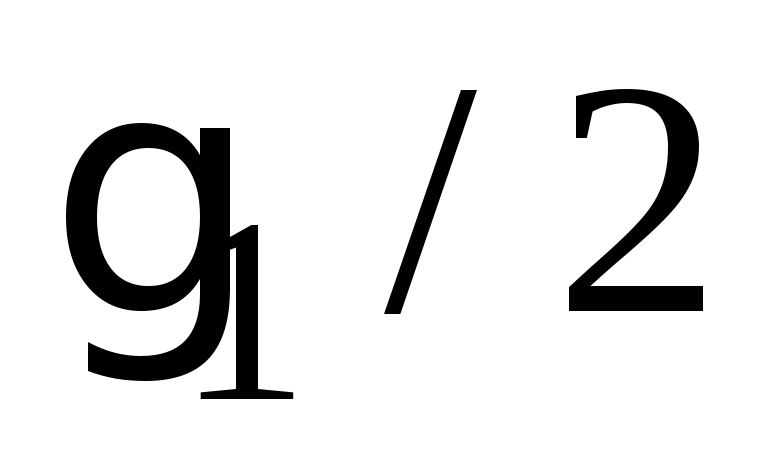

Привыкание коллоидных систем – при медленном введении электролита его требуется больше для коагуляции, чем при быстром введении.
5.4.2. Примеры коагуляции. Образование почв
Мы рассмотрели развитие основных идей, определяющих содержание проблемы устойчивости. Так, одна из важнейших задач заключается в сохранении устойчивого состояния суспензий, эмульсий и других объектов, проходящих в процессе переработки через сложные системы производственных агрегатов. Не менее важной для народного хозяйства является и обратная задача – скорейшего разрушения дисперсных систем: дымов, туманов, эмульсий, промышленных и сточных вод. Ограничимся здесь иллюстрацией многообразия и сложности коагуляционных явлений на примерах, связанных с процессами почвообразования.
Почвы образуются при разрушении горных пород в результате выветривания, выщелачивания, гидролиза и т.д. Эти процессы приводят к образованию окислов: как нерастворимых, типа SiO2, Al2O3, Fe2O3 (точнее – их гидроокисей), так и растворимых, типа RO и R2O (где R – металл). Из-за значительной гидратации нерастворимых элементов почвы и дальнему взаимодействию в процессе взаимной коагуляции образуются структурированные коагуляты, близкие по свойствам к гелям, называемые коагелями. Эти коллоидно-химические процессы определяют все многообразие существующих типов почв.
Например, подзолистые почвы, типичные для северных районов нашей страны, образуются в условиях малого содержания органических остатков (гуминовых веществ) и большой влажности, вымывающей окислы основного характера (RO и R2O). Остающиеся коагели характеризуются высоким содержанием SiO2 и малым количеством питательных веществ, необходимых для растений.
Наоборот, черноземные почвы средней полосы России образуются в условиях малой влажности. В этих условиях ионы Са 2+ и Mg 2+ не вымываются и, взаимодействия с гуминовыми кислотами, образуют нерастворимые высокомолекулярные коллоидные частицы – гуматы Са 2+ и Mg 2+ . В процессе взаимной коагуляции положительно заряженных частиц R2O3 с отрицательно заряженными гуматами и SiO2 возникают структурированные коагели, составляющие основу для образования плодородной почвы. Таким же образом и на основе коагуляционных представлений можно обосновать генезис и других типов почв.
Интересным примером коагуляционных процессов является возникновение иловых почв в дельтах рек. Наиболее примечательна в этом отношении дельта Нила, образующегося в результате слияния двух рек – Белого и Голубого Нила. Воды Белого Нила, берущего начало в болотах центральной Африки, несут большое количество органических (гуминовых) веществ, частично защищающих минеральные частицы. Эта высокодисперсная система является, благодаря защитному действию гуматов, весьма устойчивой, и воды Белого Нила на всем его протяжении характеризуются значительной мутностью.
Голубой Нил, стекая с горных хребтов Эфиопии, содержит (вследствие размывания горных пород) большое количество минеральных солей, вызывающих коагуляцию и осаждение гидрофобных минеральных частиц. Поэтому воды Голубого Нила совершенно прозрачны.
После слияния двух рек, вода Нила продолжает оставаться мутной, т.к. концентрация солей в воде Голубого Нила не достигает порога коагуляции, соответствующего сильно гидрофилизированным частицам, содержащимся в воде Белого Нила. Коагуляция наступает лишь в устье, где речная вода встречается с солеными водами Средиземного моря и остановка течения способствует седиментации коагулированных агрегатов, приводящей к образованию плодородной дельты.
На этом примере, как в грандиозной панораме, мы видим все многообразие явлений устойчивости дисперсных систем и ее нарушений и можем вполне оценить ту огромную роль, которую играли коагуляционные процессы в создании первых очагов человеческой цивилизации (в дельтах Нила, Евфрата и Тигра, Волги, Дона, Днепра, Амударьи, Дуная и других великих рек).
Источник



