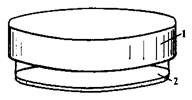
Термостат
Так как для роста и развития микробов нужна постоянная оптимальная для каждого вида определенная температура, то для выращивания микробных культур в лаборатории необходимо иметь специальные термостаты (от греческого therme — тепло, жар, statos — постоянный, неменяющийся). Термостаты — приборы, в которых непрерывно автоматически поддерживается заданная (высокая или низкая) температура.
Термостаты представляют собой металлические ящики — шкафы с двойными стенками, обогреваемые теплым воздухом (воздушные термостаты) или водой (водяные термостаты) (рис. 51).
В настоящее время большинство термостатов конструируется с электрическим обогревом. Снаружи термостаты покрываются теплоизолирующим материалом (асбестом и пр.). На верхней крышке термостата устанавливается термометр и терморегулятор для поддержания температуры на определенном уровне. Существуют различные системы терморегуляторов (ртутные, биметаллические), подробно описываемые в паспорте, прилагаемом к прибору.
Водяные термостаты более теплоустойчивы, чем воздушные. Равномерная постоянная температура рабочего пространства водяного термостата поддерживается благодаря большой массе воды, заливаемой в пространство между стенками термостата. В микробиологической лаборатории консервного завода рекомендуется иметь:
а) два термостата, отрегулированных на 37°С: в одном из этих термостатов выдерживают отобранную для анализа готовую продукцию перед исследованием, во втором — выращивают посевы продукции с объектов технологических линий;
б) термостат на 55 °С для выращивания термофильных микроорганизмов;
в) термостат на 43 °С для бактериологического анализа воды.
Источник
Стерилизации и других микробиологических целей



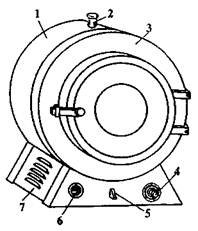
Термостат – прибор для поддержания постоянства температуры — применяют для выращивания культур микроорганизмов. Он представляет собой шкаф (рисунок 1), в котором поддерживается в течение длительного времени определенная температура. Оптимальная температура для размножения многих микроорганизмов 37 ºС. Термостаты бывают суховоздушными и водяными.
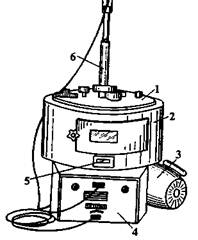
Сушильный шкаф (печь Пастера) используют для стерилизации сухим жаром посуды, инвентаря и сухих материалов, например крахмала, мела (рисунок 2). Стерилизуемый материал предварительно заворачивают в бумагу и помещают в шкаф так, чтобы он не касался стенок. Стерилизацию проводят при температуре 160 ºС в течение двух часов. Поднимать температуру выше 180 ºС не рекомендуется: ватные пробки и бумага начинают разрушаться (буреют, становятся ломкими). Простерилизованный материал вынимают после отключения и охлаждения шкафа, лучше, когда температура в шкафу сравняется с комнатной.
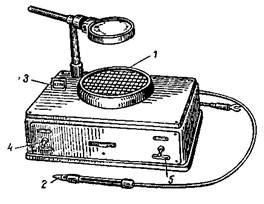
Прибор для счета колоний(рисунок 3) — полуавтоматический счетчик, снабженный электропером с пружинным устройством, предназначенный для счета колоний бактерий в чашках Петри. Чашку
Петри с колониями бактерий устанавливают вверх дном на растровое стекло. Легкий нажим электропера на участке дна чашки Петри, соответствующем положению колонии, оставляет на стекле метку. При этом держатель поднимается вверх, цепь замыкается, и показания счетчика увеличиваются на единицу. Отсчет количества колоний бактерий производится путем вычисления разности показаний импульсного счетчика до начала отсчета и после его окончания.
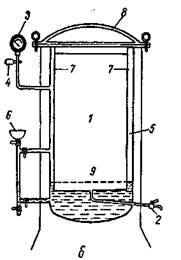
Автоклав (рисунок 4) – толстостенный аппарат, предназначенный для стерилизации посуды и питательных сред паром под давлением. Это герметичный котел с двойными металлическими стенками и крышкой. Пространство между стенками (водопаровая камера) заполняется водой. Внутренняя часть (стерилизационная камера) снабжена манометром, предохранительными клапанами и краном для спуска воды и пара. Для создания герметичности автоклав плотно закрывается крышкой с резиновой прокладкой. Применяют для стерилизации питательных сред под давлением от 0,5 до 1,0 МПа в течение 20…30 минут.
1 – корпус; 2 – термометр; 1 – крышка; 2 – корпус;
3 – дверца; 4 – потенциометр; 3 – редуктор; 4 – блок управления;
5 – тумблер; 6 – лампа; 5 – маркировка; 6 – термометр
7 – вентиляционные отверстия
Рисунок 1 – Термостат Рисунок 2 — Сушильный шкаф
1 – столик для чашки Петри; 2 – перо с пружинным устройством;
3 – показатель счетчика; 4 – тумблер для включения импульсного счетчика; 5 – тумблер для включения лампы освещения счетчика
Рисунок 3 — Прибор для счёта колоний микроорганизмов
|
|
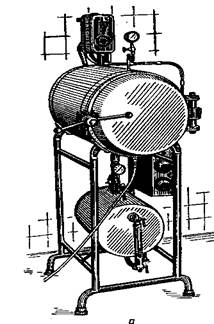
1 – стерилизационная камера; 2 – кран для выхода воздуха;
3 – манометр; 4 – предохранительный клапан;
5 – водопаровая камера; 6 – воронка для заполнения автоклава водой;
7 – отверстия для поступления пара в стерилизационную камеру;
8 – крышка; 9 – подставка для размещения стерилизуемых материалов
Рисунок 4 – Горизонтальный (а) и вертикальный (схема) (б) автоклавы
1 – крышка; 2 – дно
Рисунок 5 — Чашка Петри
Холодильникииспользуются в микробиологических лабораториях для хранения культур микроорганизмов, питательных сред, сывороток и прочих биологически активных препаратов при температуре около 4 ºС. Для сохранения биопрепаратов при температуре ниже 0 ºС используются низкотемпературные холодильники, в которых поддерживается температура минус 20 ºС и ниже.
Аппарат Коха применяют для стерилизации питательных сред, разрушающихся при температуре выше 100 ºС. Он представляет собой металлический полый цилиндр с двойным дном и конусообразной крышкой, которая имеет отверстие для выхода пара. Аппарат покрыт теплоизолирующим материалом (асбестом или линолеумом). Сосуды с питательными средами ставят на подставку с отверстиями, находящуюся внутри аппарата неплотно, чтобы обеспечить возможность наибольшего контакта их с паром. Обработка стерилизуемого материала в аппарате Коха производится в течение трех дней по 30 минут ежедневно. В перерывах между стерилизацией среду помещают на двадцать четыре часа в термостат при 28…30 ºС.

Центрифугиприменяются для осаждения микроорганизмов и других клеток, для разделения неоднородных жидкостей (эмульсии, суспензии). В основе метода центрифугирования лежит принцип отделения крупных частиц с большей плотностью при низких скоростях. При повышении скорости центрифуг можно осадить все более мелкие частицы.
Микроанаэростат — аппарат для выращивания микроорганизмов в анаэробных условиях.
4.2 Посуда и инструменты, применяемые
в микробиологической лаборатории
Выращивают микроорганизмы в стеклянной посуде: пробирках, колбах или чашках Петри. В пробирках микроорганизмы культивируют как в жидких, так и на плотных средах. Жидкой средой для аэробных культур заполняют обычно 
При помощи пипеток проводят пересев жидких культур микроорганизмов. Бродильные трубки используют для определения активности брожения по газообразованию.
Для работы с микроорганизмами используют специальные бактериологические иглы, петли и шпатели (рисунок 6). Их изготавливают из платиновой проволоки, которую закрепляют в специальных металлических держателях или впаивают в стеклянные палочки. Толщина игл и петель не должна превышать 0,5 мм, шпателя – 1,5 мм и более. При посевах (и пересевах) культур микроорганизмов из колоний, выросших на плотных средах, применяются иглы или шпатели. Шпатели также используют для взятия клеток микроорганизмов из колоний, врастающих в субстрат, и для размазывания жидких культур на поверхности плотной питательной среды. Суспензии микроорганизмов берут петлей.
При приготовлении препаратов микроорганизмов предметные стекла удерживают на весу пинцетами Корнэ или специальными пинцетами-держателями. Сушить препараты целесообразно на верхнем ярусе сушильного металлического столика Коха. Промывать их удобно на приспособлениях – перекладинах или на так называемых препаратодержателях – параллельно расположенных стеклянных палочках, соединенных резиновыми трубками (длина палочек от 20 до 30 см, трубок от 15 до 20 см). Палочки устанавливают над фарфоровыми чашками или ваннами.
Источник
Термостат для выращивания бактерий
Для успешного культивирования микроорганизмов важно не только правильно подобрать питательную среду и правильно произвести посев, но еще необходимо создать и оптимальные условия: обеспечить соответствующую температуру, влажность, аэрацию. Как правило, успешное культивирование микроорганизмов в лаборатории удается только при тщательном воспроизведении условий природной для них среды.
Оптимальную температуру при культивировании большинства патогенных для теплокровных (в том числе и человека) микроорганизмов (37 градусов) создают в термостате.
Термостат представляет собой прибор с двойными стенками, между которыми находится воздух или вода. Подогрев воды осуществляется при помощи электрического тока. Термостат снабжен терморегулятором, автоматически поддерживающим нужную температуру, и термометром для контроля за температурой.
Пробирки с посевами устанавливают в штативах на полках термостата. Чашки в термостате должны стоять вверх дном.
Чтобы воздух в термостате свободно циркулировал и нагрев был равномерным, полки в термостате делают с прорезами и при работе плотно не загружают.
Чтобы не охладить культуры, термостат надолго не оставляют открытым.
Жизнь микроорганизмов возможна только во влажных условиях. Для микробов необходима капельно – жидкая среда – вода, так как питательные вещества проникают в клетку только в растворенном состоянии. Минимальное содержание свободной воды, при котором еще возможно развитие, для большинства микроорганизмов равно примерно 20%.
При культивировании в жидких питательных средах проблемы поддержания влажности не существует.
Свежеприготовленные агаризированные среды всегда содержат некоторое количество капельно – жидкой воды. Она бывает заметна в виде более или менее обильного конденсата, Однако при длительном хранении культур на плотных средах при комнатной температуре и даже в холодильнике среды подсыхают, что может привести к гибели микроорганизмов. Поэтому необходимо производить регулярные своевременные пересевы культур, не допуская подсыхания сред. Если предполагается длительное культивирование в термостате, то чашки или пробирки лучше всего поместить во влажную камеру, т.е в закрытый сосуд, где имеется емкость с водой. Некоторые грибы могут расти на плотных субстратах без капельно – жидкой среды, но во влажной атмосфере.
В день посева плотные питательные среды, основу которых составляет агар – агар, расплавляют на водяной бане и в жидком состоянии стерильно разливают в чашки Петри. После застывания агара и подсушивания конденсационной воды в термостате, можно производить посев на пластинчатый агар. Скашивать плотные питательные среды в пробирках также лучше в день посева. При культивировании микробов особенно чувствительных к отсутствию влаги (например, гонококков) в термостат ставят открытый сосуд с водой.
Подавляющему большинству микробов, в том числе и патогенным, свет не нужен. Прямые солнечные лучи отрицательно влияют на развитие многих микроорганизмов, поэтому их культивируют в неосвещенных термостатах. Однако, для изучения пигментообразования, которое происходит активнее при рассеянном свете, культуры после термостата выдерживают 2 – 3 дня при комнатном освещении.
Микроорганизмы, использующие в процессах обмена веществ энергию света, выращиваются при освещении. Для освещения обычно применяют лампы накаливания мощностью 75 – 100 вт. При культивировании водорослей можно использовать и люминесцентные лампы.
Большинство патогенных микробов культивируют 18 – 24 часа, но есть виды, развивающиеся значительно быстрее (холерный вибрион 8 – 10 часов) или медленнее (бруцеллы 5 – 27 дней, туберкулезные бактерии 4 – 6 недель и т.д.).
Продолжительность культивирования микроорганизмов зависит от скорости их размножения. Чтобы сохранить влагу в пробирках при длительном культивировании микробов, ватные пробки после посева заменяют стерильными резиновыми или надевают на них резиновые колпачки.
По потребности микробов в свободном кислороде их делят на облигатные аэробы (возбудители холеры, чумы, туберкулеза), анаэробы (возбудители столбняка, ботулизма, газовой раневой инфекции, бактероиды) и факультативные анаэробы (возбудители брюшного тифа, дизентерии, стафилококки и др.). Эти группы требуют различных условий культивирования.
При культивировании аэробов и факультативных анаэробов поступление необходимого кислорода осуществляется при пассивной и активной аэрации.
Пассивная аэрация – это культивирование микроорганизмов на плотных и жидких питательных средах, закрытых ватными или ватно – марлевыми пробками, а также на плотных питательных средах в чашках Петри. В этом случае микроорганизмы развиваются на поверхности среды и получают кислород непосредственно из воздуха пробирки или чашки Петри. Поэтому при поверхностном культивировании микроорганизмов стараются увеличить площадь соприкосновения среды с воздухом. Для этого среды наливают тонким слоем в посуду с широким дном (чашки Петри, колбы Виноградского, матрацы).
На жидких средах аэробные микроорганизмы растут в виде пленок, обычно достаточно плотных. Факультативные анаэробы развиваются также и в толще жидкой среды, образуя более или менее равномерное помутнение или хлопья. Для них характерны менее плотные пленки, чем для облигатных аэробов.
Поверхностное культивирование микроорганизмов применяют в лабораториях и в промышленности.
Активную аэрацию применяют при глубинном культивировании микробов, когда их выращивают в больших объемах среды. Чтобы достаточно снабдить кислородом такие культуры, их помещают в специальные качалки – постоянное перемешивание культуры обеспечивает соприкосновение ее с воздухом. При культивировании микробов в объемах жидкости, достигающих десятков и сотен литров, используются приборы, называемые реакторами или ферменторами. Воздух продувают через культуру при помощи специальных устройств.
Культивирование анаэробов сложнее, чем аэробов, так как их необходимо лишить доступа свободного кислорода воздуха. Для этого из питательной среды удаляют воздух, применяя различные способы:
1. Удаление кислорода механическим путем. Анаэробные микроорганизмы можно культивировать в обычных чашках Петри, помещая их сразу после засева в анаэростат, из которого затем откачивается воздух. Анаэростаты – это вакуумные металлические или стеклянные эксикаторы. Металлические анаэростаты имеют герметически закрывающуюся крышку и снабжены манометром. Они способны сохранять высокое разряжение в течение длительного времени. Стеклянные вакуумные эксикаторы имеют пришлифованную крышку с краном на шлифах для откачивания воздуха. Пришлифованные поверхности эксикатора во избежание проникновения в него воздуха покрывают специальной вакуумной смазкой.
2. Замещение воздуха в анаэростате азотом, аргоном, водородом или смесью азота с углекислым газом.
3. Культивирование в высоком столбике агара с глюкозой. При этом способе микроорганизмы растут на дне, защищенные от воздуха высоким слоем среды.
4. Удаление кислорода химическим способом достигается при его окислении различных веществ кислородом, содержащимся в среде и сосудах для культивирования.
5. Метод Виньяля – Вейона заключается в том, что посев производят в пробирку с расплавленным и остуженным до 45 градусов агаром. Содержимое пробирки перемешивают и набирают в пастеровскую пипетку при помощи груши, заполняя пипетку до самого верха. Необходимо следить, чтобы в пипетку не попали пузырьки воздуха. Тонкий конец пипетки запаивают и пипетку помещают в термостат. В толще агара вырастают изолированные колонии анаэробов.
6. Добавление в среду редуцирующих (окисляющих) веществ. Используют среду Китт – Тароцци, содержащую в качестве редуцирующих веществ 0,5% раствор глюкозы, кусочки печени или яичного белка. Перед посевом среду кипятят 20 минут на водяной бане для удаления из нее растворенного кислорода. Перед посевом в пробирку на поверхность питательной среды наливают стерильное масло слоем 0,5 – 1,0 см для защиты анаэробов от проникновения кислорода.
7. Биологический метод Фортнера. В чашку Петри наливают толстым слоем агар с 5% крови. Чтобы культуры не смешивались, по диаметру чашки делают желобок в агаре. На одну половину питательной среды засевают аэробы, на другую – анаэробы. Края чашки тщательно заливают парафином. Посевы ставят в термостат. Сначала вырастают аэробы, а после поглощения ими кислорода, находящегося в чашке, начнут развиваться анаэробы.
Культивирование актиномицетов, грибов, микоплазм, L-форм, спирохет и простейших принципиально сходно с культивированием бактерий. Для них разработаны специальные среды и подобраны режимы, соответствующие их потребностям.
По типу питания грибы являются гетеротрофами. В качестве источника углерода грибы могут использовать большинство органических веществ. Однако, некоторые грибы лучше используют глюкозу, другие – фруктозу или пентозу. В качестве источника азота грибы могут использовать такие органические соединения как белки, пептон, пептиды, аминокислоты, соли аммония, нитраты, азот атмосферы. Диапазон использования перечисленных источников азота у разных видов грибов неодинаков.
Для роста и жизнедеятельности грибов необходимы минеральные вещества. Кроме макроэлементов (углерода, кислорода, водорода, азота, серы, фосфора, калия, кальция, магния, железа) им необходимы и микроэлементы (марганец, цинк, медь, кобальт, никель и др.).
Важную роль в физиологии грибов играют витамины. Потребность в витаминах у грибов зависит от ростовой реакции.
В отношении питательных сред большинство грибов крайне непритязательны. Они хорошо растут на самых разнообразных субстратах: картофеле, моркови, сахарном агаре, глицериновом агаре. Оптимальный рост грибов происходит при температуре 26 – 28 градусов. В зависимости от состава питательной среды особенности культуральных чвойств того или иного гриба могут варьировать.
Грибы культивируют с разными целями – для поддержания в жизнеспособном состоянии без потери функций и особенностей строения, для идентификации, получения продуктов метаболизма грибов, сохранения посевных культур и т.д. Подбор среды для культивирования грибов зависит от цели исследования и биологических особенностей микроорганизма.
Среды для культивирования грибов по составу ингредиентов бывают: 1. Природные – разнообразные субстраты растительного и животного происхождения (корнеплоды, зерно злаков, листья, стебли растений, органы и ткани животных).
2. Полусинтетические – это комбинированные среды из природных субстратов и химически известных компонентов.
3. Синтетические – состоящие из ингредиентов известного состава. Различные комбинации ингредиентов в синтетических средах и их концентраций практически не ограничены и могут служить для выяснения разнообразных процессов жизнедеятельности грибов, связанных с их ростом, размножением и физиологической активностью.
Для актиномицетов наиболее подходящими питательными средами являются щелочной глицериновый агар, картофель, сывороточные, мясные и асцитические среды, а также агар Сабуро. Посевы культивируют в аэробных и анаэробных условиях при 35 – 37 градусах не менее двух недель.
Культивирование кишечных простейших на специальных питательных средах является биологическим методом обогащения, позволяющим из единичных экземпляров паразитов получить достаточное их количество. Увеличение количества экземпляров в результате их размножения на питательной среде облегчает обнаружение и изучение паразитов.
Для культивирования кишечных амеб применяется среда, в состав которой входят четыре яйца и среда Локка (1000 мл дистиллированной воды, NaHCOз – 0,2г, хлористый кальций – 0,2г, KCl – 0,4г, NaCl – 9,0г, глюкозы – 2,5г, рН среды – 7,4). Для получения скошенной поверхности среды, пробирки в наклонном положении помещают в аппарат для свертывания и выдерживают при 70 градусах до затвердевания. Перед посевом в пробирку с плотной питательной средой добавляется несколько капель инактивированной человеческой или лошадиной сыворотки и 1 – 2 петли стерильного рисового отвара.
Для культивирования жгутиконосцев к 200 мл среды Локка добавляется одно яйцо, и полученная смесь подогревается на водяной бане в течение 15 минут. Затем смесь фильтруется через марлю, разливается по 5 – 6 мл в пробирки и стерилизуется в автоклаве под давлением в течение 20 минут.
При культивировании балантидий может быть использована среда Френкеля (4,0г аспарагина, 6,0г ammonium lacticum, 2,0г двухзамещенного фосфорнокислого калия, 5,0г NaCl, 1000 мл дистиллированной воды). Среда стерилизуется в автоклаве в течение 20 минут при 120 градусах, 1 атм. Затем к ней добавляются стерильные лошадиная сыворотка в разведении 1:10 и 2 – 3 капли крахмала (рН среды 7,2 – 7,4).
Культивирование простейших осуществляется в термостате при 37 градусах. Пересевы проводятся через день.
Риккетсии, хламидии и вирусы, являющиеся строгими внутриклеточными паразитами, совершенно не культивируются на искусственных питательных средах, используемых для культивирования бактерий, грибов, микоплазм и простейших.
Риккетсии обладают собственным метаболизмом, однако являются полностью энергетически зависимыми от тканевой клетки, поэтому риккетсии и являются внутриклеточными паразитами.. В клетке хозяина каждый вид риккетсий размножается только в определенных местах: в цитоплазме, ядре или вакуолях клеток. Риккетсии культивируются в кишечнике платяных вшей, желточном мешке развивающегося куриного эмбриона, в клетках легких белых мышей, в клетках неперевиваемых культур тканей.
У хламидий наблюдается не только энергетическая зависимость от клетки ткани, но и слабо выражена метаболическая активность. Поэтому хламидии можно культивировать только в желточном мешке развивающегося куриного эмбриона или в клетках культур тканей.
Культивирование вирусов проводится для их выделения и накопления с диагностическими целями, для последующего их изучения, для получения биологических препаратов, для изучения вирусного онкогенеза и патогенеза вирусных инфекций.
Вирусы являются строгими внутриклеточными паразитами и для их культивирования применяются (при строгом контроле) три метода:
1) в организме восприимчивого животного;
2) в развивающемся курином эмбрионе;
3) в культуре клеток.
В вирусологической практике для культивирования вирусов используют преимущественно новорожденных животных, поскольку они более чувствительны к вирусам. Этот метод имеет ограниченное применение, поскольку вирусы обладают очень выраженным специфическим тропизмом.
Куриные эмбрионы используются для культивирования только некоторых вирусов – гриппа, герпеса, натуральной и обезьяней оспы, паротита.
Наиболее широко в вирусологической практике для культивирования вирусов используются клетки культур тканей. Эти клетки по числу жизнеспособных генераций можно подразделить на три группы:
1. Первичные;
2. Перевиваемые;
3. Полуперевиваемые.
К первичным культурам относятся культуры клеток, способные выдерживать не более 5 – 10 пассажей. Их готовят преимущественно из эмбриональных тканей: почечной ткани эмбриона человека и обезьян, амниона человека, куриного эмбриона, эмбриона мышей, а также из почек взрослых обезьян.
К полуперевиваемым культурам клеток относятся культуры диплоидных клеток, получаемых из фибробластов человеческого эмбриона. Эти клетки выдерживают до 150 генераций, сохраняя исходный диплоидный набор хромосом. Диплоидные клетки нашли широкое применение в вирусологии.
Перевиваемые культуры получают преимущественно из опухолевых клеток одного типа, хорошо размножающихся in vitro в течение длительного времени. К таким клеткам относятся линии, ведущие свое начало от карцином человека (HeLa, Hep -2 и др.). Основное преимущество перевиваемых линий перед первичной культурой клеток состоит в их способности размножаться в лабораторных условиях в течение длительного срока в многочисленных генерациях.
Для выращивания культур клеток любого типа необходимы питательные среды. Наиболее широкое применение нашла среда 199. В состав этой среды входят минеральные соли, глюкоза, аминокислоты, витамины, ко – ферменты и многие другие компоненты. Кроме того, в питательную среду обязательно вносят сыворотку крови и буферные растворы для поддержания стабильного рН. Чтобы предотвратить бактериальное загрязнение, в среду добавляют антибиотики.
Источник