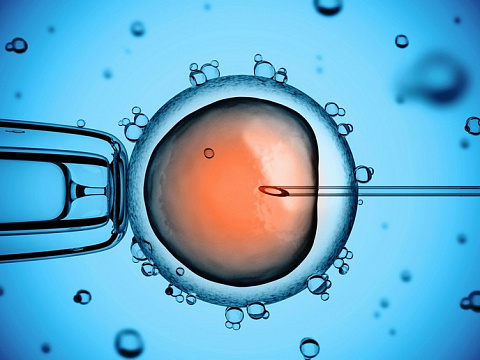
Ученые вырастили эмбрион мыши вне матки
Профессор Якоб Ханна из Института науки Вейцмана и его группа смогли вырастить эмбрион мыши вне матки. Они разработали метод, который позволяет отслеживать развитие эмбриона, а также понять, как работают гены и выявлять врожденные дефекты и пороки развития.
Ханна объясняет, что информация об эмбриональном развитии млекопитающих получена либо из наблюдений за этим процессом у лягушек и рыб, либо из статических изображений рассеченных эмбрионов мыши.
По словам ученого, идея выращивания эмбрионов вне матки существует еще до 1930-х годов, но более ранние эксперименты имели ограниченный успех. Команда Ханны решила возобновить эти усилия.
За семь лет исследователи разработали двухэтапный процесс и смогли вырастить нормально развивающиеся мышиные эмбрионы вне матки в течение шести дней. Это примерно треть срока их вынашивания, который составляет 20 дней. К этому моменту у эмбрионов уже формируется тело и органы.
На первом этапе, который длился около двух дней, исследователи работали с эмбрионами в возрасте нескольких дней — сразу после того, как они должны были быть имплантированы в матку. На этом этапе эмбрионы представляли собой шарики, состоящие из 250 одинаковых стволовых клеток. Их поместили на специальную питательную среду, и шарики закрепились внутри лабораторной посуды. После этого эмбрионы удваиваются и утраиваются в размерах, формируются три слоя: внутренний, средний и внешний.
По прошествии двух дней, когда эмбрионы вступили в следующую стадию развития —формирование органов из каждого из слоев — им потребовались дополнительные условия. Ученые поместили их в питательный раствор в крошечные мензурки, установив те на ролики, которые позволяли раствору непрерывно перемешиваться. Таким образом, эмбрионы могли расти без притока материнской крови к плаценте.
Команда сравнила полученные образцы с эмбрионами, удаленными у беременных мышей в соответствующий период времени. Они оказались практически идентичными.
В последующих экспериментах ученые поместили в зародыши гены, которые пометили растущие органы флуоресцентными цветами. Успех этой попытки показал, что дальнейшие эксперименты, включающие различные генетические и другие манипуляции, должны дать надежные результаты.
По словам Ханны, теперь ученые могут внедрять гены в клетки эмбриона, заражать их вирусами и проводить другие эксперименты. Команда уверена, что этот метод снизит стоимость и ускорит процесс исследований в области биологии развития, а также уменьшит потребность в лабораторных животных.
Следующим шагом лаборатории станет проверка того, можно ли пропустить этап удаления эмбрионов у беременных мышей. Ученые намерены создать искусственные эмбрионы из стволовых клеток.
Среди прочего, они надеются выяснить, почему при многих беременностях не удается имплантировать эмбрион, почему окно для имплантации так мало, а также, как стволовые клетки постепенно теряют свои свойства и при каких условиях беременности плод будет развиваться с нарушениями.
Источник
Биомешок или искусственная матка: заменят ли технологии женское тело
Будут ли искусственно выращивать детей вне тела женщины? Как далеко ушли репродуктивные технологии? Заменят ли секс-роботы нам партнеров? Смогут ли инновации изменить нашу жизнь, перевернув традиционный уклад? На эти и другие вопросы Дженни Климан ищет ответы в своей книге «Секс без людей, мясо без животных. Кто проектирует мир будущего». Журналистка провела десятки интервью с учеными, программистами, врачами и другими экспертами, чтобы понять, какое будущее ждет нас уже завтра. Перевод книги выходит в издательстве «Индивидуум» и поступит в продажу уже на этой неделе. Forbes Woman публикует отрывок об этических границах эктогенеза.
Печально известен случай 2012 года, когда беременная итальянка прилетела в Англию на двухнедельные курсы авиакомпании Ryanair в Станстеде. В отеле у нее началась паническая атака, она позвонила в полицию, там связались по телефону с ее матерью. Она объяснила, что ее дочь, скорее всего, не приняла лекарство от биполярного расстройства. Полиция поместила девушку в психиатрическую больницу по закону о психическом здоровье. Через пять недель по приказу опекунского суда, полученному филиалом Национальной службы здравоохранения в Мид-Эссексе, женщине насильно дали успокоительное, после чего без разрешения провели роды с кесаревым сечением. Соцслужба Эссекса немедленно забрала дочь, а мать отправили обратно в Италию без ребенка.
Когда год спустя публике стали известны подробности, которые можно обнародовать по закону, соцслужба Эссекса оправдывалась тем, что действовала во благо ребенка. Даже в якобы либеральной и просвещенной Норвегии желание государства защитить младенцев может перевесить значение заботы о тех, кто их вынашивает. Между 2008 и 2014 годами число новорожденных, которых сразу после родов забирала у матерей норвежская служба защиты детей, утроилось. Самая распространенная причина для «приказов о неотложном попечении» — с большим отрывом — не злоупотребление наркотиками или алкоголем, а «отсутствие родительских навыков»: неопределенный термин, включающий в себя матерей из стран, где приемлемо физическое наказание детей, матерей с психическими заболеваниями и матерей с эпизодами беспорядочного образа жизни в прошлом.
Если некоторым матерям нельзя доверять новорожденного, будут ли им доверять беременность, когда появится альтернативный метод гестации? Может ли мать, непригодная для воспитания собственного ребенка, считаться ответственным инкубатором? Если будущее деторождения означает выбор между эктогенезом и естественной беременностью, наше отношение к тому, что «естественно», изменится навсегда. Легко представить будущее, где в «помощь», которую уже сейчас предлагают работодатели в Кремниевой долине и за ее пределами, когда персонал может заморозить свои яйцеклетки и сосредоточиться на работе в самые продуктивные годы карьеры, войдет пункт по выращиванию младенца в искусственной матке, чтобы не прерываться на время беременности и родов. Использование настоящей матки в человеческом теле в итоге может стать признаком низкого статуса, бедности, неблагополучной жизни, незапланированной беременности или клеймом потенциально опасной сторонницы естественных родов — точно так же, как сегодня мы относимся к приверженкам «свободных родов», которые решают производить ребенка на свет без всякого медицинского участия во время или после беременности.
«Естественные» роды сами по себе могут стать безответственным и легкомысленным выбором. Сегодня самая главная экзистенциальная угроза для нерожденных младенцев исходит не от наркотиков, алкоголя или женщин, «непригодных» для беременности, а от матерей, не желающих детей. Эктогенез сможет «спасти» абортированный плод: его можно пересадить в искусственную матку и передать желающим родителям.
В Великобритании границы аборта привязаны к жизнеспособности вне утробы — вот почему в 1990 году они снизились с 28 до 24 недель. Полный эктогенез значит, что жизнеспособным будет любой плод, даже эмбрионы, и у любого неродившегося ребенка может появиться право на жизнь. Даже частичный эктогенез перевернет дебаты об аборте с ног на голову. Мы считаем аборт одним выбором — решением избавиться от плода, но на самом деле их два: решение не вынашивать младенца и решение прервать его жизнь. Эктогенез впервые разведет и подчеркнет их. Если тело женщины перестанет быть инкубатором, аборт будет отвечать требованиям как защиты свободы, так и защиты жизни. Государства позволят женщинам выбирать, что будет с их телами, в то же время запрещая прерывать жизнь плода.
С чего мать должна в одиночку решать, умереть ли ребенку, если его могут спасти технологии? Феминистка-активистка и писательница Сорайя Чемали задумалась об этом за пять лет до того, как на мировую сцену вышли живыми и невредимыми ягнята из мешков. В эссе 2012 года для Rewire.News она писала, что «…неотъемлемое от текущих дебатов противоречие — между правами женщины и государственным интересом к плоду — исчезнет, как только женщина и плод смогут стать независимыми друг от друга моментально и безопасно. Мужчины и женщины станут равны в репродуктивном выборе, и женщины потеряют примат, каким сейчас наделены благодаря беременности».
Ее текст кончается мрачным ударом по этому праву на выбор: «Настоящее антиутопическое будущее наступит, когда мы с ностальгией оглянемся на короткий период, в который дело Роу против Уэйда (историческое решение Верховного суда США 1973 года о законности абортов до 28-й недели беременности) было релевантно и являлось пиком репродуктивной свободы для женщин».
Сорайя сейчас в Вашингтоне, и мы созваниваемся по телефону. Я начинаю с вопроса о том, что она подумала, когда впервые услышала о биомешке, но в ответ слышу долгий и мрачный смех. «Я довольно цинично и откровенно пессимистично отношусь к любой технологии, обещающей стать поистине подрывной или революционной. Всегда смеюсь, когда футуристы-технологи — до сих пор по большей части мужчины, по большей части белые, по большей части из элиты — объявляют, будто их идея прогрессивная и подрывная, ведь это они так активно поддерживают патриархат. Это они порождают столько подспудных неравенств в обществе. Это как объяснять рыбе, что такое вода».
Даже несмотря на успехи Мэтта Кемпа в WIRF и команды изобретателей биомешка, Сорайя с осторожностью говорит, что, по ее мнению, полный эктогенез станет жизнеспособной и распространенной технологией репродукции только через несколько поколений.
«Это невероятно сложно, и я все еще думаю, что эктогенез займет больше времени, чем некоторые думают, — говорит она. — Но я согласна с тем, что это неизбежно». Это просто очередной шаг в фрагментации материнства. Технология искусственной матки — разработанная по большей части мужчинами — позволит женщинам стать не более чем поставщицами половых клеток, такими же отстраненными от своих созревающих младенцев, как и мужчины. Сорайя говорит, что ультразвук показывает, насколько уже сейчас женские тела считаются побочными в репродуктивной медицине.
«Я много лет говорю: не показывайте фотографии гребаных развивающихся плодов, если не показываете все тело женщины. Я понимаю, при беременности теряешь голову, но такая вот я ужасная феминистка-кайфоломка. Я говорю: «О, как мило, а почему бы не сделать снимок побольше». Ультразвук совершенно осознанно разработали так, чтобы показывать плод в виде планеты в бездне, в вакууме, в контейнере, в банке. На фоне черных обоев. Полностью стирая женщину, чье тело дает жизнь».
Мне сложно представить, чтобы у нас прижился ультразвук в полный рост, но я понимаю, к чему ведет Сорайя. Флейк говорил, что один из главных продающих моментов биомешка в том, что он позволит обоим родителям видеть своего ребенка в реальном времени, раз он находится вне тела матери. А как только матери и отцы станут равно удалены от младенцев, они получат на них равные права — и это равенство будет основано на том, что женщины лишатся своей детородной силы. Сорайя согласна, что у эктогенеза есть потенциал освободить женщин от бремени, ныне сопровождающего материнство. «Меня разрывает эта дилемма, — говорит она. — Думаю: «Ну наконец-то, можно уже покончить с культурным гнетом мышления, будто это неотъемлемо от нашей природы, будто это неизбежная первичная роль для всех женщин?» И эта мысль освобождает». Но при этом Сорайя — «преданный фанат литературных антиутопий, особенно феминистских», так что видит у этой технологии мрачный потенциал лишить женщин прав. Даже в самых мизогинических обществах, говорит она, женщин ценят за способность вынашивать детей, «по крайней мере, пока есть шанс, что родится сын». Сделав воспроизводство равным, эктогенез отнимет универсальную силу, что бесспорно есть у всех женщин и нет ни у одного мужчины.
Источник
Перенос эмбрионов в матку: один, два или три
Вопрос о том, сколько эмбрионов переносить в полость матки, всегда решается совместно – врачом и клиентами. Но помимо желания здесь играют роль и другие факторы.
Возраст. Самый главный фактор. По законодательству нашей страны женщинам в возрасте до 35 лет в рамках одного протокола можно переносить не более двух эмбрионов, женщинам после 35 лет – не более трех.
Количество попыток ЭКО. Если в анамнезе уже было три или более неудачных протокола, врачи могут перенести в матку сразу 3 эмбриона вне зависимости от возраста клиентки.
Наличие сопутствующих заболеваний. Если у женщины есть серьезные хронические болезни или другие патологии, врачи не рекомендуют переносить больше одного эмбриона. Такая тактика помогает снизить риски обострения и прогрессирования заболеваний.
Также важную роль в выборе играют:
- анамнез предыдущих беременностей и родов.
- операции на матке (в матку с рубцом не стоит переносить более одного эмбриона).
- телосложение и вес женщины
Важно: если риски осложнений при подсадке двух и более эмбрионов высоки, лучше все же уменьшить их количество. По статистике, пересадка одного эмбриона приводит к наступлению беременности в 50-60% случаев, а перенос двух повышает эту цифру на 15%. Но в тоже время серьезно возрастают и риски, связанные с многоплодной беременностью. Поэтому прежде чем выбрать то или иное количество эмбрионов, нужно тщательно взвесить все «за» и «против».
Источник
Оплодотворение яйцеклеток и культивирование эмбрионов
Экстракорпоральное оплодотворение — это метод лечения бесплодия, при котором оплодотворение яйцеклеклетки и начальные этапы развития эмбриона происходят вне организма женщины.
Показания для лечения бесплодия помощью ЭКО :
- Отсутствие проходимости маточных труб
- Различные формы эндометриоза
- Высокий риск генетических заболевания у ребенка, требующий проведения преимплантационной генетической диагностики эмбриона перед его переносом
- Высокий риск хромосомной патологии плода, ассоциированный со старшим репродуктивным возрастом родителей (страше 35 лет)
- Мужское бесплодие
- Эндокринное бесплодие.
Протокол ЭКО состоит из целого ряда последовательных этапов:
- Стимуляция суперовуляции/ мониторинг роста фолликула в естественном цикле
- Трансвагинальная пункция фолликулов. Этап извлечения яйцеклеток из яичников женщины.
- Проведение опдлодотворения яйцеклеток сперматозоидами партнера/донора спермы
- Культивирование эмбрионов
- Перенос эмбрионов
- Возможно проведение криоконсервации эмбрионов с целью отсроченного переноса, например, после получения результатов преимплантационной генетической диагностики, или проведения программы отсроченного материнства, программы сохранения фертильности, когда перенос эмбринов может быть проведен спустя месяцы или годы после получения эмбрионов.
Гаметы (ооциты и сперматозоиды) получают от биологических родителей или из банка доноров. Яйцеклетки извлекают из яичников женщины методом пункции фолликулов в ходе их естественного созревания. Но, как правило, в программах ВРТ используют медикаментозное стимулирование для получения достаточного количества ооцитов. Оплодотворение происходит в лабораторных условиях под контролем специалистов. В некоторых протоколах даже слияние сперматозоида и яйцеклетки контролируется эмбриологом (ICSI). После in vitro оплодотворения зиготы переносят в специальную, обогащенную альбумином, питательную среду для нормального предимплантационного развития эмбрионов. Процесс выращивания эмбриона в условиях in vitro называют культивированием.
В каких условиях культивируют эмбрионы
Ключевым моментом эмбриологического этапа программы ЭКО для предимплантационных эмбрионов человека, развивающихся in vitro, является создание максимально приближенных условий к условиям in vivo.
Эмбрионы культивируются в инкубаторах. Обязательными условиями для in vitro культивирования эмбрионов являются:
- температура 37 градусов Цельсия;
- рН культуральной среды, стабильность которой обеспечивается слоем минерального масла сверху культуральной среды и концентрацией СО2
- определенное содержание углекислого газа (5,5%-6.0% в зависимости от выбранной культуральной среды), азота и кислорода (не более 5%).
В инкубаторе находятся яйцеклетки перед оплодотворением, полученные в результате пункции фолликулов или после разморозки ооцитов. Все процессы, включая оплодотворение, дробление, бластуляция также проходят в условиях инкубатора.
Как долго эмбрионы культивируются в инкубаторе
После оплодотворения культивирование эмбрионов может продолжаться в условиях in vitro до 5-6 дней. Продолжительность зависит от нескольких факторов:
- количество полученных ооцитов/эмбрионов;
- возраст и состояние здоровья пациента/реципиента;
- необходимость проведения ПГТ-А, ПГТ-М
Если получено и оплодотворено небольшое количество яйцеклеток (1-2), то перенос можно проводить на третий день развития эмбрионов. Женщинам, у которых в анамнезе уже есть 1-2 попытки ЭКО и есть достаточное количество эмбрионов, чтобы выбрать лучший эмбрион для переноса в полость матки, рекомендуется подсаживать эмбрионы на пятый день развития. Если предполагается проведение предимплантационного генетического тестирования (ПГТ), то эмбрионы культивируются до 5-6 суток с целью проведения биопсии трофэктодермы на стадии бластоцисты.
Какие среды используются для культивирования эмбрионов
От культуральной среды зависит правильное развитие и продолжительность культитвирования эмбрионов. Чаще всего используют 2 типа сред:
- двух-шаговая культуральная среда (sequential medium): используется с 1-3 день с заменой среды на 3-5 день культивирования:
- в состав среды для культивирования с 1-го по 3-й день развития входят аминокислоты, белки, витамины, лактат кальция. Среда имеет определенный состав и уровень pH, который обеспечивает правильное развитие эмбриона на ранних стадиях дробления;
- для пролонгированного культивирования с 3-го до 5-6-го дня используют среды с глюкозой, аминокислотами, таурином, комплексом витаминов, альбумином. Состав элементов поддерживает рост и развитие эмбриона до стадии бластоцисты, максимально укрепляет его, обеспечивает высокую жизнеспособность и готовность к имплантации.
- универсальные, одношаговые среды (one step medium), подходящие для культивирования с 1-5 день развития эмбрионов без замены среды.
Этапы роста и развития эмбриона в процессе культивации
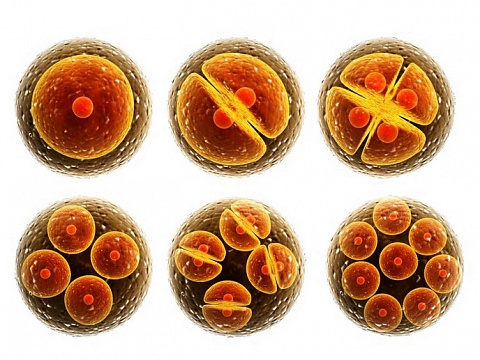
После оплодотворения зигота проходит ряд изменений, свидетельствующих о правильном развитии:
- на следующий день после оплодотворения клетка исследуется на наличие пронуклеусов — клеточных ядер родительских гамет. Наличие двух пронуклеусов (2PN) -нормальное оплодотоворение. Зиготы с нормальным оплодотворением отбираются и культивируются дальше. Если пронуклеусы не просматриваются под микроскопом, яйцеклетка считается не оплодотворенной (0PN). Аномальным оплодотворением считается наличие 3-х (ЗPN) и более пронуклеусов. Яйцеклетки не оплодотворенные и с анамальным оплодотворением не культивируются.
- во второй день развития эмбрион проходит 2 последовательных митотических деления дробления и, в норме, имеет 4 бластомера расположенных в форме тетраэдра, равных по размеру, одноядерных, без фрагментации (Grade 1) (по классификации 4A (цифра 4 обозначает количество бластомеров, буква А -бластомеры хорошего качества ), (Alpha Scientists in Reproductive Medicine and ESHRE Special Interest Group of Embryology, 2011)
- для 3-го дня развития оптимальным считается 8-клеточный эмбрион с равными по размеру, одноядерными бластомерами, без фрагментации. По международной классификации обозначение 8А (Grade 1)
- на четвертый день эмбрион формирует морулу, состоит из 12- 16 плотно прилегающих друг к другу бластомеров, начинается первая клеточная дифференциация: наружные клетки морулы в дальнейшем будут формировать трофэктодерму (ТЭ), внутренние клетки-внутреннюю клеточную массу (ВКМ) При естественной беременности на этой стадии происходит мигрирование морулы из маточных труб в матку.
- на пятый и шестой день предимплантационного развития эмбриона формируется бластоцита — сфера с внутренней полостью (бластоцель), выстланная рядом клеток трофэктодермы (трофобласт, из которого в дальнейшем формируются различные экстраэмбриональные структуры) и компактная группа клеток внутренней клеточной массы (эмбриобласт- клетки самого зародыша). Перенос бластоциты высокоэффективен, каждая вторая подсадка заканчивается беременностью.
Дольше 6-7 дней эмбрионы не культивируют, их необходимо либо перенести в полость матки реципиента, либо подвергнуть криоконсервации.
Что такое протокол культивирования эмбрионов
Протокол культивирования — это документ, в котором эмбриолог отражает все стадии развития эмбрионов по дням. В протоколе культивирования указываются генетические родители (пациенты/доноры) и реципиенты (пациенты/суррогатная мать). Отмечается количество полученных в результате пункции ооцитов, их зрелость, наличие отклонений цитоплазмы и оболочки ооцитов, а также заносится спермограмма. Далее вносятся результаты оплодотворения и культивирования, морфологические характеристики каждого эмбриона, фиксируются эмбрионы которым проведена биопсия, сделан перенос в полость матки или проведена криоконсервация, отмечаются условия культивирования, какие среды были использованы.
В МЦРМ эмбриологи действуют по четко прописанным протоколам/алгоритмам. . Алгоритмы отработаны, прописаны в СОП (Стандартное Описание Процедуры), что исключает возможность какой-либо ошибки. На каждом этапе работы эмбриолога с биологическим материалом пациентов существует «контроль качества», соответствующий строгим международным критериям. Эмбриологи нашего центра работают в лаборатории, построенной по специальному проекту, оснащенной новым современным оборудованием, с использованием качественных культуральных сред и вспомогательных материалов, используя в своей практике современные методы и эффективные разработки, позволяющие достичь высоких результатов.
Источник