Достижения биотехнологии
Биотехнология – это наука, изучающая возможность использовать живые организмы или продукты их жизнедеятельности для решения определенных технологических задач.
С помощью биотехнологий, происходит обеспечение определенных человеческих потребностей, например: разработка медицинских препаратов, модификация или создание новых видов растений и животных, что увеличивает качество пищевых продуктов.
Биотехнология в современной медицине
Биотехнология, как наука, зарекомендовала себя в конце ХХ века, а именно в начале 70-х годов. Все началось с генетической инженерия, когда ученые смогли перенести генетический материал из одного организма к другому без осуществления половых процессов. Для этого была использовано рекомбинантная ДНК или рДНК. Такой метод применяется для изменения или улучшения определенного организма.
Чтобы создать молекулу рДНК нужно:
- извлечь молекулу ДНК из клетки животного или растения;
- обработать изолированную клетку и плазмиду, а затем смешать их;
- затем, измененная плазмида переносится в бактерию, а та в свою очередь приумножает копии информации, что были внесены в нее.
Медицинские биотехнологии подразделяются на 2 большие группы:
- Диагностические, которые, в свою очередь, бывают: химическими (определение диагностических веществ и параметров обмена); физическими (определение физических полей организма);
- Лечебные.
К медицинской биотехнологии относят такие производственные процессы, в ходе которых создаются биообъекты или вещества медицинского назначения. Это ферменты, витамины, антибиотики, отдельные микробные полисахариды, которые могут применяться как самостоятельные средства или как вспомогательные вещества при создании различных лекарственных форм, аминокислоты.
Так, методы биотехнологий применяются:
- для производства человеческого инсулина путем использования генно-модифицированных бактерий;
- для создания эритропоэтина (гормона, стимулирующего образование эритроцитов в костном мозге.
Медицинская генетика в будущем сможет не только предотвращать появление на свет неполноценных детей путем диагностирования генетических заболеваний, но и проводить пересадку генов для решения существующей проблемы.
Биотехнология в будущем даст человечеству огромные возможности не только в медицине, но и в других направлениях современных наук.
Биотехнологии в современной науке
Биотехнологии в современной науке несет огромную пользу. За счет открытия генной инженерии стало возможным выведения новых сортов растений и пород животных, которые принесут пользу сельскому хозяйству.
Изучения биотехнологии связано не только лишь с науками биологического направления. В микроэлектронике разработаны ион-селективные транзисторы на основе полевого эффекта (HpaI).
Биотехнология необходима для повышения нефтеотдачи нефтяных пластов. Наиболее развитым направлением является использование биотехнологии в экологии для очистки промышленных и бытовых сточных вод.
В развитие биотехнологии внесли свой вклад многие другие дисциплины, именно поэтому биотехнологии стоит отнести к комплексной науке.
Еще одной причиной активного изучения и усовершенствования знаний в биотехнологии стал вопрос в недостатке (или будущем дефиците) социально-экономических потребностей.
В мире существуют такие проблемы, как:
- нехватка пресной или очищенной воды (в некоторых странах);
- загрязнение окружающей среды различными химическими веществами;
- дефицит энергетического ресурса;
- необходимость усовершенствования и получения совершенно новые экологически чистых материалов и продуктов;
- повышение уровня медицины.
Ученые уверенны, что решить эти и многие другие проблемы возможно при помощи биотехнологии.
Основные типовые технологические приемы современной биотехнологии
Биотехнологию можно выделить не только как науку, но еще и как сферу практической деятельности человека, которая отвечает за производство разного вида продукции при участии живых организмов или их клеток.
Теоретической основой для биотехнологии в свое время стала такая наука, как генетика, это случилось в ХХ веке. А вот практически биотехнология основывалась на микробиологической промышленности.
Микробиологическая промышленность в свою очередь получила сильный толчок в развитии после открытия и активного производства антибиотиков.
Объектами, с которыми работает биотехнология, являются вирусы, бактерии, различные представители флоры и фауны, грибы, а также органоиды и изолированные клетки.
Наглядная биотехнология. Генная и клеточная инженерия
Генетическая и клеточная инженерия в сочетании с биохимией – это основные сферы современной биотехнологии.
Клеточная инженерия – выращивание в специальных условиях клеток различных живых организмов (растений, животных, бактерий), разного рода исследования над ними (комбинация, извлечение или пересадка).
Самой успешной считается клеточная инженерия растений. При помощи клеточной инженерии растений стало возможным ускорение селекционных процессов, что позволяет выводить новые сорта сельхоз культур. Теперь выведение нового сорта сократилось от 11 лет до 3-4.
Генетическая (или генная) инженерия – отдел молекулярной биологии, в котором занимаются изучением и выделением генов из клеток живых организмов, после чего над ними проводятся манипуляции для достижения определенной цели. Главными инструментами, которые используются в генной инженерии, являются ферменты и векторы.
Биотехнологии клонирования
Клонирование – это процесс получения клонов (то есть потомков полностью идентичных прототипу). Первый опыт клонирования был проведен на растениях, которые клонировались вегетативным путем. Каждое отдельное растение, которое получилось вследствие клонирования, называлось клоном.
В процессе развития генетики это термин начали применять не только к растениям, но и к генетическому выведению бактерий.
Уже в конце ХХ века ученые начали активное обсуждение клонирования человека. Таким образом, термин «клон» стал употребляться в СМИ, а позже и в литературе и искусстве.
Что касается бактерий, то у них клонирование – это практически единственный способ размножения. Именно «клонирование бактерий» употребляется в том случаи, когда процесс искусственный и им управляет человек. Этот термин не касается естественного размножения микроорганизмов.
Генетическая инженерия
Генная инженерия – это искусственные изменения в генотипе микроорганизма, вызванное вмешательством человека, для получения культур с необходимыми качествами.
Генная инженерия занимается исследованиями и изучением не только микроорганизмов, но и человека, активно изучает заболевания, связанные с иммунной системой и онкологией.
Клеточная биотехнология растений
Клеточная биотехнология основывается на применении клеток, тканей и протопластов. Чтобы успешно управлять клетками, необходимо отделить их от растения и создать им все необходимые условия для успешного существования и размножения вне организма растения. Такой метод выращивания и размножения клеток носит название «культуры изолированных тканей» и получил особое значение из-за возможности применения в биотехнологии.
Биотехнологии в современном мире и жизни человека
Потенциал, который открывает биотехнология для человека, велик не только в фундаментальной науке, но и в других сферах деятельности и областях знаний. При использовании биотехнологических методов стало возможно массовое производство всех необходимых белков.
Значительно проще стали процессы получения продуктов ферментации. В будущем биотехнологии позволят улучшать животных и растений. Учеными рассматриваются варианты борьбы с наследственными болезнями при помощи генной инженерии.
Генная инженерия, как основное направление в биотехнологии, значительно ускоряет решение проблемы продовольственного, аграрного, энергетического и экологического кризисов.
Самое большее влияние биотехнология оказывает на медицину и фармацевтику. Прогнозируется, что в будущем станет возможным диагностика и лечение тех заболеваний, которые имеют статус «неизлечимых».
Этические аспекты некоторых достижений в биотехнологии
После того, как стало известно, что некоторые научные лаборатории не только проводили опыты на человеческих эмбрионах, но и пытались произвести клонирование людей – пошла волна бурного обсуждения этого вопроса не только среди ученых, но и среди обычных людей.
В биотехнологии можно выделить две этические проблемы, связанные с клонированием человека:
- терапевтическое клонирование (культивация человеческих эмбрионов для применения их клеток с целью лечения);
- репродуктивное клонирование (создание человеческих клонов).
Современные достижения и проблемы биотехнологии
При помощи биотехнологии было и будет получено огромное количество продуктов для здравоохранения, сельского хозяйства продовольственной и химической промышленности. Стоит упомянуть, что многие из продуктов никаким другим способом не могли быть получены.
Что касается проблем, так основным образом – это этические аспекты, связанные с тем, что общество отрицает и считает негативным клонирование человека или человеческого эмбриона.
Современное состояние и перспективы биотехнологии
В биотехнологии активно начала развиваться отрасль микробного синтеза ценных для человечества веществ. Это может повлечь за собой смену распределения роли продовольственной базы, основанной на растениях и животных, в сторону микробного синтеза.
Получение экологически чистой энергии при помощи биотехнологий – еще одно важное и перспективное направление в науке.
Компании, разрабатывающие новые биотехнологии
Журнал «Forbes» представил список самых инновационных компаний мира по разработке биотехнологий, в него вошли такие компании, как: «Genentech», «Novartis International AG», «Merck & Co», «Pfizer», «Sanofi», «Perrigo». Все эти компании напрямую связаны с фармацевтикой и развиваются именно в этом направлении.
Многие из компаний успешно принимают активное участие в развитии российского рынка биотехнологий:
- «Novartis International AG» – компания занимается выведением вакцин и производством препаратов в сфере онкологии, одно из предприятий работает в СПб.
- «Pfizer» – производит безрецептурные препараты в разных отраслях медицины. Pfizer уже несколько лет реализует в России программу «Больше, чем образование» по соглашениям с МГУ им. М.В. Ломоносова и Санкт-Петербургской государственной химико-фармацевтической академией.
- «Sanofi» – компания занимается производством препаратов для лечения сахарного диабета и склероза. В России успешно работает уникальное предприятие компании – завод полного цикла по производству инсулинов «Санофи-Авентис Восток».
В России особая роль отводится Кластеру биомедицинских технологий Инновационного центра «Сколково», ОАО «РВК» и ОАО «Роснано». Фармацевтическими и медицинскими биотехнологиями занимаются компании ОАО «Акрихин», ООО «Герофарм», НПФ «Литех». Центр высоких технологий «Химрар» объединяет высокотехнологичные организации, ведущие разработки и производство инновационных 14 компаний, которые занимаются разработкой лекарственных препаратов на основе новейших «постгеномных» технологий.
Помимо этого, существуют и молодые стартапы, разрабатывающие новые биотехнологии:
- «3Д Биопринтинг Солюшенс» на основе трёхмерной биопечати создает органы из стволовых клеток пациента;
- «БиоМикроГели» предлагает разработки по очистке воды и почвы с помощью микрогелей.
- биомедицинский холдинг «Атлас» проводит анализ микробиоты организма в рамках проекта «OhmyGut».
Источник
Тканевая инженерия — окно в современную медицину
19 октября 2011
Тканевая инженерия — окно в современную медицину
В перспективе тканевая инженерия, если и не приведет к бессмертию, то уж точно сделает решение многих современных проблем медицины более чем реальным.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Петр I мечтал «прорубить окно в Европу», а ученые нашего времени — окно в современную медицину. Сочетание «медицина + биотехнология» нашло свое отражение в тканевой инженерии — технологии, открывающей возможность восстановления утраченных органов без трансплантации. Методы и результаты тканевой инженерии поражают: это получение живых (а не искусственных!) органов и тканей; регенерация тканей; печать кровеносных сосудов на 3D-принтере; использование «тающих» в организме хирургических шовных нитей и многое другое.
Конкурс «био/мол/текст»-2011
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2011 в номинации «Лучшая обзорная статья».
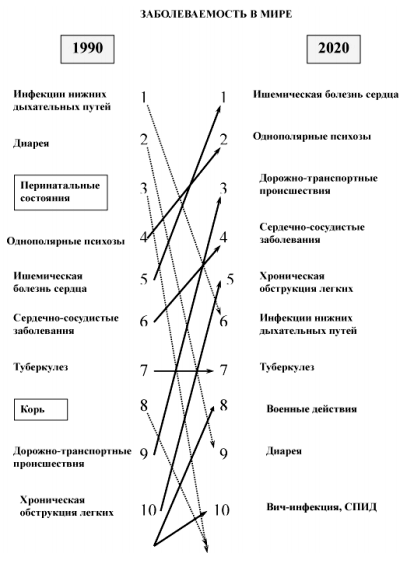
В последние десятилетия стали отчетливо проявляться тревожные тенденции старения населения, роста количества заболеваний и инвалидизации людей трудоспособного возраста, что настоятельно требует освоения и внедрения в клиническую практику новых, более эффективных и доступных методов восстановительного лечения больных. На рисунке 1 показано, как изменяется структура заболеваний в настоящее время.
Рисунок 1. Мировая динамика частоты заболеваний.
На сегодняшний день наука и техника предлагает несколько альтернативных путей восстановления или замены поврежденных или пораженных патологией тканей и органов:
- трансплантацию;
- имплантацию;
- тканевую инженерию.
В рамках данной статьи мы подробнее остановимся на возможностях и перспективах тканевой инженерии.
Тканевая инженерия — современная инновационная технология
Принципиально новый подход — клеточная и тканевая инженерия — является последним достижением в области молекулярной и клеточной биологии. Этот подход открыл широкие перспективы для создания эффективных биомедицинских технологий, с помощью которых становится возможным восстановление поврежденных тканей и органов и лечение ряда тяжелых метаболических заболеваний человека.
Цель тканевой инженерии — конструирование и выращивание вне организма человека живых, функциональных тканей или органов для последующей трансплантации пациенту с целью замены или стимуляции регенерации поврежденных органа или ткани. Иными словами, на месте дефекта должна быть восстановлена трехмерная структура ткани.
Важно отметить, что обычные имплантаты из инертных материалов могут устранить только физические и механические недостатки поврежденных тканей, — в отличие от тканей, полученных методом инженерии, которые восстанавливают, в том числе, и биологические (метаболические) функции. То есть, происходит регенерация ткани, а не простое замещение ее синтетическим материалом.
Однако для развития и совершенствования методов реконструктивной медицины на базе тканевой инженерии необходимо освоение новых высокофункциональных материалов. Эти материалы, применяемые для создания биоимплантатов, должны придавать тканеинженерным конструкциям характеристики, присущие живым тканям:
- способность к самовосстановлению;
- способность поддерживать кровоснабжение;
- способность изменять строение и свойства в ответ на факторы окружающей среды, включая механическую нагрузку.
Клетки и матриксы — основа основ для тканевой инженерии
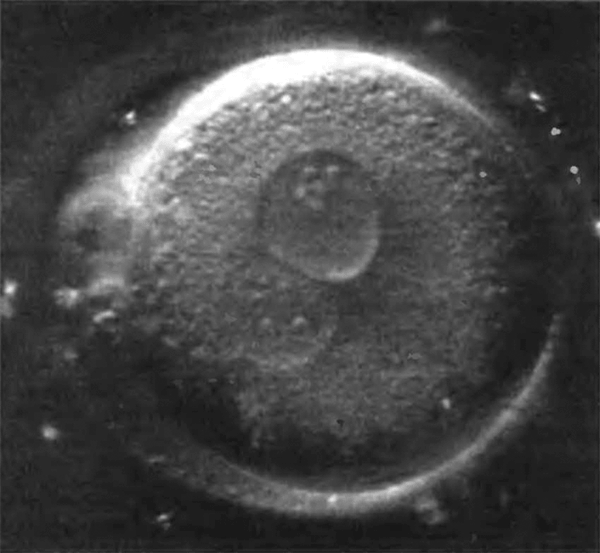
Наиболее важным элементом успеха является наличие необходимого количества функционально активных клеток, способных дифференцироваться, поддерживать соответствующий фенотип и выполнять конкретные биологические функции. Источником клеток могут быть ткани организма и внутренние органы. Возможно использование соответствующих клеток от пациента, нуждающегося в реконструктивной терапии, или от близкого родственника (аутогенных клеток). Могут быть использованы клетки различного происхождения, в том числе первичные (рис. 2) и стволовые клетки (рис. 3).
Рисунок 2. Первичная клетка человека.
библиотека Федерации Киокушинкай г. Южноуральска
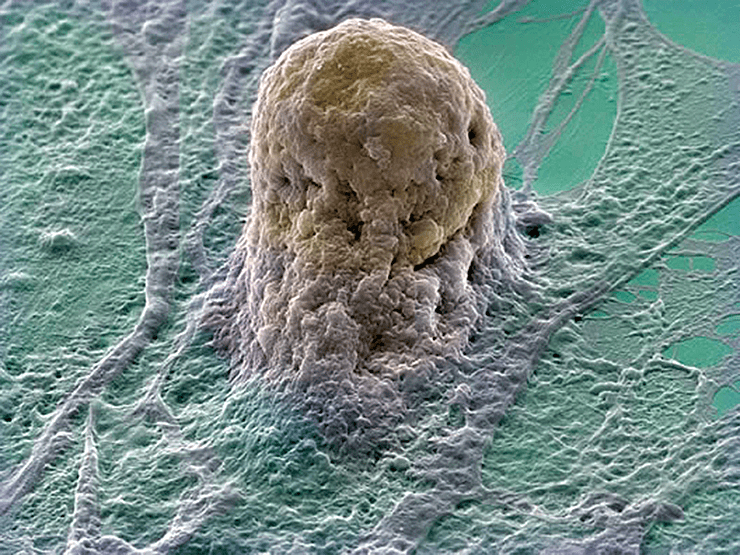
Рисунок 3. Стволовая клетка человека.
Первичные клетки — это зрелые клетки определенной ткани, которые могут быть взяты непосредственно от организма-донора (ex vivo) хирургическим путем. Если первичные клетки взяты у определенного организма-донора, и впоследствии необходимо имплантировать эти клетки ему же в качестве реципиента, то вероятность отторжения имплантированной ткани исключается, поскольку присутствует максимально возможная иммунологическая совместимость первичных клеток и реципиента. Однако первичные клетки, как правило, не способны делиться — их потенциал к размножению и росту низок. При культивировании таких клеток in vitro (посредством тканевой инженерии) для некоторых типов клеток возможна дедифференцировка, то есть потеря специфических, индивидуальных свойств. Так, например, хондроциты, вводимые в культуру вне организма, часто продуцируют фиброзный, а не прозрачный хрящ.
Поскольку первичные клетки не способны делиться и могут потерять свои специфичные свойства, возникла необходимость альтернативных источников клеток для развития технологий клеточной инженерии. Таковой альтернативой стали стволовые клетки.
Рисунок 4. Биокерамические изделия из ортофосфатов кальция.
Стволовые клетки — недифференцированные клетки, которые имеют способность к делению, самообновлению и дифференцировке в различные типы специализированных клеток под воздействием конкретных биологических стимулов (см.: «Была клетка простая, стала стволовая» [3]). Стволовые клетки подразделяются на «взрослые» [2] и «эмбриональные». Эмбриональные стволовые клетки образуются из внутренней клеточной массы развития зародыша на ранней стадии, а взрослые — из тканей взрослого организма, пуповины или даже плодных тканей. Однако существует этическая проблема, связанная с неизбежным разрушением человеческого эмбриона при получении эмбриональных стволовых клеток [4]. Поэтому предпочтительнее «добыча» клеток из тканей взрослого организма. Так, например, в 2007 году Шинью Яманакой (Shinya Yamanaka) из Киотского университета Японии были открыты индуцированные плюрипотентные стволовые клетки (ИПСК), получаемые из покровных тканей человека (в основном, из кожи). ИПСК открывают поистине невиданные возможности для регенеративной медицины, хотя, прежде чем они всерьез войдут в медицинскую практику, предстоит решить еще немало проблем (см.: «Снежный ком проблем с плюрипотентностью» [5]).
Для направления организации, поддержания роста и дифференцировки клеток в процессе реконструкции поврежденной ткани необходим специальный носитель клеток — матрикс, представляющий из себя трехмерную сеть, похожую на губку или пемзу (рис. 4). Для их создания применяют биологически инертные синтетические материалы, материалы на основе природных полимеров (хитозан, альгинат, коллаген) и биокомпозиты. Так, например, эквиваленты костной ткани получают путем направленной дифференцировки стволовых клеток костного мозга, пуповинной крови или жировой ткани в остеобласты, которые затем наносят на различные материалы, поддерживающие их деление (например, донорскую кость, коллагеновые матрицы и др.).
«Фирменная» стратегия тканевой инженерии
На сегодняшний день одна из стратегий тканевой инженерии такова:
- Отбор и культивирование собственных или донорских стволовых клеток.
- Разработка специального носителя для клеток (матрицы) на основе биосовместимых материалов.
- Нанесение культуры клеток на матрицу и размножение клеток в биореакторе со специальными условиями культивирования.
- Непосредственное внедрение тканеинженерной конструкции в область пораженного органа или предварительное размещение в области, хорошо снабжаемой кровью, для дозревания и формирования микроциркуляции внутри конструкции (префабрикация).
Матриксы через некоторое время после имплантации в организм хозяина полностью исчезают (в зависимости от скорости роста ткани), а в месте дефекта останется только новая ткань. Также возможно внедрение матрикса с уже частично сформированной новой тканью («биокомпозит»). Безусловно, после имплантации тканеинженерная конструкция должна сохранить свои структуру и функции в течение периода времени, достаточного для восстановления нормально функционирующей ткани в месте дефекта, и интегрироваться с окружающими тканями. Но, к сожалению, идеальные матриксы, удовлетворяющие всем необходимым условиям, пока не созданы.
Кровеносные сосуды из принтера
Перспективные тканеинженерные технологии открыли возможность лабораторного создания живых тканей и органов, но перед созданием сложных органов наука пока бессильна. Однако сравнительно недавно ученые под руководством доктора Гунтера Товара (Gunter Tovar) из Общества Фраунгофера в Германии сделали огромнейший прорыв в сфере тканевой инженерии — они разработали технологию создания кровеносных сосудов. А ведь казалось, что капиллярные структуры создать искусственно невозможно, поскольку они должны быть гибкими, эластичными, малой формы и при этом взаимодействовать с естественными тканями. Как ни странно, но на помощь пришли производственные технологии — метод быстрого прототипирования (другими словами, 3D-печать). Подразумевается, что сложная трехмерная модель (в нашем случае кровеносный сосуд) печатается на трехмерном струйном принтере с использованием специальных «чернил» (рис. 5).
Рисунок 5. Технология «печати» искусственного кровеносного сосуда.
Принтер наносит материал послойно, и в определенных местах слои соединяются химически. Однако заметим, что для мельчайших капилляров трехмерные принтеры пока недостаточно точны. В связи с этим был применен метод многофотонной полимеризации, используемый в полимерной промышленности. Короткие интенсивные лазерные импульсы, обрабатывающие материал, так сильно возбуждают молекулы, что они взаимодействуют друг с другом, соединяясь в длинные цепочки. Таким образом, материал полимеризуется и становится твердым, но эластичным, как естественные материалы. Эти реакции настолько управляемы, что с их помощью можно создавать мельчайшие структуры по трехмерному «чертежу».
А для того, чтобы созданные кровеносные сосуды могли состыковаться с клетками организма, при изготовлении сосудов в них интегрируют модифицированные биологические структуры (например, гепарин) и «якорные» белки. На следующем этапе в системе созданных «трубочек» закрепляются клетки эндотелия (однослойный пласт плоских клеток, выстилающий внутреннюю поверхность кровеносных сосудов) — для того, чтобы компоненты крови не приклеивались к стенкам сосудистой системы, а свободно транспортировались по ней.
Однако прежде чем действительно можно будет имплантировать выращенные в лаборатории органы с собственными кровеносными сосудами, пройдет еще какое-то время.
Давай, Россия, давай вперед!
Без ложной скромности скажем, что и в России создана научная основа для практического применения биомедицинских материалов нового поколения. Интересную разработку предложила молодой учёный из Красноярска Екатерина Игоревна Шишацкая (рис. 6) — растворимый биосовместимый полимер биопластотан [7]. Суть своей разработки она объясняет просто: «в настоящее время практические медики испытывают большой дефицит материалов, способных заменить сегменты человеческого организма. Нам удалось синтезировать уникальный материал, который в состоянии заменить элементы органов и тканей человека». Разработка Екатерины Игоревны найдет применение, прежде всего, в хирургии. «Самое простое — это, например, шовные нити, сделанные из нашего полимера, которые растворяются после того, как зарастает рана, — говорит Шишацкая. — Также можно делать специальные вставки в сосуды — стенты. Это маленькие полые трубки, которые используют, чтобы расширить сосуд. Через некоторое время после операции сосуд восстанавливается, а полимерный заменитель растворяется» [8].
Рисунок 6. Лауреат премии Президента РФ Екатерина Игоревна Шишацкая.
Первый опыт трансплантации тканеинженерной конструкции в клинике
Рисунок 7. Паоло Маккиарини, мастер-класс которого «Клеточные технологии для тканевой инженерии и выращивания органов» прошел в Москве в 2010 году.
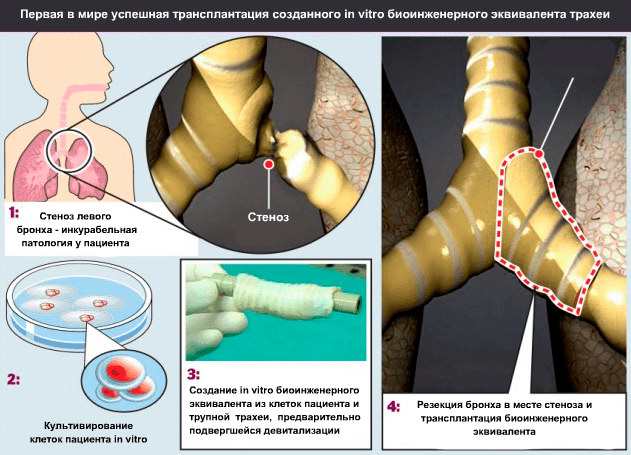
Осенью 2008 года руководитель клиники Университета Барселоны (Испания) и Медицинской школы Ганновера (Германия) профессор Паоло Маккиарини (Paolo Macchiarini; рис. 7) провел первую успешную операцию по трансплантации биоинженерного эквивалента трахеи пациентке со стенозом главного левого бронха на протяжении 3 см (рис. 8) [11].
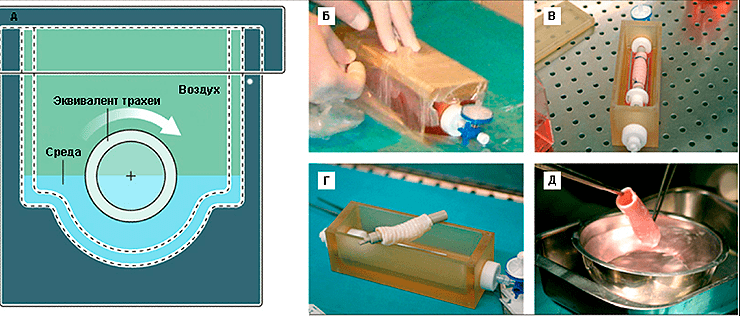
В качестве матрикса будущего трансплантата был взят сегмент трупной трахеи длиной 7 см. Чтобы получить природную матрицу, по свойствам превосходящую все то, что можно сделать из полимерных трубок, трахею очистили от окружающей соединительной ткани, клеток донора и антигенов гистосовместимости. Очищение заключалось в 25 циклах девитализации с применением 4%-деоксихолата натрия и дезоксирибонуклеазы I (процесс занял 6 недель). После каждого цикла девитализации проводили гистологическое исследование ткани для выявления количества оставшихся ядросодержащих клеток, а также иммуногистохимическое исследование на наличие в ткани антигенов гистосовместимости HLA-ABC, HLA-DR, HLA-DP и HLA-DQ. Благодаря биореактору собственной разработки (рис. 9) ученые на поверхность медленно вращающегося отрезка трахеи равномерно нанесли шприцем суспензию клеток. Затем трансплантат, наполовину погруженный в среду для культивирования, вращался вокруг своей оси с целью попеременного контакта клеток со средой и воздухом.
Рисунок 8. Операция по пересадке пациентке трахеи.
Рисунок 9. Биореактор для создания тканеинженерного эквивалента трахеи. А — схема биореактора, вид с боку. Б — герметизация биореактора. В — биореактор с тканеинженерным эквивалентом трахеи in situ. Г — биореактор после удаления эквивалента трахеи. Д — вид эквивалента трахеи непосредственно перед операцией.
Эквивалент трахеи находился в биореакторе 96 часов; затем его трансплантировали пациентке. При операции был полностью удален главный левый бронх и участок трахеи, к которому он примыкал. В образовавшийся промежуток вшили трансплантат, а некоторое несоответствие диаметров просветов тканеинженерного эквивалента и бронха реципиента было преодолено благодаря эластичности донорской ткани.
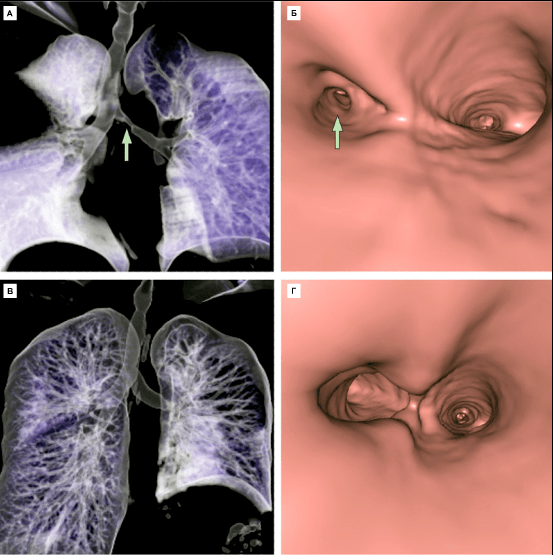
По истечении десяти суток после операции пациентка была выписана из клиники без признаков дыхательной недостаточности и иммунной реакции отторжения трансплантата. По данным компьютерной томографии, с помощью которых была сделана виртуальная 3D реконструкция дыхательных путей, тканеинженерный эквивалент был практически неотличим от собственных бронхов пациентки (рис. 10).
Рисунок 10. Виртуальная 3D-реконструкция дыхательных путей по данным компьютерной томографии и бронхоскопии перед операцией (А, Б) и через 1 месяц и после замены стенозного участка левого главного бронха тканеинженерным эквивалентом (В, Г). Стрелкой указан стеноз.
Источник