Актуальная активная и потенциальная кислотность почв. Изменение почвенной реакции. Известкование кислых почв
Различают актуальную (активную) и потенциальную кислотность почв в зависимости от того, при каком взаимодействии она проявляется и измеряется.
Актуальная кислотность почвы обусловлена наличием водородных ионов (протонов) в почвенном растворе, активность которых зависит от свойств (ионной силы) раствора, влияющих на коэффициент активности иона. Актуальная кислотность почвы измеряется при взаимодействии почвы с дистиллированной водой [водный рН, рНн2о, рН (Н20)] при разбавлении 1:2,5 либо в пасте. Иногда рН почвы измеряют непосредственно в почве при естественной влажности, но для этого она должна быть достаточно увлажненной и гомогенной для обеспечения надежного контакта с измерительным электродом. Можно актуальную кислотность почвы измерять и колориметрически или путем титрования.
Потенциальная кислотность — способность почвы при взаимодействии с растворами солей проявлять себя как слабая кислота. Потенциальная кислотность определяется свойствами твердой фазы почвы, обусловливающей появление дополнительного количества протонов в растворе при взаимодействиях с удобрениями или химикатами.
Кислая реакция солевых вытяжек из почв объясняется появлением в растворе ионов водорода (гидроксония Н30 + ) в результате вытеснения из почвенного поглощающего комплекса, а также взаимодействия с водой молекулярных кислот и гидратиро- ванных катионов. Гидратированные катионы при этом можно рассматривать как кислоты (Бренстед — Лоури). Наиболее сильные кислотные свойства в воде проявляют двух- и особенно трехзарядные катионы металлов
В зависимости от характера взаимодействующего с почвой раствора различают две формы потенциальной кислотности почв — обменную и гидролитическую, характеризующиеся как последовательные этапы выделения в раствор дополнительных количеств протонов из твердой фазы.
Обменная кислотность обнаруживается при взаимодействии с почвой растворов нейтральных солей. При этом происходит эквивалентный обмен катиона нейтральной соли на ионы водорода, алюминия и другие, находящиеся в поглощающем комплексе. Обычно для определения обменной кислотности почв используют 1 н. раствор КС1 (рН около 6,0).
Природа обменной кислотности зависит от состава и свойств почвенных коллоидов. Кислотность органических почвенных коллоидов (гумусовые кислоты) обусловлена главным образом обменным водородом, причем непосредственным источником обменного водорода служат органические кислоты, включая гумусовые, и угольная кислота. При взаимодействии с коллоидами водород этих кислот внедряется в их диффузный слой, занимая место оснований, которые выщелачиваются или выпадают в осадок
Кислотность минеральных коллоидов связана с наличием в почвенном поглощающем комплексе обменных ионов водорода, алюминия или железа. Источником обменных алюминия и железа служат ионы кристаллической решетки глинистых минералов и гидроксидов, мобилизуемые органическими кислотами или присутствующие в почвенном растворе и также внедряющиеся в диффузный слой почвенных коллоидов.
При взаимодействии кислой почвы с раствором хлорида калия в результате обмена калия на водород в растворе появляется соляная кислота, а при обмене на алюминий — хлорид алюминия (III)
Образующаяся в растворе кислота оттитровывается щелочью (кислотность выражается в мг-экв/100 г) или определяется по рН раствора, который в данном случае характеризуется как солевой рН,рНКС1, рН(КС1) По значениям рН можно ориентировочно определить роль различных ионов в образовании кислотности При рН меньше 4,0 кислотность обусловлена главным образом обменным водородом, при рН от 4,0 до 5,5 — обменным алюминием
В кислых почвах (подзолистые, серые лесные, красноземы) солевой рН всегда меньше, чем водный рН, поскольку в этих почвах имеется обменный водород и (или) алюминий Для насыщенных основаниями почв солевой рН не определяется
Гидролитическая кислотность обнаруживается при воздействии на почву раствора гидролитически щелочной соли сильного основания и слабой кислоты, при котором происходит более полное вытеснение поглощенных водорода и других кислотных ионов Для определения гидролитической кислотности обычно используют 1 и раствор CH3COONa с рН 8,2 При взаимодействии уксуснокислого натрия с почвой могут происходить реакции в зависимости от содержания в ней алюминия или водорода, аналогичные приведенным выше
Количество образующейся уксусной кислоты, определяемое титрованием, характеризует гидролитическую кислотность почвы
При наличии в почве обменного алюминия образующийся в результате обменной реакции уксуснокислый алюминий распадается на гидроксид алюминия и уксусную кислоту
Так как нейтральная соль вытесняет лишь часть поглощенного водорода, а гидролитически щелочная соль — почти весь, то гидролитическая кислотность обычно больше обменной Иногда гидролитическая кислотность оказывается меньше обменной за счет поглощения почвой анионов уксусной кислоты и вытеснения ионов ОН , в результате чего уменьшается кислотность вытяжек.
Наличие потенциальной кислотности характерно для почв, обедненных основаниями (Са2+, Mg2+ и др.). Чем больше почва обеднена основаниями, тем резче проявляет она кислотные свойства.
В природе распространение кислых почв связано с определенными условиями почвообразования (подзолистые, бурые лесные, красноземы, желтоземы). Большое значение в образовании почв с той или иной реакцией имеет характер почвообразуюгцей породы. Подзолистые почвы, бедные основаниями, в основном приурочены к выщелоченным, бескарбонатным породам. Характер почвообразовательного процесса откладывает существенный отпечаток на формирование реакции почв. В одних случаях этот процесс приводит к потере оснований и подкислению (подзолистый процесс), в других — наблюдается постепенное обогащение почвы основаниями (дерновый процесс). Большое значение в формировании кислых почв имеют кл и магические условия. Промывной характер водного режима приводит к выносу солей из почвы, способствует выходу в раствор поглощенных С а2 , Mg2+ в обмен на водородные ионы и их последующему выщелачиванию. Растительность также оказывает влияние на характер почвенной реакции. Хвойные леса и сфагнум способствуют усилению кислотности благодаря кислым свойствам их органических остатков; лиственные леса и травянистая растительность благоприятствуют накоплению оснований.
Сельскохозяйственная деятельность человека вызывает изменение почвенной реакции. Само отчуждение урожаев с полей приводит к постепенному обеднению почв элементами, входящими в состав растений, в том числе и основаниями. Длительная обработка почвы в условиях зоны подзолистых почв способствует обеднению ее Са2+ и Mg2+. Снизить рН почвы может и внесение физиологически кислых минеральных удобрений.
Кислая реакция почв неблагоприятна для большинства культурных растений и полезных микроорганизмов. Кислые почвы обладают плохими физическими свойствами. Из-за недостатка оснований органическое вещество в этих почвах не закрепляется, почвы обеднены питательными веществами. Степень отрицательного влияния кислой реакции почв на растения зависит от того, какой элемент является причиной почвенной кислотности — водород или алюминий. Алюминий оказывает на растения более сильное токсическое действие, чем водород. Так, при повышении содержания обменного алюминия до 10—12 мг/100 г наблюдается выпадение клевера в посевах. Опытами Н. С. Авдонина показано, что наличие в кислых почвах обменного алюминия служит причиной гибели посевов озимых зерновых культур при перезимовке.
Доля участия в почвенном поглощающем комплексе обменных катионов водорода и алюминия, определяемых как обменная или гидролитическая кислотность, характеризует ненасыщенность почв основаниями
Степень насыщенности почв основаниями — это количество обменных оснований (обычно Ca2 + + Mg2 + ), выраженные в процентах от емкости поглощения
K=S/Е- 100=S/(S+#> • 100, (40)
где V — степень насыщенности основаниями, %, S — сумма обменных оснований, мг-экв/100 г, Е — емкость поглощения, мг- экв/100 г, Н— гидролитическая кислотность, мг-экв/100 г
Таким образом, ненасыщенность почв основаниями характеризуется разностью между емкостью поглощения при избранном значении рН и содержанием в почве обменных оснований
Основным методом повышения продуктивности кислых почв, снижения их кислотности служит известкование
При внесении извести СаС03 при наличии избытка углекислоты переходит в растворимый Са(НС03)2, который взаимодействует с почвой по следующей схеме
]2Н + + Са(НС03)2 —> [ППК2 ] Са2++ 2Н20 + 2С02
Почвы с высокой степенью насыщенности не нуждаются в известковании Путем сопоставления степени насыщенности почв с отзывчивостью на известкование в полевых опытах установлена следующая примерная шкала
Обычно доза извести рассчитывается по гидролитической кислотности пахотного слоя почвы
При плотности почвы 1,3 г/см3 ее масса в 20-сантиметровом пахотном слое на 1 га составляет 2600 т При этом каждый 1 мг-экв гидролитической кислотности на 100 г почвы требует для нейтрализации 1,3 т СаС03 на 1 га Однако обычно используется не полная доза извести, рассчитанная по гидролитической кислотности, а лишь какая-то часть ее, определяемая в соответствии со свойствами выращиваемых культур
Дозу СаС03 для известкования кислых почв определяют и по обменной кислотности, показателем которой служит солевой рН, в соответствии со следующими критериями, приведенными в табл 37
Таблица 37. Дозы извести в зависимости от рН солевой суспензии и гранулометрического состава почвы (в т/га)
Гранулометрический рН солевой суспензии
4,5 и ниже 4,6 4,8 5,0 5,2 5,4-5,5
Супеси и легкие суглинки 4,0 3,5 3,0 2,5 2,0 2,0
Средние и тяжелые суглинки 6,0 5,5 5,0 4,5 4,0 3,5
Источник
Показатель pH почвы (как определить кислотность почвы)
Большинство растений предпочитают слабокислые и нейтральные почвы. Но если грунт сильнокислый или щелочной, выращивать на нем даже неприхотливые растения сложно. Для определения кислой, нейтральной или щелочной среды почвы используют показатель pH.
Содержание
Показатель pH — специальный показатель, отражающий кислотно-щелочной баланс почвы. В этом материале даны понятия что такое показатель pH, какие типы почвы (от слабокислой до сильнощелочной) соответствуют численным значениям показателя рН, а также способы для его определения или измерения.
ЧТО такое показатель pH почвы
Кислотность показывает концентрацию ионов водорода, определяющих кислотно-щелочной баланс грунта. Для этого есть показатель pH. Показатель, отражающий кислотно-щелочной баланс почвы, раствора или другой среды. Измеряется в единицах от 0 до 14 (см таблицу):
| Значение показателя pH | Характеристика |
| 0 … 6,9 | среда кислая (преобладают кислоты) |
| 7,0 | среда нейтральная (кислоты и щелочи нейтрализуют друг друга). |
| 7,1 … 14 | среда щелочная (преобладают щелочи). |
| Примечание: а) чем больше pH: тем меньше кислотность почвы; тем больше щелочность почвы. б) чем меньше pH: тем больше кислотность почвы; тем меньше щелочность почвы. |
Показатель pH почвы (его численное значение) чаще всего колеблется в диапазоне 3,5-8,5.
Типы почвогрунтов, в зависимости от показателя pH принято разделять на следующие типы (см. таблицу):
| Значение показателя pH | Тип почвы |
| менее 4 | сильнокислая |
| 4 … 5 | среднекислая |
| 5 … 6 | слабокислая |
| 6 … 7 | нейтральная |
| 7 … 8 | слабощелочная |
| 8 … 8,5 | среднещелочная |
| более 8,5 | сильнощелочная |
Также принято различать два типа кислотности — актуальную кислотность (отражает реальное состояние, сколько сейчас в почве есть ионов водорода) и потенциальную кислотность (потенциально возможное состояние):
- АКТУАЛЬНАЯ определяет присутствие в почве ионов водорода: чем их больше, тем выше кислотность (соответственно, тем меньше значение pH).
- ПОТЕНЦИАЛЬНАЯ определяет присутствие в почве обменно поглощенных ионов водорода и других частиц – марганца, железа, алюминия.
Всем садоводам и огородникам следует ориентироваться ТОЛЬКО на актуальную кислотность, которая измеряется химическими индикаторами, приборами и другими способами. Далее рассмотрим как определить показатель pH почвы.
КАК определить показатель pH почвы (кислотность почвы)
Способов определения множество – это и «народные» (с использованием уксуса или лакмусовой бумаги), и современные (с применением электронных приборов pH-метров/ кислотомеров).
Самые распространенные способы определения кислотности почвы:
- Лакмусовой бумагой;
- Измерительные приборы pH-метры;
- Визуальный способ (по растениям-маркерам);
- С помощью уксуса;
- Заказ исследование почвы в лаборатории.
а) Лакмусовая бумага
Показатель pH почвы определяется по цвету бумаги. Лакмусовая бумага есть в продаже в любом садовом центре.

б) Измерение pH-метром (кислотомером)
Для определения кислотности разработаны и внедрены в производство целый ряд pH-метров (кислотомеров) – специальных портативных приборов, позволяющих определять не только кислотность, но и другие ключевые показатели почвы – влажность, температуру, освещённость и пр.
pH-метр — это прибор для измерения водородного показателя, характеризующего активность ионов водорода в растворах/средах (почва, вода, пищевая продукция и сырье, объекты производственных системах, в том числе в агрессивных средах). Действие pH-метра основано на измерении величины ЭДС электродной системы, которая пропорциональна активности ионов водорода в растворе — pH (водородному показателю).
Для использования в ЛПХ и в сельскохозяйственном производстве выпускается широкий ряд простых в применении электронных или электронно-механических pH-метров. Популярность их из года в год растет. Это самый точный и актуальный на сегодня способ определения кислотности почвы.

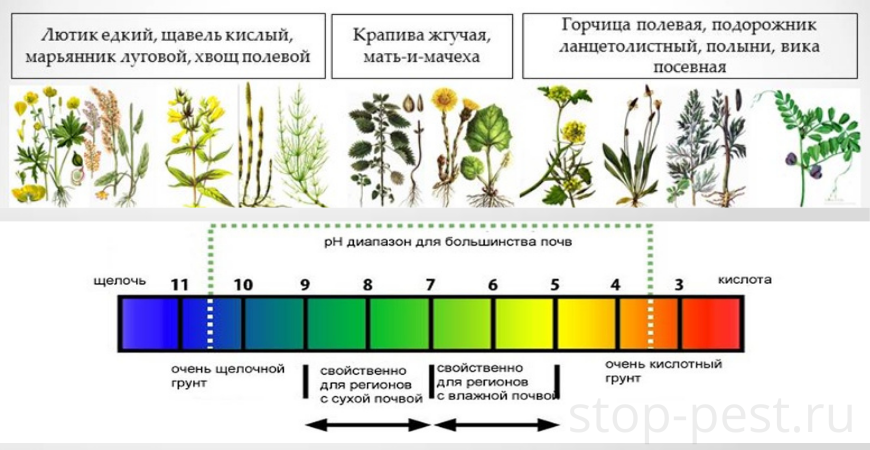
в) Визуальный способ
В данном случае речь идет по определению кислотности почвы по растениям – маркерам. Например, если на участке хорошо растет щавель и хвощ, то почва кислая, а если мак и вьюнок – щелочная.
| Значение pH | Тип почвы | Растения-маркеры |
| менее 4 | сильнокислая | растений нет, на верхнем слое бархатистый зеленый налет |
| 4 … 5 | среднекислая | подорожник, дикий щавель, мята дикая, хвощ, фиалка и др. |
| 5 … 6 | слабокислая | папоротник, ромашка, пырей, одуванчик, сныть обыкновенная, клевер, мать-и-мачеха и др. |
| 6 … 7 | нейтральная | мокрица, лебеда, пастушья сумка, |
| более 7 | щелочная | мак, вьюнок, дрема белая |
г) С помощью уксуса
В плоскую емкость помещается небольшое количество почвогрунта. Затем заливается 6% раствором уксуса. По реакции определяем кислотность почвы:
- реакции нет, то почва кислая;
- реакция слабая (мало пузырьков) — почва слабокислая или близкая к норме;
- реакция бурная — значит, щелочная среда.
д) Заказать исследование почвы в лаборатории
Раскисление почвы
Раскисление почвы – единственный способ поднять ее рН до нужной отметки (т. е. до 5,0 и выше). Раскисление почвы процесс не сложный, но требует определенных знаний. Процесс не быстрый, около полугода. Осень самое благоприятное время, чтобы к весне кислотно-щелочной баланс почвы был на оптимальном уровне.
Для раскисления используют следующие способы/материалы:
Источник
